Thiele管熔点测定
实验目的 1、了解熔点测定的概念、特点和意义。
2、掌握测定熔点的操作。
实验原理
(一)测熔点时几个概念
熔点:是指固体物质在一定大气压下,固液两相达到平衡时的温度。一般可以 认为是固体物质在受热到一定温度时,由固态转变为液态,此时的温度即为该物质 的熔点。
熔程:固体物质从开始熔化到完全熔化的温度范围即为熔程(也叫熔点范围)。
初熔:固体刚开始熔化的温度(或观察到有少量液体出现时的温度)。
全熔:固体刚好全部熔化时的温度。
(二)熔点测定的特点:
操作正确时,纯的有机化合物一般都有固定的熔点,熔程不超过0.5-1℃。混有杂质时,熔点会降低,熔程增大。
(三)熔点测定的意义
纯净的固体有机物一般都有固定的熔点,因此通过测定熔点可鉴定有机物,还能区别熔点相近的有机物。
根据熔程的长短可检验有机物的纯度。一般,有机物纯度越高,熔程越短;纯度越低,熔程越长。反之亦然。
实验仪器及其规格
温度计 提勒管(b形管) 熔点毛细管 酒精灯 开口橡皮塞 玻棒 玻管 表面皿 250ml圆底烧瓶等。
测定熔点的仪器装置
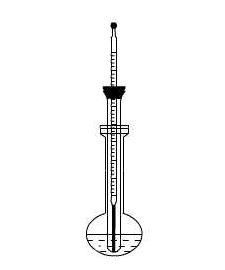
实验图25 提勒管式熔点测定装置 实验图26 双浴式熔点测定装置
操作步骤
1、填装样品:将待测样品(样品一定要干燥)放在洁净、干燥的表面皿中,用玻璃钉研细,装入熔点管中,往毛细管内装样品时,一定要反复冲撞夯实,管外样品要用卫生纸擦干净,高度2-3 mm。
2、安装装置:将提勒管固定在铁架台上,装入浴液,按实验图25所示安装,温度计及毛细管的插入位置要精确。
3、准备热浴:一般选用浓硫酸作浴液(适用于测熔点在220℃以下的样品),要注意浓硫酸的安全使用。
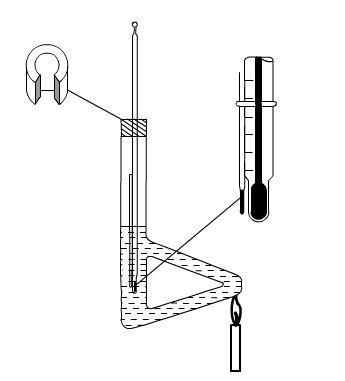
4、加热:用酒精灯在提勒管弯曲处的底部加热。注意升温速度的控制。
5、读数:当发现样品出现潮湿时,表明固体开始熔化,记录初熔温度。当固体完全熔化,呈透明状态时,记录全熔温度。这两个温度值就是该化合物的熔程。
6、平行实验:熔点的测定至少要有两次重复的数据。每一次测定都必须用新的熔点管,装新样品。进行第二次测定时,要等浴液冷却至样品熔点以下约20℃左右再进行。
7、拆除装置:先擦干温度计上的浓硫酸再水洗,浓硫酸回收。
注意事项
1、熔点管本身要干净,如有灰尘等,能产生4-10℃的误差。管壁不能太厚,封口要均匀。熔点管底未封好会产生漏管。熔点管壁太厚,热传导时间长,会产生熔点偏高。
2、样品粉碎要细,填装要实,否则产生空隙,不易传热,造成熔程变大。样品不干燥或含有杂质,会使熔点偏低,熔程变大。样品用量要适中,样品量太少不便观察,而且熔点偏低;太多会造成熔程变大,熔点偏高。
3、实验中,加热时,升温速度不宜太快,让热传导有充分的时间。升温速度过快,熔点偏高。
4、使用硫酸作加热浴液要特别小心,不能让有机物碰到浓硫酸,否则使浴液颜色变深,有碍熔点的观察。若出现这种情况,可加入少许硝酸钾晶体共热后使之脱色。
数据记录和处理
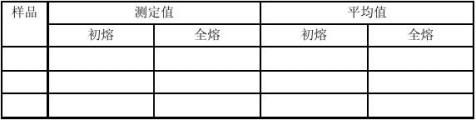
实验表1-1 熔点测定数据记录表
思考
1、测熔点时,若有下列情况将产生什么结果?
(1)熔点管壁太厚。
(2)熔点管不洁净。
(3)样品未完全干燥或含有杂质。
(4)样品研得不细或装得不紧密。
(5)加热太快。
(6)样品装得太多。
2、熔点毛细管是否可以重复使用?
3、如何检验两种熔点相近的物质是否为同一纯净物?
第二篇:熔点的测定
熔点的测定
熔点是有机化合物最重要的物理常数之一,常以m.p.表示。它不仅可以用来鉴定固体有机物,同时根据熔程(自初熔至全熔的温度范围)的长短可定性地判别该物质的纯度。此外,根据混合熔点是否下降,还可以判断熔点相同的化合物是否是同一种物质。
1.基本原理
物质的熔点是指该物质的固液两态在大气压力下达到平衡时的温度。纯的固体有机化合物一般都具有固定的熔点,即在大气压力下,固液两态之间的变化非常敏锐,熔程不超过0.5~1℃,但如混有杂质时,则其熔点下降,且熔程也较长。
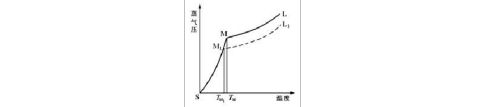
纯物质的熔点可以从蒸气压与温度的变化曲线(图1)来理解。固态蒸气压—温度曲线SM的变化速率比相应的液态蒸气压—温度曲线 ML的变化速率大,因而两曲线相交在M点,这时的温度TM即为该物质的熔点。只有在此温度时,固液两相的蒸气压才相等,固液两相才达到平衡,这就是纯晶体物质有固定熔点的原因。当温度消超过TM,即使很小的变化时,只要有足够的时间,固体就可以全部转变为液体。因此,为了精确测定熔点,在接近熔点时加热速度一定要缓慢,这样才能使熔化过程尽可能接近于两相平衡的条件。
若化合物含有杂质,并假定两者不生成固溶体,则根据拉乌尔定律,在一定压力和温度下,在溶剂中增加溶质的量,将导致溶剂蒸气分压的降低,所以出现新的液态曲线M1L1,在M1点建立新的平衡,相应的温度为 TM1,即发生熔点下降。应当指出,如有杂质存在,融化过程中固相和液相平衡时的相对量在不断改变,因此两相平衡时不是一个温度点TM1,而是从最低共熔点(与杂质能共同结晶成共熔混合物,其熔化的温度称之为最低共熔点)到TM1一段。这说明杂质的存在不但使初熔温度降低,而且还会使熔程变长,所以在测熔点时一定要记录初熔和全熔的温度。
图1 蒸气压—温度曲线
将杂质加入纯化合物中产生熔点下降的方法也可用于化合物的鉴定。通常把熔点相同的两个化合物混合后测定的熔点称为混合熔点。如混合熔点仍为原来的熔点,一般可认为两个化合物相同。如混合熔点下降,且熔程也长,则可确定这两种物质不是相同的物质。测定时一般将两个样品以1﹕9、1﹕1、9﹕l三种不同比例的混合样品分别测其熔点,以比较测得的结果。混合熔点的测定虽然也有少数例外,但对于鉴定有机化合物,验证两化合物是否是同一物质仍有很大的实用价值。
2.毛细管法测熔点
该法操作简便,样品用量少。虽然测得的熔点往往略高于标准熔点,但已能满足一般要求,是常用的测定方法,具体操作如下:
(1)熔点管的制备参见玻璃工操作部分。
(2)样品的装入
将少许待测的干燥样品置于干净的表面皿上,研成细的粉末,并集成小堆。将熔点管开口端向下反复插入粉末中几次。取一根长约30~40 cm的干净玻璃管,垂直于另一表面皿上,将熔点管开口端朝上。从玻璃管上端自由落下,上下弹跳几次,使晶体振落于熔点管底部。如此重复数次,能使样品填装紧密。样品高度为2~3mm,装入样品如有空隙,将导致传热不均匀,影响测定结果。粘附于管外的粉末必须拭去,以免污染浴液。
(3)加热装置
有各种形式的加热装置,但实验室最常用的是提勒管,又称b形管(图 2)。管口装有开口软木塞或橡胶塞(必须有开口与大气相通,否则会造成爆炸事故),温度计插入其中,刻度应面向胶塞开口处,水银球位于b形管上下两叉管口中间。b形管内装入浴液(加热液体),液面至上叉管处即可,因为加热时浴液体积会增大。采用水、石蜡或硅油作浴液时,装好样品的熔点管用橡皮圈套在温度计上;采用浓硫酸作浴液时,可借少许浓硫酸粘附于温度计下端,使熔点管的底部正靠在水银球侧面的中部。在图示的侧管部位用小火加热,受热时浴液以对流方式传至管内各部分,因此不需要任何搅拌,就能使浴液温度均匀上升。
图 2 提勒管测熔点
所用的溶液通常有水、浓硫酸、石蜡及硅油等。硫酸价格便宜,使用普遍,但腐蚀性强。高温时会分解放出三氧化硫,故加热不宜过快,使用时要倍加小心,并戴上防护眼镜。硫酸适用于测定250℃以下的熔点,若熔点在250℃以上时,可用硫酸和硫酸钾(7﹕3)混合液作为浴液。当有机物使硫酸颜色变深并妨碍观察时,加入几颗硝酸钾晶体,加热后即可褪色。石蜡比较安全,但容易变黄,分解温度为 220℃,一般在170℃以下使用。硅油不易燃,在相当宽的温度范围内粘度变化不大,温度可达250℃,是较理想的浴液。
(4)熔点的测定
将b形管垂直夹于铁台上,以浓硫酸作为浴液时,将粘附有熔点管的温度计仔细地插入其中,不要使熔点管漂移。以小火在图示部位加热,开始升温速度可以快些,到与熔点差约15℃时,调整火焰使每分钟上升约1~2℃,越接近熔点升温速度越要缓慢。掌握升温速度是准确测定熔点的关键,这样一方面是为了保证有充分的时间让热量由熔点管外传至管内,使样品熔化;另一方面因操作者不能同时观察温度计读数和样品的变化情况,只有缓慢加热才能使此误差减小。记录熔点时要记下样品开始塌落并有液相产生(初熔)和固体完全消失时(全熔)的温度计读数。例如,初熔温度156℃,全熔温度158℃,则熔点应记录为156~158℃,而不是它们的平均值157℃,因为这样所表示的熔程完全不同,前者为2℃,而后者则为0℃。
在加热过程中如有分解、变色、萎缩或升华等现象也应如实记录。容易分解的样品在低于熔点时就会分解变色,分解的产物作为杂质使样品熔点下降,下降情况与加热的快慢或所含的分解物多少有关。如硫脲快速加热时,分解物少,熔点为180℃。反之,熔点可下降至167~172℃。有的样品在熔化时伴随着分解变色或发泡,这时的熔点也称为分解点。如丙二酸的熔点为135℃(分解),表示该物质在135℃熔化,同时也发生分解(也可能不熔化而直接分解)。许多样品在熔化前瞬间会发生软化或萎缩,这并不代表分解,而是晶体结构的一种改变。有的样品加热时有液体凝结在熔点管壁,可能是放出结晶溶剂的缘故,不要误认为是初熔。有的样品蒸气压较高,在熔化时或熔化前发生升华,则可把样品放在两端封闭的熔点管内,并全部浸入浴内测定,因为压力对熔点的测定影响不大。
毛细管法也能测定低熔点(-50℃以上)的样品,通常是把熔点管内的样品放在一个盛有干冰—甲醇致冷剂的大烧杯中固化,然后在搅拌下缓慢微热致冷剂,使样品熔化并记录熔点。
测定熔点至少要有两次重复数据,一般一个样品要测定3~5次,重复数据的次数越多,说明该熔点数据越可靠。每次测定必须用新的熔点管装样品。若要测定高熔点样品或熔点是未知的,为了节约时间,可对样品快速试测一次,以测得近似的熔点。待浴温冷至熔点以下 20℃,再另取一份样品缓缓加热作准确的测定。
b形管内的硫酸要冷却到用手可以触摸时才能倒入回收瓶中,温度计应冷却后用纸擦去硫酸方可用水冲洗,以免水银球破裂。
3.显微熔点测定法
这种测定方法要用显微熔点测定仪。测定时样品用量更少,只需几颗小粒晶体。在显微镜下能清楚地看到样品受热变化的过程,如升华、分解、脱水和多晶形物质的晶型转化等。操作时先将专用的载玻片用丙酮洗净,用擦镜纸擦干,放在一个可移动的支持器内,然后将研细的样品小心地放在载玻片的中央。另取一载玻片盖住样品,使样品位于加热台的中心空洞上,并盖上保温圆玻璃盖。加热台旁边插有校正过的温度计或热电偶。打开照明灯,调节焦距使从镜头中可以看到晶体外形。开启加热器,用变压器调节加热速度,当接近样品熔点时,控制温度使每分钟上升1~2℃,把样品的结晶棱角开始变圆时的温度作为初熔温度,结晶完全消失时的温度作为全熔温度。熔点测好后应停止加热,稍冷片刻后用镊子取出载玻片,将一厚铝块置于加热台上加快冷却,然后清洗载玻片以备再用。
如要测定混合熔点,应将两种样品各取少许放在载玻片上,让其彼此靠近,用另一载玻片轻压并稍微转动一下,使样品紧密接触后进行测定,其它操作同上。
