实验二 熔点的测定
一、实验目的
1.了解熔点测定的意义。
2.掌握熔点测定的操作方法。
3.了解利用对纯粹有机化合物的熔点测定校正温度计的方法。
4.掌握热浴间接加热技术。
二、实验原理
晶体化合物的固液两态在大气压力下成平衡时的温度称为该化合物的熔点。纯粹的固体有机化合物一般都有固定的熔点,即在一定的压力下,固液两态之间的变化是非常敏锐的,自初熔至全熔(熔点范围称为熔程),温度不超过0.5-1℃。如果该物质含有杂质,则其熔点往往较纯粹者为低,且熔程较长。故测定熔点对于鉴定纯粹有机物和定性判断固体化合物的纯度具有很大的价值。

如果在一定的温度和压力下,将某物质的固液两相置于同一容器中,将可能发生三种情况:固相迅速转化为液相;液相迅速转化为固相;固相液相同时并存。
上图(1)表示该物质固体的蒸气压随温度升高而增大的曲线;
上图(2)表示该物质液体的蒸气压随温度升高而增大的曲线;
上图(3)表示(1)与(2)的加合,由于固相的蒸气压随温度变化的速率较相应的液相大,最后两曲线相交于M处(只能在此温度时),此时固液两相同时并存,它所对应的温度TM即为该物质的熔点。
上图(4)当含杂质时(假定两者不形成固溶体),根据拉乌耳(Raoult)定律可知,在一定的压力和温度条件下,在溶剂中增加溶质,导致溶剂蒸气分压降低(图中M1L’1),固液两相交点M1即代表含有杂质化合物达到熔点时的固液相平衡共存点,TM1为含杂质时的熔点,显然,此时的熔点较纯粹者低。
三、课堂内容
1.通过提问检查学生预习情况(CAI课件预习及实验书预习),提问内容如下:
(1)什么是熔点? 测定熔点有何意义?
(2)什么是熔程?纯净的固体有机化合物的熔程是多少?物质不纯时熔点及熔程有何变化?
(3)测熔点时样品为什么要研细,装实?
(4)油浴温度下降多少时再换另一根样品管?
(5)熔点管中装样品多少?
(6)当接近熔点时加热速度为多少?
(7)做本实验时应注意什么?
2.让学生演示安装及操作并讲解。
3.教师讲解熔点测定仪的使用与操作方法及注意事项。
四、课堂学生测试的样品

五、仪器、药品
仪器:①Thiele管;②200℃温度计;③熔点管、长玻璃管(60cm);④表面皿(中号)、锉刀、切口软木塞、胶塞、橡皮圈⑤数字熔点仪、镊子等。⑥酒精灯
药品:未知物1苯甲酸;未知物2水杨酸;浓硫酸(热载体);工业酒精
六、实验步骤
1.熔点管的制备(参见相关实验)
2.向熔点管填装样品
样品粉末要研细,取少许研细干燥的待测样品于表面皿上,并聚成一堆。将熔点管开口向下插入样品中,然后将熔点管开口向上轻轻在桌面上敲击,使样品进入熔点管,再取约40cm的干净玻璃管垂直台面上,把熔点管上端自由落下,重复几次使样品填装紧密均匀,以达到测熔点时传热迅速均匀的目的。样品高度约2-3mm。装好后去除沾在熔点管外的样品,以免沾污热浴。一次熔点测定一般同时装好4根熔点管。对于易升华或易吸潮的物质,装好后立即把毛细管口用小火熔封。
3.热浴的选择与装配仪器
根据样品的熔点选择合适的加热浴液。加热温度在140℃以下时,选用液体石蜡或甘油。温度低于220℃时可选用浓硫酸,因硫酸具有较强的腐蚀性,所以操作时应注意安全。
向b形管中加入浴液至支管之上1cm处。然后固定在铁架台上;毛细管底部应位于温度计水银球中部,用橡皮圈或线绳将毛细管固定在温度计上,橡皮圈不能浸入浴液;用b形管时,温度计的水银球应处于两侧的中部,不能接触管壁。
4.校正温度计
将已知样品放入热浴中,测定其熔点,将测定值与文献值对照,其差值即为校正系数。
5.测定
(1)粗测
若未知物的熔点,应先粗测一次。粗测加热可稍快,升温速率约5-6℃/min。到样品熔化,记录熔点的近似值。
(2)精确测定
测定前,先待热浴温度降至熔点约30℃以下,换一根样品管,慢慢加热,一开始5℃/min,当达到熔点下约15℃时,以1-2℃/min升温,接近熔点时,以0.2-0.3℃/min升温,当毛细管中样品开始塌落和有湿润现象,出现下滴液体时,表明样品已开始熔化,为始熔,记下温度,继续微热,至成透明液体,记下温度为全熔。
①熔点测定至少要进行2次,2次的数据应一致。每次测定必须用新装样品的毛细管,不可用已测过熔点的样品管。对于未知熔点的测定,可先以快速加热粗测,然后待浴液冷却至熔点以下约30℃左右时,再做精密的测定。
②通常在熔程为0.5-1.0℃时化合物则被认为是纯物质。
③物质熔点测定是有机化学工作者常用的一种技术,所得的数据可用来鉴定晶体的有机化合物并作为该化合物纯度的一种指标。
七、装置图
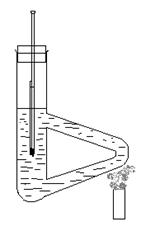
八、注意事项
1.实训完毕,待浴液冷却后,将浴液倒回原瓶中,用滤纸擦去温度计上的浴液冷却后,用水冲洗,以免温度计水银球破裂。
2.样品要研细、装实,使热量传导迅速均匀。样品高度2-3mm,沾附于管外粉末必须擦去,以免污染加热浴液。
3.控制升温速度,开始稍快,当传热液温度距离该化合物熔点约10℃时,调整火焰上升速度为1-2℃/min,愈接近熔点,升温速度愈慢,使0.2-0.3/min。
4.仪器的装配一般是从下向上,从左到右,先难后易逐个地装配,拆卸时,按照与装配时相反的顺序,逐个拆除。
5.仪器用铁夹牢固地夹住,不宜太松或太紧,铁夹不能与玻璃直接接触,应套上橡皮管,垫上石棉网,需要加热的仪器,应夹住仪器受热最低的位置,冷却管则应夹在中间部分。
6.每个样品测三次(粗测一次,细测两次)。
7.注意观察温度计的温度。
8.油浴温度下降30℃以下时更换另一根管。
9.用熔点测定仪测熔点时,取放盖玻片和隔热玻璃时,一定要用镊子夹持,严禁用手触摸,以免烫伤(因熔点热台属高温部件)。
10.温度超过250℃时,浓硫酸发生白烟,防碍温度的读数,在这种情况下,可在浓硫酸中加入硫酸钾,加热使成饱和溶液,然后进行测定。
11.在热浴中使用的浓硫酸有时由于有机物掉入酸内而变黑,防碍对样品熔融过程的观察,在这种情况下,可以加入一些硝酸钾晶体,以除去有机物质。
九、熔点测定可能产生误差的因素
1.熔点管不洁净。如含有灰尘等,能产生4-10℃的误差。
例如,熔点管内壁含有碱性物质,能催化醛或酮的羟醛缩合,或使糖类及其衍生物发生变旋作用,而使熔点降低,熔程变大;故熔点管必须洁净。
2.点管底未封好而产生漏管。检查是否为漏管,不能用吹气的方法,否则会使熔点管内产生水蒸气及其它杂质。检查的方法为:当装好样品的毛细管浸入浴液后,发现样品变黄或管底渗入液体,说明为漏管,应弃去,另换一根。
3.样品粉碎不够细。填装不结实,产生空隙,则不易传热,造成熔程变大。
4.样品不干燥或含有杂质。根据拉乌耳(Raoult)定律,会使熔点偏低,熔程变大。
5.样品量的多少也会影响。太少不便观察,产生熔点偏低;太多会造成熔程变大,熔点偏高。
6.升温速度应慢,让热传导有充分的时间。升温速度过快,熔点偏高。
7.熔点管壁太厚,热传导时间长,会产生熔点偏高。
归纳上述因素为四个:
(1)熔点管规范(包括规格、管底封闭、洁净等)。
(2)样品合格(包括干燥、粒度等)。
(3)样品填装符合要求(量的多少、填充结实与否)。
(4)升温速度。
十、实验要求
1.准确测试样品的熔点。
2.实验后上交实验报告。
十一、讨论题
1.测定熔点时产生误差的因素有哪些?
2.毛细管法与数字熔点仪法测熔点的优缺点各是什么?
3.两个样品的熔点相同,能否确定它们是同一种物质?
4.测定熔点时,下列情况对实验结果有何影响?
(1)加热过快 (2)样品中有杂质 (3)熔点管太厚
(4)熔点管不干净 (5)温度计未校正
5.若样品研磨的不细,对装样品有什么影响?对测定有机物的熔点数据是否可靠?
6.加热的快慢为什么会影响熔点?在什么情况下加热可以快一些,而在什么情况下加热则要慢一些?
7.是否可以使用第一次测定熔点时已经熔化了的有机化合物再做第二次测定呢?为什么?
第二篇:二元合金平衡相图测定实验指导书
二元合金平衡相图测定实验指导书
一、实验目的
熟悉用热分析法测定金属与合金的临界点,并根据临界点画出二元合金相图。
二、实验原理
相图是一种表示合金状态随温度、成分而变化的图形,又称状态图或平衡图。根据相图可以确定合金的浇注温度,进行热处理的可能性,形成各种组织的条件等。
到目前为止,几乎所有的相图都是通过实验测定出来的。金属及合金的状态发生变化将引起其性质发生变化,例如液体金属结晶或固态相变时将会产生热效应,合金相变时其电阻、体积、磁性等物理性质亦会发生变化。金属及合金发生相变时(包括液体结晶和固态相变)引起其某种性质变化所对应的温度称为临界温度,又称临界点。因此可以通过测定金属及合金的性质来求出其临界点。把这些临界点标注在以温度为纵坐标、成分为横坐标的图上,然后把各个相同意义的临界点连接成线,就构成了完整的相图。可见,相图的建立过程就是金属与合金临界点的测定过程。
测定金属与合金临界点的方法很多,如热分析法、热膨胀法、电阻测定法、显微分析法、磁性测定法、 X 射线分析法等,但其中最常用、最基本的方法是热分析法。
热分析法是通过测量、记录金属或合金在缓慢加热或冷却过程中温度随时间的变化来确定其临界点。测定时将金属自高温缓慢地冷却,在冷却过程中每隔相等时间测量、记录一次温度,由此得到温度与时间的关系曲线,称为冷却曲线。
金属或合金在缓冷过程中,当没有发生相变时,温度随时间增加而均匀地降低;一旦发生了某种转变,则由于有热效应产生,冷却曲线上就会出现转折,该转折点所对应的温度就是所求的临界点。因此,测出冷却曲线就可很容易地确定相变临界点。图 3-1 就是根据测定的一组冷却曲线建立相图的实例。
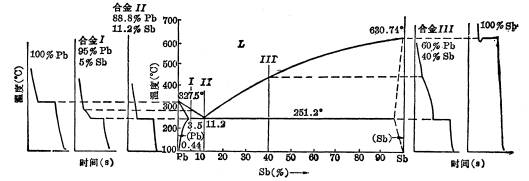
图 3-1 Pb-Sb 二元相图的测定
热分析法简便易行,对于测定由液态转变为固态时的临界点,效果较为明显。但对固态溶解度变化因相变潜热小,难用热分析法测定,需用其它方法。
三、实验设备与温度测量
热分析用实验设备和装置如图 3-2 所示。由图可见,测温装置主要是由热电偶和电位差计组成。

图 3-2 热分析实验装置简图
1- 坩埚电炉 ( 3 ~ 5kw ); 2- 陶瓷坩锅( 30 或 50ml ); 3- 变阻器; 4- 热电偶; 5- 恒温器;
6- 电位差计(或长图自动平衡记录仪); 7- 覆盖剂(木炭粉或石墨粉)
热电偶是由两种不同金属丝所组成,这两种金属丝一端被焊接在一起形成热接点,而未焊接的一端是冷接点(又称自由端),用导线连接在电位差计上。若将热接点加热,则电路中就会产生热电势,它的数值可由电位差计测定。热接点的温度愈高,热电势就愈大,电位差计指针所指的数值也就愈大。
在两端相联的热电偶中所产生的热电势,可由下式决定:
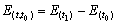 ( 3-1 )
( 3-1 )
式中, E ( t 1 ) 为热接点的热电势,其数值由热接点的温度 t 1 而定。 E ( t 0 ) 为冷接点的热电势,其数值由冷接点的温度 t 0 而定。
当 t 0 为常数,例如 0 ℃时, E ( t 1 , t 0 )= E ( t 1 ) 。这时,热电势可直接由热接点的温度(即加热温度)来决定。当冷接点不是 0 ℃(即 t' 0 )。而增加为 t 0 时,由( 3-1 )式可知,因冷接点温度的改变,热电偶所产生的热电势也发生改变。因而,必须对冷接点的温度进行修正。修正可按下式进行,即:
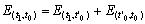 ( 3-2 )
( 3-2 )
( 3-2 )式的实际应用如图 3-3 所示。
例如,设 t' 0 =60 ℃, t 0 =0 ℃,已测知 t 1 温度时热电偶中所产生的热电势 E ( t 1,60 ° ) =31mV, 求 E ( t 1,0 ° ) 。此时,若应用图 3-3 所示的热电偶特性曲线,必须先求出冷接点温度 t 0 =0 ℃时的热电势数值。
E ( t 1,0 ° ) = E ( t 1,60 ° ) + E (60 ° ,0 ° ) , 由图 3-3 可查出 E (60 ° ,0 ° ) =4.03mV 。
∴ E ( t 1,0 ° ) =31+4.03=35.03mV
根据图 3-3 中所示曲线, 36.03mV 的热电势相当于热接点的温度为 441 ℃。
热电偶有很多类型。
此外,热电偶接长图自动平衡记录仪也是目前常用的测温装置,但需配合使用数据放大器或调整仪器内部上限及下限锰铜丝制电阻值。使用该仪器可在记录纸上自动画出冷却曲线。
除热电偶电位差计测温装置外,也可利用水银温度计直接测温;但水银温度计本身受温度影响较大,测温不准确,且易于因预热不当、骤冷骤热而破裂,造成事故。水银温度计最高使用温度为 550 ℃,因此,对较高熔点金属加纯锑等不能使用。
随着科学技术的发展,目前已开始用微处理机来测定冷却曲线,更为简便、可靠。
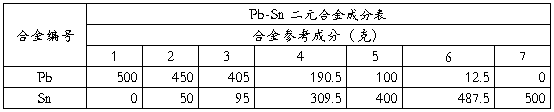
本实验用合金可在 Pb-Sb 或 Pb-Sn 二元合金系中任选一种进行。合金系成分参考下表 。
四、实验步骤
1 .预先配好所选合金系中的七种金属与合金,分别放在陶瓷坩埚中。试验时,各组将合金放在坩埚电炉中加热,待合金熔化后,将热电偶连同保护瓷套管插入金属液中,热电偶的工作端应处于金属液中部,不要靠近坩埚壁、坩埚底或金属液面。热电偶的自由端可以直接接到电位差计上,但此时应考虑自由端温度补偿,接线时要注意电极的正负。
2 .加热升温至金属与合金熔点以上 100 ℃左右,然后关闭电源。为防止金属氧化,应在熔化的金属液面上覆盖一层木炭粉或石墨粉。
3 .当合金开始冷却时,若用人工测温,则需每隔 1min 记录一次电位差计的读数,在临界点附近,可以每隔半分钟作一次记录。
4 .根据所得数据,作出冷却曲线(以热电势—时间或温度—时间为坐标),根据冷却曲线找出临界点。若测得的数值为毫伏数,则应换算成所对应的温度。换算时应考虑自由端的温度及热电偶的误差(各热电偶均有校正表)。根据各组所测得的临界点,建立铅—锑或铅—锡二元合金相图。
五、实验报告要求
1 .每组将本所选定的合金在冷却过程中热电势随时间的变化数据记录于表中。
2 .根据上表记录的数据,用方格纸绘出所测合金的冷却曲
线,并注明合金成分,标注出临界点。
3 .根据各种成分合金的临界点,按比例作出 Pb-Sn 合金相图。
4 .对实验结果进行分析和总结。
