药 品 不 良 反 应 / 事 件 报 告 表
首次报告□ 跟踪报告□ 编码:
报告类型:新的□ 严重□ 一般□ 报告单位类别:医疗机构□ 经营企业□ 生产企业□ 个人□ 其他□
严重药品不良反应,是指因使用药品引起以下损害情形之一的反应:
1) 导致死亡;
2)危及生命;
3)致癌、致畸、致出生缺陷;
4)导致显著的或者永久的人体伤残或者器官功能的损伤;
5)导致住院或者住院时间延长;
6)导致其他重要医学事件,如不进行治疗可能出现上述所列情况的。
新的药品不良反应:是指药品说明书中未载明的不良反应。说明书中已有描述,但不良反应发生的性质、程度、后果或者频率与说明书描述不一致或者更严重的,按照新的药品不良反应处理。
报告时限
新的、严重的药品不良反应应于发现或者获知之日起15日内报告,其中死亡病例须立即报告,其他药品不良反应 30日内报告。有随访信息的,应当及时报告。
其他说明
怀疑药品:是指患者使用的怀疑与不良反应发生有关的药品。
并用药品:指发生此药品不良反应时患者除怀疑药品外的其他用药情况,包括患者自行购买的药品或中草药等。
用法用量:包括每次用药剂量、给药途径、每日给药次数,例如,5mg,口服,每日2次。
报告的处理
所有的报告将会录入数据库,专业人员会分析药品和不良反应/事件之间的关系。根据药品风险的普遍性或者严重程度,决定是否需要采取相关措施,如在药品说明书中加入警示信息,更新药品如何安全使用的信息等。在极少数情况下,当认为药品的风险大于效益时,药品也会撤市。
第二篇:局令第07号附件1药品不良反应/事件报告表
附表1 制表单位:国家食品药品监督管理局
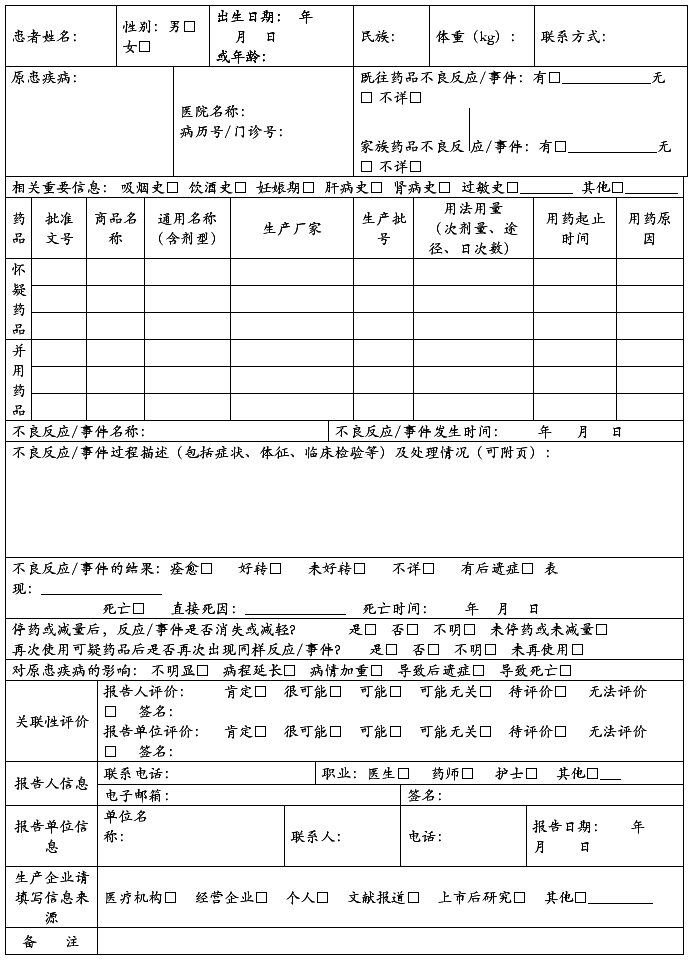
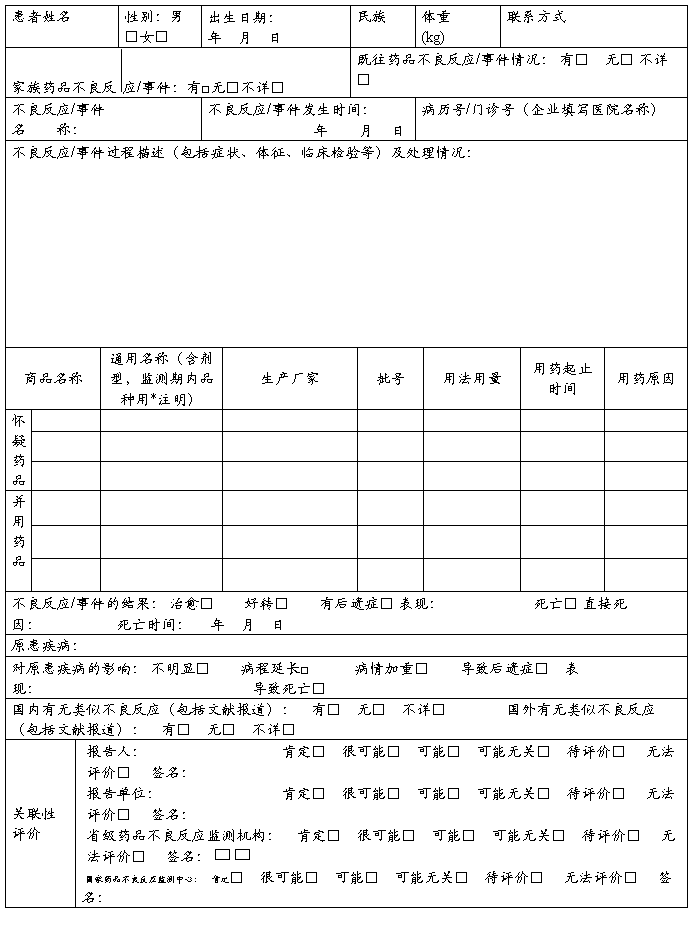
药品不良反应 / 事件报告表
新的□严重□一般□ 医疗卫生机构□ 生产企业经营企业□ 个人□ 编码□□□□□□□□□□□□□□□□□□□
单位名称: 部门: 电话: 报告日期: 年 月 日



报告人职业(医疗机构):医生□ 药师□ 护士□ 其他□ 报告人职务职称(企业): 报告人签名:
◇不良反应/事件分析

◇严重药品不良反应/事件是指有下列情形之一者:
① 引起死亡 □
② 致畸、致癌或出生缺陷 □
③ 对生命有危险并能够导致人体永久的或显著的伤残 □
④ 对器官功能产生永久损伤 □
⑤ 导致住院或住院时间延长 □
◇编码规则:
省(自治区、直辖市) 市(地区) 县(区) 单位 年代 流水号
□□ □□ □□ □□□□ □□□□ □□□□□
注:省(自治区、直辖市)、市(地区)、县(区)编码按中华人民共和国行政区划代码填写。
单位编码第一位如下填写:医疗机构1、军队医院2、计生机构3、生产企业4、经营企业5。
个人报告单位编码一栏填写6000
◇注:通用名称一栏,首次获准进口5年内的进口品种用*注明
国家药品不良反应监测中心 药品不良反应监测中心
通信地址:北京市崇文区法华南里11号楼二层 通信地址:
邮 编:100061 邮 编:
电 话:(010)67164979 电 话:
传 真:(010)67184951 传 真:
E – mail :report@adr.gov.cn E – mail:
新的、严重的药品不良反应/事件病例报告要求
药品生产企业报告要求
1. 填报《药品不良反应/事件报告表》;
2. 产品质量检验报告;
3. 药品说明书(进口药品还须报送国外药品说明书);
4. 产品注册、再注册时间,是否在监测期内(进口药是否为首次获准进口5年内);
5. 产品状态(是否是国家基本药物、国家非处方药、国家医疗保险药品、中药保护品种);
6. 国内上年度的销售量和销售范围;
7. 境外使用情况(包括注册国家、注册时间);
8. 变更情况(药品成分或处方、质量标准、生产工艺、说明书变更情况);
9. 国内外临床安全性研究及有关文献报道情况;
10. 除第1、2项以外,其他项目一年之内如无变更,可以免报。
