表1 听课纪录设计
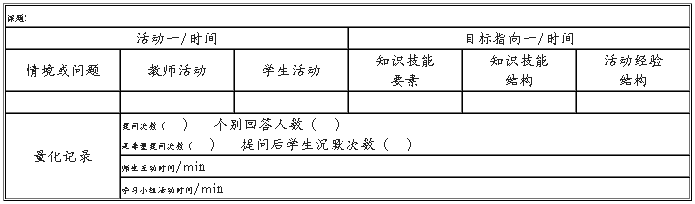
2. 案例分析——“氯气的性质”听课纪录
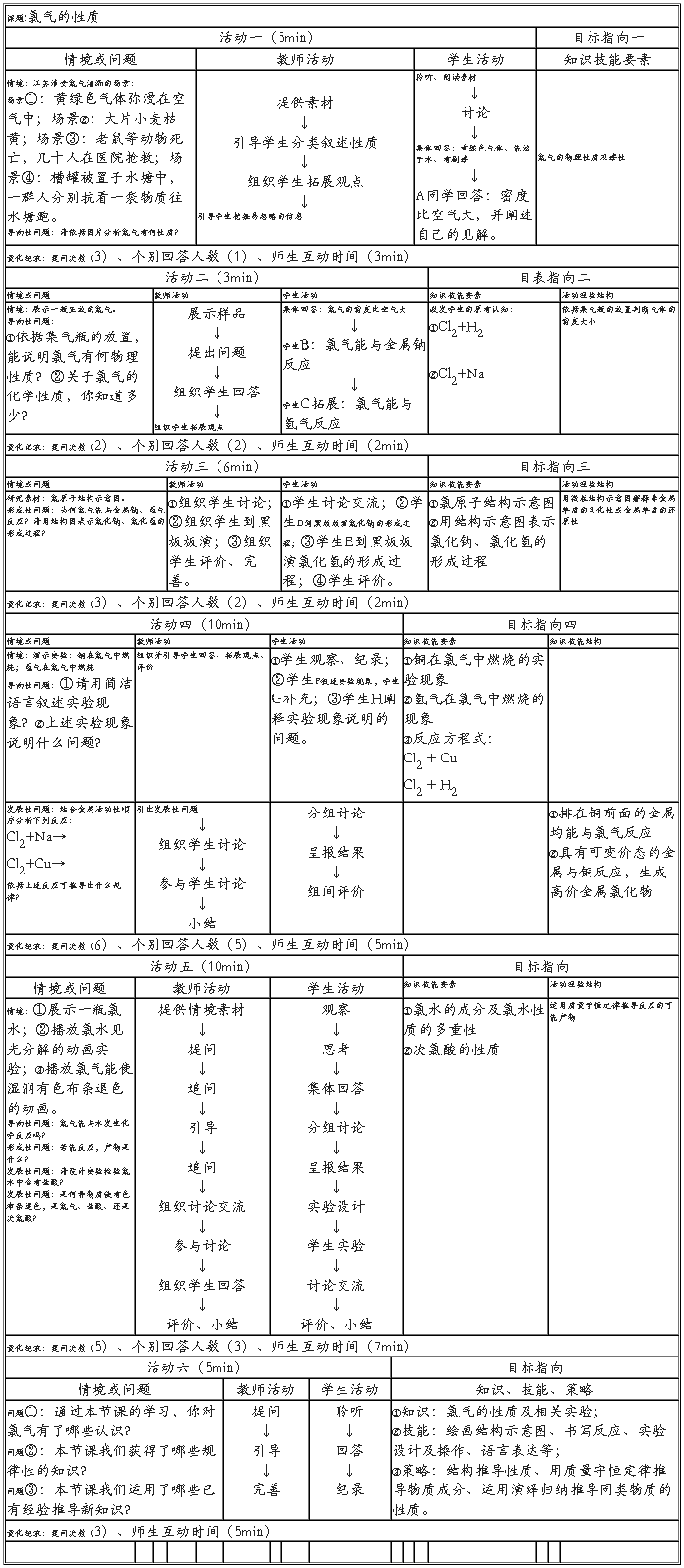
3. 对使用者的建议
3.1灵活运用表1:可以横向纪录活动(情境或问题→教师活动→学生活动)、目标指向(知识技能要素→知识技能结构→活动经验结构),也可纵向纪录。
3.2有目的纪录:对于听课者自认为有价值的东西,必须做好翔实的纪录,这里的详记不是对授课者的口述笔录,而是把听课者的思考及时融入并记录,对于授课者的某些设计或行为,听课者还应及时纪录遗憾。
3.3听课的问题准备:课堂教学中有许多典型事件,这些事件可以从不同角度反映教师在处理这些事件时的行为、态度、思想情感,提出问题的思路等,听课者应及时纪录这些问题,并从教育理论、教学方法、教学艺术的高度进行归纳。
3.4整理听课笔记:这是听课后必不可少的环节,在问题的分类(导向性问题、形成性问题、发展性问题)及目标指向这一块,有时需要听课者在课后进行综合审视才能定夺,因为有些问题及目标指向具有综合性。
二、评课设计的实践研究
1. 评课设计的思维框架
表2 评课设计
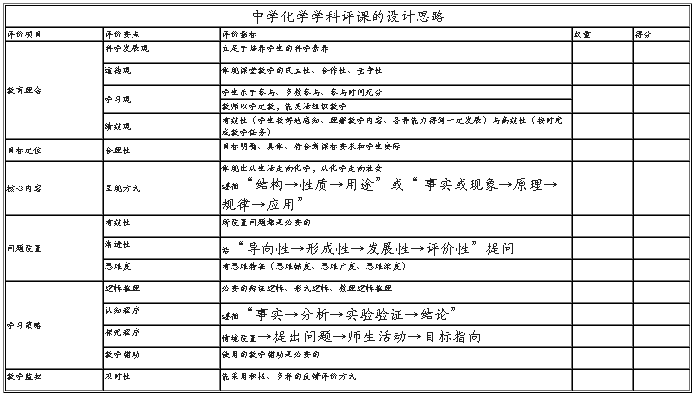
2. 评课的实施——评“氯气的性质”一课
2.1 评教育理念
本节课教师提问次数22次,个别回答次数13次,师生互动时间24分钟,多数学生乐于参与教学,教学中多次使用了对比、类比、演绎、归纳等方法,学生对氯气(含氯水)的性质及相关实验达到了基本了解程度、对分析问题和解决问题的方法达到了基本了解程度、对氯气在生活及生产的影响达到了基本了解程度,基本体现了新课程所倡导的科学发展观、道德观、学习观及绩效观,但教师讲解的时间约占教学总时间的60%,说明本节课没有采用实验探究教学,教学设计还有较大开发空间。
2.2 评目标定位
本节课定位的目标是:了解氯气的物理性质及氯气与铜、氢气反应的现象,理解氯气的化学性质,分析氯气与金属反应的规律及氯气与水反应的产物,基本符合学生的认知能力及课标要求。
2.3 评核心内容
本节课从氯气泄漏事故及氯原子结构出发,引出系列问题,然后结合实验现象,依次呈现出氯气的物理性质、氯气与氢气及铜的反应、氯气与金属反应的规律、氯气与水的反应,充分体现了从生活走向化学及线索引探的思想。
2.4 评问题设置
在本节课中,教师善于设计台阶式问题,从导向性问题到形成性问题再到发展性问题,降低了提问的难度,课堂教学连续性较好。
2.5 评学习策略
本节课通过多媒体播放氯气泄漏的场景及氯水见光分解的动画、展示氯水样品、演示实验,使学生的认识从感性上升到理性;在分析氯气化学性质时,应用了辩证逻辑推理(结构决定性质)及形势逻辑推理(演绎→归纳→演绎),使学生认识从理性抽象到理性具体。可见学习策略的使用是合理且必要的。
2.6评教学监控
本节课主要采用问题讨论综合教学法,评价方式比较单一,缺少一些解决实际问题的题目。
3. 对使用者的建议
3.1 本评课设计属于综合评价指标体系,而综合评价一节课是一项复杂的工作,因此评课时可以找侧重点,从局部上评。
3.2 评课时评价指标可以多样化,其中有四点是应该关注的:一面(课堂的整体效果)、二线(教师教的主线及学生学的主线)、三点(课堂教学的亮点)、四辅助(教学媒体的使用情况)。
第二篇:初中化学课听课记录中学化学评课笔记
初中化学课听课记录中学化学评课笔记
听课时间:2010年9月24日,第二节。
听课地点:C159教室
听课年级:九年级
听课班级:C159
听课学科:化学
上课教师:XX
上课内容:课题3 制取氧气 (第一课时)
教学过程记录:
教师:提出问题
1、请同学们描述一下氧气的物理性质。
2、氧气有哪些化学性质?
3、根据氧气的性质说明氧气有何重要用途。
师生归纳引入:氧气有很多重要用途,那你们想知道氧气是如何制得的吗?
教师:你认为有哪些方法可以获得氧气?
学生:讨论交流
教师演示:展示实验室制取氧气的药品:过氧化氢溶液、高锰酸钾、氯酸钾、二氧化锰,学生观察颜色和状态。
学生演示,教师指导:
1、 在试管中加入约5ml5%的过氧化氢溶液,用带火星的木条伸入试管。
观察:木条没有燃烧。
师生分析原因:
①无氧气放出 ②有氧气放出,但是量太少,不足以让木条复燃。
2、 向上述试管加入少量二氧化锰,用带火星的木条伸入试管。
观察:木条复燃
师生分析原因:
①过氧化氢和二氧化锰发生反应,有氧气生成。
②二氧化锰没有参与反应,但它是过氧化氢发生化学变化的条件,也可能是促进者。
重新加入过氧化氢溶液:
观察:①木条复燃 ②试管底部二氧化锰的量好象没有变化
师生分析原因:二氧化锰没有参与反应,它不是反应物,它的量如果用精密仪器称量,我们会发现并没有发生变化,且还可继续使用,说明二氧化锰的质量、化学性质并没有改变。
学生活动:学生阅读教材,进行小结。
催化剂:在化学反应里能改变其他物质的化学反应速率,而本身的质量和化学性质在反应前后都没有发生变化的物质,也叫触媒。例:汽车排气管有一个尾气处理装置,里面加入了一种催化剂,使会污染空气的一氧化碳和一氧化氮反应生成了无污染的氮气和二氧化碳。
催化作用:催化剂在化学反应中所起的作用。
催化剂用途:
老师强调:
1、改变(加快或减慢)速率,不能片面说是加快。
2、二氧化锰对过氧化氢(氯酸钾)的分解是有催化作用,但不是专做催化剂的。
3、催化剂不能增大或减少生成物质量。
学生实验探究:
二氧化锰
1、实验原理:在刚才的实验中,用二氧化锰做催化剂,过氧化氢分解加速,这一反应可以如下表示:过氧化氢 水+氧气
2、气体发生装置:
3、气体收集装置:
问题:根据氧气的物理性质,可用什么方法收集氧气?
归纳:氧气不易溶于水,故可用排水法;氧气密度比空气大,故可用向上排空气法。
4、检验与验满:
问题:根据氧气的化学性质,如何判断氧气已集满?如何检验氧气?
归纳:用带火星的木条靠近集气瓶,木条复燃,证明已满(气泡从瓶口溢出,证明已满);用带火星木条伸入试管中,发现木条复燃,说明是氧气。
5、老师组装仪器,演示实验,检验气体(排水法)并讲解注意事项。
学生活动:除了用过氧化氢分解的方法制取氧气外,实验室还可用哪些方法制取氧气呢?请同学阅读教材。
演示实验:
教师演示加热氯酸钾的方法制取氧气(用向上排空气法收集)。
按照实验步骤边操作边讲解。
学生:写出此反应的文字表达式及加热分解高锰酸钾制氧气的文字表达式:
二氧化锰
加 热
氯酸钾 氯化钾+氧气
加热
高锰酸钾 锰酸钾 + 二氧化锰 +氧气
学生讨论:
1、 分析上述三个制取氧气的反应,有何特点?它们与化合反应有何不同?
2、 用过氧化氢制取氧气与用高锰酸钾制取氧气哪一套装置更好,怎样来比较两套装置的优劣?
归纳总结:
1、分解反应概念 2、特点:一变多 (AB→A+B)
学生课堂练习:幻灯片
教师:工业上用氧气的特点是量大,工业上制取氧气也和我们实验室制取一样吗?
学生阅读教材资料:工业上如何大量制取氧气,并思考工业上制取氧气的原则、特点及方法。
师生归纳:
1、原则、特点:原料是否易得、价格是否便宜、成本是否低廉、能否大量生产及对环境的影响。
2、方法:分离液态空气法(物理方法)
课堂小结
通过本课的学习,收获是 。
在的问题是
作业布置
评议:
1、能面向全体学生,因材施教。
2、教学设计合理,重点突出,难点突破好。
3、教学过程层次清楚。
4、教学方法得当。
5、课堂调控好、师生配合默契。
6、学生参与度高,课堂气氛活跃。
7、将教师演示实验改成学生演示,教师指导,大大激发了学生的积极性。
8、建议在写文字表达式的时候,可写出化学式,便于降低以后学习的难度。
