实验四 色谱法测定固体催化剂的表面积
一、实验目的
1. 掌握用流动吸附色谱法测定催化剂比表面积的方法。
2. 通过实验了解BET多层吸附理论在测定比表面积方面的应用。
二、实验原理
催化剂的表面积是其重要的物性之一。表面积的大小直接影响催化剂的效能。因此在催化剂研究、制造和应用的过程中,测定催化剂的表面积是十分重要的。
固体催化剂表面积的测定方法较多。经典的BET法,由于设备复杂、安装麻烦,应用受到一定限制。气相色谱的发展,为催化剂表面积测定提供了一种快速方法。色谱法测定催化剂固体表面积,不需要复杂的真空系统,不接触水银,操作和数据处理较简单,因此在实验室和工厂中得到了广泛应用。
色谱法测固体比表面积是以氮为吸附质、以氢气或氦气作为载气,二者按一定的比例通入样品管,当装有待测样品的样品管浸入液氮时,混合气中的氮气被样品所吸附,而载气不被吸附,He-N2混气或H2-N2混气的比例发生变化。这时在记录仪上出现吸附峰。各种气体的导热系数不尽相同,氢和氦的导热系数比氮要大得多,具体各种气体的导热系数如下表

同样,在随后的每个样品解吸过程中,被吸附的N2又释放出来。氮、氦气体比例的变化导致热导池与匹配电阻所构成的惠斯登电桥中A、B二端电位失去平衡,计算机通过采样板将它记录下来得到一个近似于正态分布的电位-时间曲线,称为脱附峰。最后在混合气中注入已知体积的纯氮,得到一个校正峰。根据校正峰和脱附峰的峰面积,即可计算在该相对压力下样品的吸附量。改变氮气和载气的混合比,可以测出几个氮的相对压力下的吸附量,从而可据BET公式计算表面积。BET公式:
P/V(P0-P)=1/VmC+(C-1)/VmC*P/P0(1)
式中:P—氮气分压,Pa;
P0—吸附温度下液氮的饱和蒸气压,Pa;
Vm—待测样品表面形成单分子层所需要的N2体积,ml;
V—待测样品所吸附气体的总体积,ml;
C—与吸附有关的常数。
其中
V=标定气体体积×待测样品峰面积/标定气体峰面积
标定气体体积需经过温度和压力的校正转换成标准状况下的体积。以P/[V(P0-P)]对P/P0作图,可得一条直线,其斜率为(C-1)/(VmC),截距为1/(VmC),由此可得:
Vm=1/(斜率+截距) (2)
若知每个被吸附分子的截面积,可求出催化剂的表面积,即
Sg=(VmNAAm)/(22400W) (3)
式中Sg——催化剂的比表面积,m2 /g;
NA——阿弗加德罗常数;
Am——被吸附气体分子的横截面积,其值为16.2×10-20m2 ;
W——待测样品重量,g;
BET公式的使用范围P/P0=0.05~0.35,相对压力超过此范围可能发生毛细管凝聚现象
三、实验流程
本实验采用3H-2000Ⅱ型氮吸附比表面仪用色谱法测定催化剂的比表面,见图1。
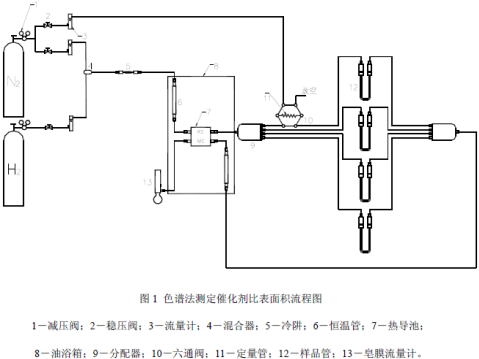
四、实验步骤
(1)样品管的制备 样品管应用重铬酸钾与浓硫酸配制的洗液浸泡后用蒸馏水冲洗干净烘干用。
(2)装样 将待测样品在110℃下烘干、恒重等预处理后,装入样品管(装样量以体积为标准,约为装样管体积的1/3至1/2以不影响流速为准),称量准确至0.1mg。
(3)安装样品管 将三个装有待测样品的样品管依次安装在从左至右的三个样品位上(假设同时测试3个待测样品),第四个样品为标准气体通道,安装一空管即可。(样品管的两个端口各套两个o形密封圈,上圈至端口约5mm,为防止漏气,样品管夹套应尽量拧紧)
(4)安装定量管 将选择好的定量管准确测量长度后安装在定量管位上,插到位即可,为自密封式接口。定量管体积可根据待测样品的比表面积大小选择合适的体积,定量管单位长度体积为4.5322ml/m。标定气体体积为定量管单位长度体积与六通阀死体积之和。
(5)打开载气减压阀 调节载气流量为100ml/min左右,等待10-15min左右使其流量稳定后用皂膜流量计准确测量,并在整个实验过程中保持载气流速不变,将六通阀置于“测量位”。
(6)打开N2减压阀 调节N2流量为10ml/min左右,用皂膜流量计准确测定混合气体总流量。(注:为使流量稳定,若载气为H2,则氢气减压阀减压表示数应在0.1MPa以上,N2减压阀表示数应在0.4 MPa以上)
(7)打开吸附仪电源开关,调节电流旋钮至最大,调节电压使电流为100mA,等待5-10min至调零显示稳定后,调节热导池电位粗调、细调旋钮,使热导池平衡,即调零输出信号为0。
(8)设定计算参数 打开数据处理应用程序,在应用程序中分别对[设置]菜单中的[显示设置]、[计算参数设置]、[试样设置]子菜单各参数进行设置。当以气体标样来标定时,只需要使[试样设置]中各参数不为零即可。(由于气体作标样时只利用该软件的积分功能,待测样品比表面积需要人工计算求得,故标准样品重量和标准比表面积及待测样品重量这几个参数不用设定)
(9)低温吸附 将两个盛满液氮的液氮杯放在从左至右的两个升降台上,调零后点击[吸附],接下来转动升降开关使两个液氮杯逐个上升,中间间隔5-10s(间隔时间视待测样品比表面积而定,待测样品比表面积越大,间隔时间相应要加长,其目的为防止样品管内气体瞬间冷缩和被吸附,将空气倒吸入热导池内)待调零显示基本稳定后,可认为吸附平衡,点击[完成],调零,准备脱附。
(10)升温脱附 用60℃左右温水升温脱附。先调零,点击[开始],降下第一个样品位的液氮,换上温水,得到第一个待测样品的脱附峰和峰面积,待调零显示归零后,同上,对第二、第三个待测样品进行脱附。待测样品脱附完毕后,将六通阀转至“标定位”,得到标定气体的峰和峰面积。(注意:如果对一个样品脱附结束后,调零显示没有完全回到零点,需要人为手动调零后,再继续下一个样品的脱附或标定)。记录各峰面积,完成一个分压点下的测定。
(11)进行下一个分压点下的测量。 若H2流量没有变化,则只用改变N2流量(每次较前一次增加约7-10ml,流量越大增加量应越大,使N2分压平均分布在0.05-0.30之间),用皂膜流量计准确测量混合气体总流量。按步骤8-11重复操作4-5次,完成一组样品的实验测定。
五、数据记录与处理
1.实验条件:
实验大气压101.325kPa,实验开始温度:29.9℃,实验结束温度:30.2,实验过程的平均温度为30.05。查得此温度下的氮气饱和蒸汽压为样品量、标样管体积、实验时大气压及室温下N2饱和蒸汽压为793.3mmHg,合793.3×101325/760=105764.63Pa。
表1 比表面积测试仪器性质:(4号设备)
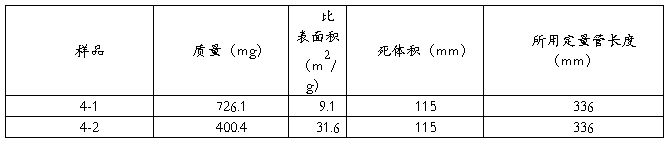
标定气体体积的校正为:4.5322*(0.115+0.336)*273.15/(273.15+30.05)=1.84mL
2、载气与混合气流量测定的原始与处理表
表2 气体流量测定计算表
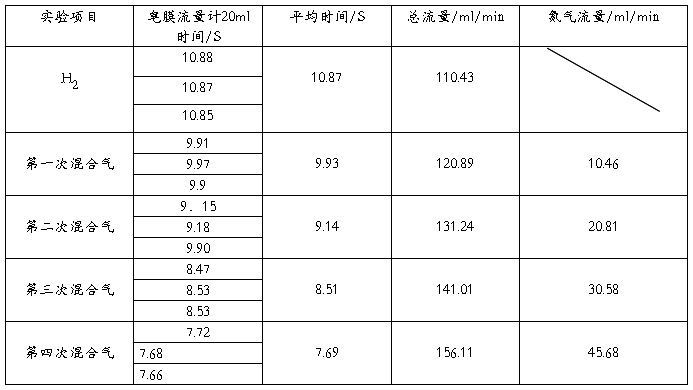
计算举例:以第一次混合气为例:平均时间9.91+9.97+9.9/3=9.93
混合气的总流量=20*3*60/(9.91+9.90+9.97)=120.89mL/min
N2的流量=120.89-110.43=10.46mL/min
3、气相色谱分析记录与结果
表3 气相色谱分析记录与结果
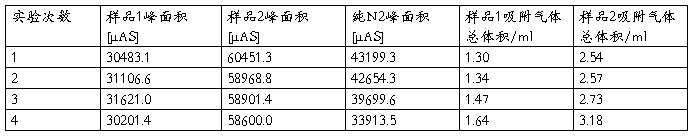
计算举例:以第一次样品1混合气为例,V=标定气体体积×待测样品峰面积/标定气体峰面积=1.84×30483.1/43199.3=1.30ml
数据处理与作图
表4 样品数据处理
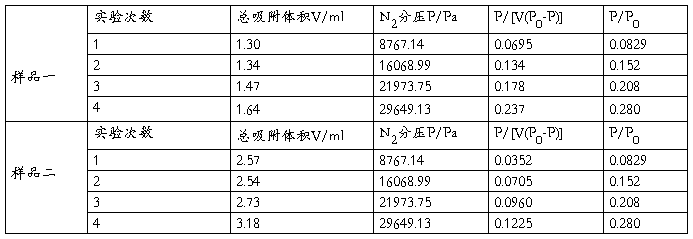
其中,N2分压P=氮气流量/总流量×标准大气压(以第一次实验为例)
=10.46/120.89*101325=8967.14
P/[V(P0-P)]=8767.14/[1.3*(105764.63-8767.14)]=0.0695
P/P0=8767.14/105764.63=0.0829
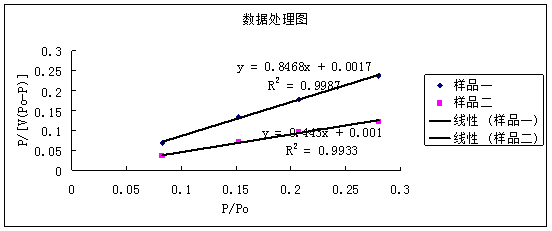
对样品一,得出回归方程为y=0.8468x+0.0017,由此可求出其截距为y=0.0017,斜率为0.8468.由实验原理分析可知,截距=0.0017=1/VmC,斜率为(C-1)/(VmC),两式联立可得Vm=1/(斜率+截距)=1/(0.8468+0.0017)=1.1786
故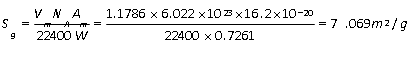
 相对误差为
相对误差为
(7.069-9.1/9.1)*100%=-22.3%
对样品二,得出回归方程为y=0.445x+0.001,由此可求出其截距为y=0.001,斜率为0.445.由实验原理分析可知,截距=0.001=1/VmC,斜率为(C-1)/(VmC),两式联立可得Vm=1/(斜率+截距)=1/(0.445+0.001)=2.24
故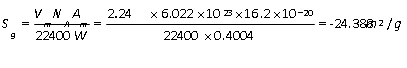
相对误差为(24.388-31.6/31.6)*100%=22.8%
实验结果误差分析
有实验计算得出的结果与理论值相比,相对误差较大,样品一达-22.3%,样品二达-22.8%,可能与实验仪器所带来的固定误差有关;同时可以保证,实验过程是严格按照规定的步骤实施的,计算与数据处理过程也经过了3次验算。现就可能导致如此大的误差的原因进行讨论:
实验仪器带来的固定误差。因为两次测量结果都是偏小的,可能与催化剂样品本身的消耗或磨损造成其自身有效比表面积的下降有关,抑或是通入气体的压力不稳定,造成载气和氮气的通入量是变化的,故导致实验结果产生偏差。(实验中也确实观察到了转子流量计示数发生变化)
实验数据准确性低带来的误差。若忽略其它误差,则可以归结于计算Vm值时偏小,即(斜率+截距)值偏大。
固定数据的准确性带来的误差。除上述原因之外,室温下氮气的饱和蒸汽压数据、被吸附气体分子的横截面积等都是值得怀疑的,而且无法排除被吸附气体分子发生重叠、架桥的可能。
也可能是载气及混合气体的流量在实验过程中不稳定,使得测定的氮气的流速产生误差。实验过程中,温度发生波动,测定的标定气体体积产生误差。测定方法本身存在着系统误差。
六、思考题
1. 实验中相对压力为什么要控制在0.05~0.35之间?
答:BET公式的使用范围P/P0=0.05~0.35,相对压力超过此范围可能发生毛细管凝聚现象。
2. 定量管体积是固定的,为什么每作一个实验点都要进行标定?
答:原因:虽然定量管的体积是固定的,但是在每个实验点实验时N2的流速是变化的,因此标定气体体积是变化的,计算得到的待测样品所吸附气体的总体积也是变化的,故需每做一个实验点都要进行标定。
3. 影响本实验误差的主要因素是什么?
答:影响本实验误差的主要因素:1载气及混合气体的流量在实验过程中不稳定,使得测定的氮气的流速产生误差。2实验过程中,温度发生波动,测定的标定气体体积产生误差。3测定方法本身存在着系统误差。4仪器自身存在着测量误差。
第二篇:色谱法测催化剂比表面积实验报告
化工专业实验报告
实验名称:色谱法测定固体催化剂的表面积
实验人员: 同组人:
实验地点:天大化工技术实验中心606室
实验时间: 2015年4月17号
年级 ;专业 ;组号;学号 指导教师:
实验成绩:
天津大学化工技术实验中心印制
一.实验目的
1. 掌握用流动吸附色谱法测定催化剂比表面积的方法。
2. 通过实验了解BET多层吸附理论在测定比表面积方面的应用。
二.实验原理
催化剂的表面积是其重要的物性之一。表面积的大小直接影响催化剂的效能。因此在催化剂研究、制造和应用的过程中,测定催化剂的表面积是十分重要的。 固体催化剂表面积的测定方法较多。经典的BET法,由于设备复杂、安装麻烦,应用受到一定限制。气相色谱的发展,为催化剂表面积测定提供了一种快速方法。色谱法测定催化剂固体表面积,不需要复杂的真空系统,不接触水银,操作和数据处理较简单,因此在实验室和工厂中得到了广泛应用。 色谱法测固体比表面积是以氮为吸附质、以氢气或氦气作为载气,二者按一定的比例通入样品管,当装有待测样品的样品管浸入液氮时,混合气中的氮气被样品所吸附,而载气不被吸附,He-N2混气或H2-N2混气的比例发生变化。这时在记录仪上出现吸附峰。各种气体的导热系数不尽相同,氢和氦的导热系数比氮要大得多,具体各种气体的导热系数如下表1。
表1 气体导热系数表

同样,在随后的每个样品解吸过程中,被吸附的N2又释放出来。氮、氦气体比例的变化导致热导池与匹配电阻所构成的惠斯登电桥中A、B二端电位失去平衡,计算机通过采样板将它记录下来得到一个近似于正态分布的电位-时间曲线,称为脱附峰。最后在混合气中注入已知体积的纯氮,得到一个校正峰。根据校正峰和脱附峰的峰面积,即可计算在该相对压力下样品的吸附量。改变氮气和载气的混合比,可以测出几个氮的相对压力下的吸附量,从而可据BET公式计算表面积。BET公式:
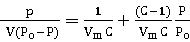 (1)
(1)
式中:P—氮气分压,Pa;
P0—吸附温度下液氮的饱和蒸气压,Pa;
Vm—待测样品表面形成单分子层所需要的N2体积,ml;
V—待测样品所吸附气体的总体积,ml; C-与吸附有关的常数
其中
V=标定气体体积×待测样品峰面积/标定气体峰面积
标定气体体积需经过温度和压力的校正转换成标准状况下的体积。以P/[V(P0-P)]对P/P0作图,可得一条直线,其斜率为(C-1)/(VmC),截距为1/(VmC),由此可得:
Vm=1/(斜率+截距) (2)
若知每个被吸附分子的截面积,可求出催化剂的表面积,即
Sg=(VmNAAm)/(22400W) (3)
式中Sg—催化剂的比表面积,m2/g;
NA—阿弗加德罗常数;
Am—被吸附气体分子的横截面积,其值为16.2×10-20m2;
W——待测样品重量,g;
BET公式的使用范围P/P0=0.05~0.35,相对压力超过此范围可能发生毛细管凝聚现象
三.实验流程
本实验采用3H-2000Ⅱ型氮吸附比表面仪用色谱法测定催化剂的比表面,见图1。
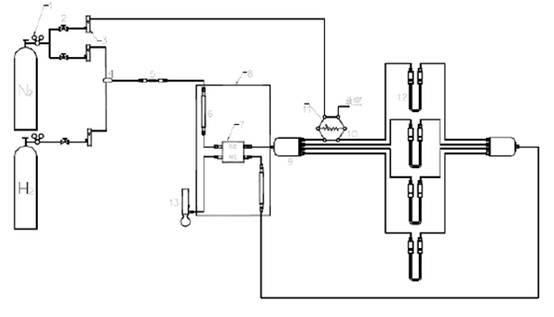
1—减压阀; 2—稳压阀; 3—流量计; 4.混合器; 5.冷阱; 6—恒温管; 7—热导池
8—油浴箱; 9—分配器; 10—六通阀; 11—定量管; 12—样品管; 13—皂膜流量计
四.实验步骤
(1)样品管的制备 样品管应用重铬酸钾与浓硫酸配制的洗液浸泡后用蒸馏水冲洗干净烘干用。
(2)装样 将待测样品在110℃下烘干、恒重等预处理后,装入样品管(装样量以体积为标准,约为装样管体积的1/3至1/2以不影响流速为准),称量准确至0.1mg。
(3)安装样品管 将三个装有待测样品的样品管依次安装在从左至右的三个样品位上(假设同时测试3个待测样品),第四个样品为标准气体通道,安装一空管即可。(样品管的两个端口各套两个o形密封圈,上圈至端口约5mm,为防止漏气,样品管夹套应尽量拧紧)
(4)安装定量管 将选择好的定量管准确测量长度后安装在定量管位上,插到位即可,为自密封式接口。定量管体积可根据待测样品的比表面积大小选择合适的体积,定量管单位长度体积为4.5322ml/m。标定气体体积为定量管体积与六通阀死体积之和。即4.5322乘以定量管长度与死体积长度之和。
(5)打开载气减压阀 调节载气流量为100ml/min左右,等待10-15min左右使其流量稳定后用皂膜流量计准确测量,并在整个实验过程中保持载气流速不变,将六通阀置于“测量位”
(6)打开N2减压阀 调节N2流量为10ml/min左右,用皂膜流量计准确测定混合气体总流量。(注:为使流量稳定,若载气为H2,则氢气减压阀减压表示数应在0.1MPa以上,N2减压阀表示数应在0.4 MPa以上)
(7)打开吸附仪电源开关,调节电流旋钮至最大,调节电压使电流为100mA,等待5-10min至调零显示稳定后,调节热导池电位粗调、细调旋钮,使热导池平衡,即调零输出信号为0。
(8) 设定计算参数 打开数据处理应用程序,在应用程序中分别对[设置]菜单中的[显示设置]、[计算参数设置]、[试样设置]子菜单各参数进行设置。当以气体标样来标定时,只需要使[试样设置]中各参数不为零即可。(由于气体作标样时只利用该软件的积分功能,待测样品比表面积需要人工计算求得,故标准样品重量和标准比表面积及待测样品重量这几个参数不用设定)
(9)低温吸附 将一个盛液氮的液氮杯(大约2/3满)放在从左至右的第二个升降台上,调零后点击[吸附],接下来转动升降开关使液氮杯上升,中间间隔5-10s(间隔时间视待测样品比表面积而定,待测样品比表面积越大,间隔时间相应要加长,其目的为防止样品管内气体瞬间冷缩和被吸附,将空气倒吸入热导池内)待调零显示基本稳定后,可认为吸附平衡,点击[完成],调零,准备脱附。
(10)升温脱附 先调零,点击[开始],降下液氮,直接利用环境温度进行脱附,降下液氮杯后,将液氮杯拿离并用盖子盖好。得到待测样品的脱附峰和峰面积,待调零显示归零后,同上。待测样品脱附完毕后,将六通阀转至“标定位”,得到标定气体的峰和峰面积。记录各峰面积,完成一个分压点下的测定。
(11)进行下一个分压点下的测量。 若H2流量没有变化,则只用改变N2流量(每次较前一次增加约10ml,使N2分压平均分布在0.05-0.30之间),用皂膜流量计准确测量混合气体总流量。继续按步骤8-11操作,完成样品的实验测定。
五,原始数据记录与处理
表2 比表面积测试仪器性质表(4号设备)

表3载气与混合气流量测定表
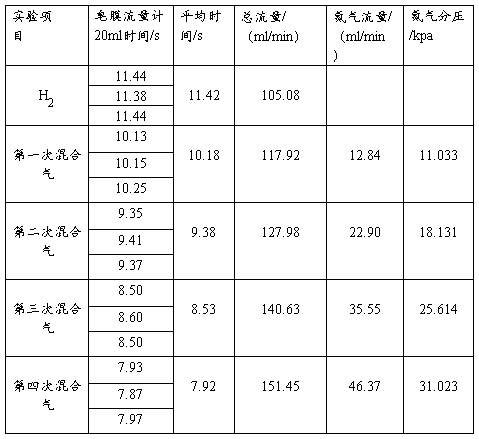
表4 气相色谱分析记录与结果表
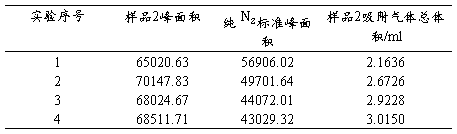
备注:1. 气体在皂膜流量计的计时体积为20ml
2. 实验开始温度为21.3℃,结束温度为21.8℃,实验过程平均温度为21.7℃
3. 吸附温度下液氮的饱和蒸汽压为793.3mmHg,P0=793.3×101.325/760=105.765kPa
4. 实验设备为第4套
六.计算举例
1. 氮气流量及分压
以氢气和第三次混合气中氮气流量及分压为例详细计算
皂膜流量计平均时间 tm=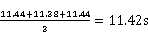
氢气流量: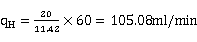
第三次混合气总流量: 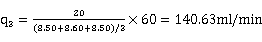
第三次进样氮气流量: 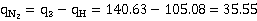 ml/min
ml/min
氮气的分压:P=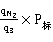 =
= 25.614kpa
25.614kpa
2. 样品2吸附N2体积
以样品2第三次混合气进样为例,计算N2的吸附总体积
标定气体体积的计算:
标定气体体积=定量管体积+六通阀死体积 (标准温度下),需对其进行温度和压力校正
定量管长度为336mm,死体积长度为115mm,平均温度为21.7℃,
标定体积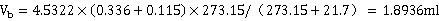
N2总体积V=标定气体体积×待测样品峰面积/标定气体峰面积
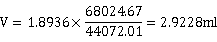
3. 待测样品表面形成单分子层所需要的N2体积
以P/[V(P0-P)对P/P0作图,可得一条直线,其斜率为(C-1)/(VmC),截距为1/(VmC)其中P0=793.3×101.325/760=105.765kPa
Vm=1/(斜率+截距)
表5 样品拟合数据表

使用excel软件做样品的线性回归得
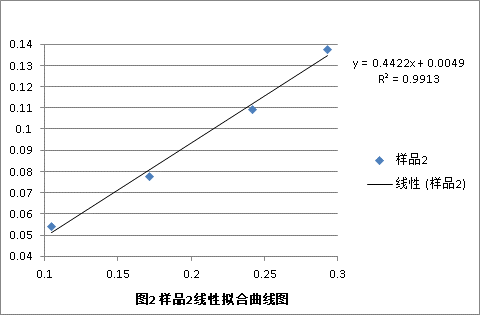
由Vm=1/(斜率+截距)
Vm=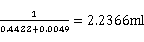
4. 计算催化剂的比表面积
Sg=(VmNAAm)/(22400W)
=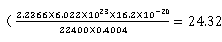 m2/g
m2/g
参考值:Sg=31.6m2/g
相对误差为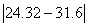 /31.6
/31.6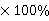 =23.04%
=23.04%
七.实验结果与误差分析
实验结果显示样品的比表面积比参考值低,而且相对误差较大,可能是以下几个原因造成
1. 由于内扩散影响,氮气没有完全进入催化剂或者中心处氮气浓度较低,吸附不完全;
2. 实验数据少,线性拟合结果误差大;
3. 催化剂样品本身的消耗或磨损造成其自身有效比表面积的下降;
4. 由于吸附氮气分子间的相互作用力,导致氮气未能在样品样品表面完全覆盖;
5. 吸附时间较短,脱吸不是十分完全,使得脱吸峰比实际可以达到的要小。
6. 通入气体的压力不稳定,造成载气和氮气的通入量是变化的,故导致实验结果产生偏差;
八.思考题
1.单分子层吸附和多分子层吸附的主要区别是什么?试叙述要点
单分子层吸附认为固体表面是均匀的,只能发生单分子层吸附,被吸附在固体表面上的分子相互之间无作用力,吸附平衡是动态平衡,各处的吸附能力相同,被吸附分子横向之间没有相互作用的假设。而多分子层吸附认为已被吸附的分子与碰撞在它们上面的气体分子之间仍可发生吸附,固体表面经常是不均匀的,各点的吸附能力不尽相同。
2. 实验中相对压力为什么要控制在0.05~0.35之间?
BET公式的使用范围P/P0=0.05~0.35,相对压力超过此范围可能发生毛细管凝聚现象
3. 样品管体积是固定的,为什么每作一个实验点都要进行标定?
每次N2进样流速都会改变,因而每次系统的稳态点都会发生变化。原先标定的峰面积由于设备稳态发生变化,都会有偏移。每作一个实验点都进行标定,可以保证在相同的设备稳态下,系统误差得到消除。因而每个实验点都要进行标定。
4. 在催化剂制备中,哪些因素会影响其比表面积?
催化剂颗粒大小,催化剂孔径大小,反应温度,压力等都会影响其比表面积
5.催化剂的比表面积,对催化剂的性能有哪些影响?试述大比表面积分子筛的优缺点。
催化剂比表面大,与反应物分子接触面积越大,原则上催化剂活性越高,但比表面大催化剂抗粉碎能力就越差。比表面积大的分子筛通过的分子应该是更小的。
大比表面积分子筛的优点有:有助于反应物的吸附,反应效率和速率均会提高;缺点:比表面积越大催化剂的粒径越小,反应物通过催化剂的压降越高,催化剂更易结块影响活性
