2016高三生物高考一轮复习建议计划
一、教学要求
以山东省生物学科《考试说明》和生物《课程标准》为主要依据,认真研究近几年课改省市高考试题特别是我省试题及全国新课标卷,制定科学细致的高三教学计划,充分挖掘探究式教学方式及“概念图”教学策略在高三生物复习中的应用空间,注重策略整合,调动学生的积极性和主动性,有效促进和指导学生的自主学习,以夯实基础为重点,以培养能力为核心,立足学科内综合,强化生物学概念的理解与应用,切实提高学生的理解能力、实验与探究能力、获取信息能力与综合运用能力,努力提高教育教学质量。
二、教学安排
按学期分两阶段组织教学,实行三轮次复习。
第一阶段:20xx年4月~20xx年2月,主要任务必修及选修模块的一轮复习。要求以《考试说明》呈现的知识内容为主线,划分复习单元,把握内在联系,梳理学习内容,形成知识体系,适当参考中图版教材,突出落实双基,初步培养能力。
必修分为十个单元:
第一单元:细胞的分子组成与结构
第1讲、组成细胞的元素和无机物;第2讲、组成细胞的有机物;第3讲、细胞的基本结构
第二单元:细胞的代谢
第1讲、生物膜系统及物质运输;第2讲、酶和ATP;第3讲、
光合作用;第4讲、细胞呼吸
第三单元:细胞的生命历程
第1讲、细胞增殖;第2讲、细胞的分化、癌变、衰老和凋亡 第四单元:遗传的细胞基础与分子基础
第1讲:减数分裂与受精;第2讲、人类对遗传物质的探索过程;第3讲、DNA分子的结构和复制;第4讲、基因的表达及其对性状的控制
第五单元:遗传的基本规律
第1讲、基因的分离规律;第2讲、基因的自由组合规律;第3讲、伴性遗传
第六单元:生物的变异
第1讲、基因突变和基因重组;第2讲、染色体变异;第3讲、人类遗传病(包括类型、监测、预防)及人类基因组计划
第七单元:生物的进化
第1讲、现代生物进化理论;第2讲、进化与生物多样性 第八单元:植物的激素调节
第1讲、植物生长素的发现和作用;第2讲、其他植物激素及其应用
第九单元:动物内环境稳态及其调节
第1讲、内环境及其稳态;第2讲、神经调节;第3讲、动物的激素调节;第4讲、血糖调节、水盐平衡的调节(包括神经调节和体液调节的关系);第5讲、免疫调节(包括艾滋病的流行和预防)
第十单元:生态系统与环境保护
第1讲、种群、群落;第2讲、生态系统的结构功能;第3讲、生态系统的稳定性及环境保护
选修分为四个单元:
第一单元:基因工程及蛋白质工程 第二单元:克隆技术
第三单元:胚胎工程
第四单元:生物技术的安全性和伦理问题
教学计划:
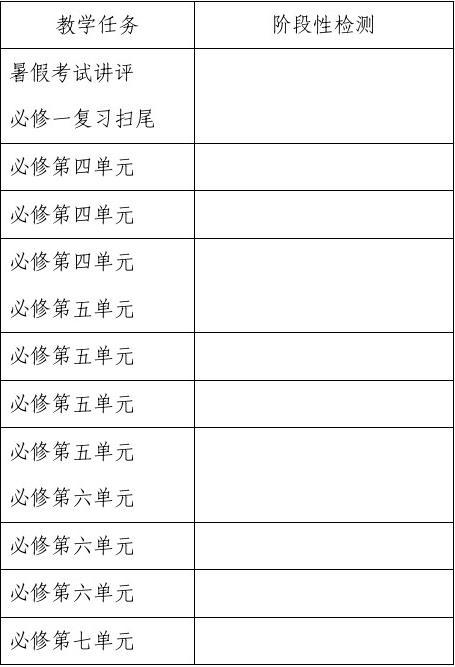
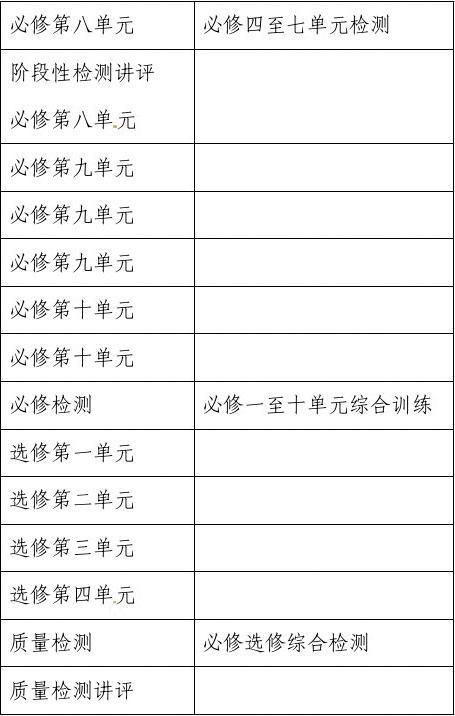
第二阶段:20xx年3月初~5月底。要求以学科内综合为重点,以专题复习为线索,以训练点评为主要手段,继续深入挖掘优化各种课程资源,特别突出内在联系,注重学科主干内容与核心知识,要求“点、线、面”有机结合,“细、实、活”相得益彰,形成完整的知识网络,并进行模拟训练和重点讲评,适当穿插理科综合,进一步提高学生分析问题和解决问题的能力,帮助学生了解理科综合的考试形式和对各种能力的要求,提高学生的应考能力。专题划分:
专题一:实验专题
专题二:细胞及其生命历程
专题三:细胞代谢
专题四:生物的遗传
专题五:生物的变异和进化
专题六:个体的稳态调节
专题七:群体的稳态调节
专题八:选修模块
三、教学措施
1、加强研究,科学把握高考方向。
一要研究《考试大纲》和《考试说明》,解决考什么的问题。要细致深入地研究《大纲》、《说明》,注重研究《说明》中能力要求所使用的行为动词及考查目标,研究考试知识内容要点及其要求层次,研究明确各级内容要求及能力要求的具体内涵,研究样题的来源与考查角度,增强备考复习的针对性与有效性。
二要研究高考试题,解决怎么考的问题。要研究近几年山东卷和全国新课标卷的采点规律,明确每年必考点、常考点和未考点。要研究特定知识点的考查角度,以预测还可能的考查角度,增强复习教学的细致性与周密性。
三要研究理综命题和应试技巧,解决怎么应对的问题。理综试题的组题质量是影响模拟训练质量的关键性因素之一,所以,要适当控制理综试题的综合性,控制好每次考查的覆盖面。强化学生的得分意识。教导学生在综合考试时,要果断取舍,树立总分至上的观念,不能在某些题目或某个学科上花费过多时间,避免出现难题
不会答,容易题没有时间答的局面,增强备考有效性及学生的考试能力。
2、改进教学方法,有效促进学生的自主学习。
生物学科高考命题在关注学生的情感态度与价值观目标的基础上,注重学科内的知识综合考查及相关能力考查。正确理解理解概念和基础理念是培养学生能力不可缺的基础,因此要倡导探究式教学方式及“概念图”教学策略在高三生物复习中的有效应用,使复习课以问题为中心、以运用为方向、以能力为目标,侧重对知识的归纳和梳理,尤其注重学科内知识的串联与综合,强化学生对概念的正确理解和真实应用。
讲评课要注重传授解题技巧,分析考查的知识点明确答题规范,培养学生良好的审题、解答、整理答案的习惯。教师要重视反馈与总结,及时矫正教与学中的漏洞。要删除无效教学环节,坚决杜绝“水过地皮湿”的现象,给学生较多主动反思和内化的时间,指导帮助学生确定复习目标、制定复习计划、做好具体的复习准备,在复习过程中能对复习的进展和复习方法做出自我监控、自我反馈和自我调节,在学习活动后对复习结果进行自我检查、自我总结、自我评价和自我补救,让学生真正成为复习备考的主人,力求复习高质高效。
3、提高命题质量,保证训练的科学性、针对性和有效性。 首先,制定命题双向细目表,明确分工也确定每次训练的考查点,增强针对性和知识覆盖面。然后,命题人(至少2人)研究细目表,针对采点搜集大量有用的素材进行组题,形成“草卷”。最后,另外两名老师做草卷,觉得挖掘不够或表达有问题或是无意义的题目进行修
改,组长定稿形成正式训练卷。 在选择习题时,要注意:一是训练要有明确的目标,二是选择的题目要有针对性和层次性,三是训练要限时和定量、适度和适量,四是训练要加强过程监督,了解学生做题情况,提高训练效率。要挖掘每道题目的潜在价值,把每个题目做深做细做透,力求深入一层,递进一步。只要教师做的工作力度大一些,挖掘深刻一些,学生就会有更大的收益。
4、优化学案与教辅,保证学生有目的有方向的自主学习。 学案作为一种被优化的学习指导卡,在关注学生的差异、引领学生学习方向、调动学生自主性、指导学生理解和应用教材内容等多方面具有较大的作用,生物复习学案的设计至少应包括“考试说明要求”、“基础知识回顾”、“重点难点突破”、“自我达标训练”四个栏目,其中“基础知识回顾”栏目一定要全面细致,尽量让学生书写,引导学生进行“地毯式”知识回顾;“重点难点突破”栏目要改变直接告诉学生的方式,而是代之以问题,引发学生思考,逐渐引导学生领悟熟练思考和表达的方法。
教辅作为一种学习材料和学科资源,在学生的自主性学习中也起到较大的作用。对于主体材料的使用要有自己的主见,决不能让资料掩盖了自己的复习思路。在学生使用前教师先进行精读精做精选,选出必做题和选做题以及删除题目,保证必做题全批全改,选做题学生自主完成,使学生有更多的选择空间,保障了作业的层次性,有利用因材施教促进学生的主动发展。
5、强化集体备课,正确处理集体备课与个人备课的关系,实现
群体优势与个人优势相结合。
集体备课是提高备课质量的重要备课形式。它可集思广益,将个人才智转化为集体优势,共同提高教学质量。集体备课应该建立在个人备课的基础上,集体备课完成后仍需再反思研究,针对自己班级的情况进行选择性吸收,形成有个性的教案。要把复习工作上升到科研水平,不要只停留在几节课或一段时间的效果上,要进行深层次的研究,总结出一套系统而有效的模式,使其发挥长效。要树立“实实在在共事,真心真意教研”的思想,不能把集体备课停留在口头上,要真正落实到行动中,充分发挥每个教师的主观能动性,充分调动全组成员的积极性,做到相互交流,集思广益,取长补短,形成合力。
第二篇:20xx年高考第一轮复习
学案1:物质的量、气体摩尔体积、物质的量浓度
【知识梳理】
一、物质的量:
1. 物质的量
(1)概念:
(2)单位:
(3)1mol的标准:
【注意】①摩尔适用于,不适用于宏观物质;如不能说“1mol大米”等 常见的微观粒子有原子、分子、离子、质子、中子、电子等或它们的特定组合 ②使用摩尔作单位时,应用 化学式指明粒子的种类 ;
如“1molH2O中含有2mol氢和1mol氧”这种说法是 错误的
2. 阿伏加德罗常数
(112所含的碳原子数, -123-1
【判断】1mol任何物质中都含阿伏伽德罗常数个分子( 错误 )
【说明】常见物质的构成微粒
由分子构成的物质: 气体、水、酸、白磷等
由离子构成的物质: 强碱、大多数盐、活泼金属氧化物等 由原子构成的物质: 晶体硅、金刚石、二氧化硅、碳化硅等
(2)微粒个数N 与物质的量n3. 摩尔质量:
(1)概念: (2 (3)摩尔质量、相对分子(或原子)质量和1mol物质所具有的质量之间的关系:
数值相等、单位不同
例:M(Na) , M(Na+)= 23g/mol ,
M(-CH3)= 15g/mol , M(D2O)
二、气体摩尔体积: 1. 影响物质体积大小的因素
决定物质体积大小的因素: 粒子数、粒子间距离、粒子大小
决定固体、液体体积大小的主要因素: 粒子数、粒子大小
决定气体体积大小的主要因素: 粒子数、粒子间距离
2. 气体摩尔体积:
(1)概念:在一定的 温度 和 压强 下, 单位物质的量 的 气体 所占的体积。 (2)公式: Vm=V/n ,单位: L/mol 或 m3/mol 。
(3)Vm=V/n的适用范围: 单一气体或混合气体 12
第1页
(4)Vm=22.4L/mol的使用条件:标准状况(0℃,101kpa)和气体
【注意】常考的标况下不是气态的物质: 水、SO3、C4以上的烃、CH2Cl2、CHCl3、CCl4、 大多数含氧衍生物等
(5)气体摩尔体积与1mol气体所占的体积关系: 数值相等、单位不同
【思考】非标况下,1mol任何气体的体积一定不等于22.4L ? 错误
(5)影响气体摩尔体积Vm大小的因素: 温度和压强 ,如常温常压下,Vm=24.5mol/L
三、阿伏加德罗定律及推论:
1. 概念: 同温同压下,相同体积的气体含有相同的粒子数(即分子数)
2. 推论:⑴同T、P下,气体体积之比等于 物质的量之比
⑵同T、P下,气体密度之比等于 摩尔质量之比
⑶同T、V下,气体压强之比等于 物质的量之比
⑷同T、P下,同体积任何气体的质量之比等于 摩尔质量之比
【例】在两个密闭容器中,分别充有质量相同的甲、乙两种气体,若两容器的温度
和压强均相同,且甲的密度大于乙的密度,则下列说法正确的是( B )
A.甲的分子数比乙的分子数多 B.甲的物质的量比乙的物质的量小
C.甲的摩尔体积比乙的摩尔体积小 D.甲的相对分子质量比乙的相对分子质量
四、物质的量浓度
1、定义: 单位体积溶液中所含溶质B的物质的量
2 mol/L
3 ②V指的是 溶液的体积而非水的体积
③氨水的溶质按NH3计算,1L 1mol/L氨水中: n(NH3)+n(NH4+)+n(NH3·H2O)=1mol
4、 w与c五、公式小结及适用范围
1、n=N/NA=m/M=V(气)/22.4L·mol-1=cV(aq)
2、M=m/n=(一个原子的质量)×NA=22.4L·mol-1
3、c=n/V(aq)=1000ρw/M
【高考排雷】有关阿伏加德罗常数NA的应用,注意事项
(单选)1、设NA表示阿伏加德罗常数,下列说法正确的是( )
A、标准状况下,2.24 L水中含有的分子数为0.1NA
B、分子数为NA的CO、C2H4混合气体体积约为22.4L,质量为28g
C、常温常压下,乙烯和环丙烷(C3H6 )组成的28g混合气体中含有3NA 个氢原子
D、常温下,32g含有少量臭氧的氧气中,共含有2NA个氧原子
E、0.1 mol·L的硫酸铜溶液中含铜离子数为0.1NA
F、含NA个Na+ 的 Na2O溶解于1L水中, Na+的物质的量浓度为1 mol/L
【总结】①、注意Vm=22.4L/mol的使用条件: 标况,气体
第2页 -1
②、由c求N时应注意:是否给了体积;若给了体积,是不是“溶液的体积” (单选)2、设NA表示阿伏加德罗常数,下列说法正确的是( )
A、2.8g乙烯和2.8g聚乙烯中含碳原子数均为0.2NA
B、1mol Na2O2 固体中含离子总数为4NA
C、13.6g熔融KHSO4中含有0.2NA 个阳离子
D、标准状况下,11.2L氦气中约含有NA 个氦原子
E、2.9g 2CaSO4·H2O含有的结晶水分子数为0.02NA
【总结】③、注意物质的组成
a b、NaHSO4的电离:NaHSO4(熔融)= Na++HSO4- NaHSO4(水溶液)=Na++H++SO42- c、Na2O2: 含2个Na和1个O2 ·H2O, CaSO4·2H2O......
(双选)3、设NA表示阿伏加德罗常数,下列说法正确的是( )
A、1L 1mol/L FeCl3溶液中含有NA 个Fe3+
B、1L 1mol/L NaHCO3溶液中含有NA 个HCO3-
C、1molNaHCO3晶体中含有NA 个HCO3
D、1.0L1.0mol·L-1CH3COOH溶液中,CH3COOH分子数为NA
E、100mL0.1mol·L-1醋酸溶液含有的分子总数一定小于0.01NA
F、常温下,100mL 1mol·LNa2CO3溶液中阴离子总数大于0.1NA
G、常温下,1 L1mol/L 的NH4NO3溶液中氮原子数为0.2 NA
【总结】④、注意 弱电解质的不完全电离和盐中弱离子的水解
(双选)4、设NA表示阿伏加德罗常数,下列说法正确的是( )
A、足量C12与5.6g Fe完全反应时,转移的电子数为0.2NA
B、0.1molMg在空气中完全燃烧生成MgO和Mg3N2,转移的电子数为0.2NA
C、常温常压下,活泼金属从盐酸中置换出1 mol H2,失去的电子数为2NA
D、1 mol Cl2参加反应转移电子数一定为2 NA
E、在反应KClO3+6HCl=KCl+3Cl2+3H2O中,每生成3mol Cl2转移的电子数为6 NA
【总结】⑤、注意复杂方程式中“转移电子数”的计算
如:Cl2 + H2O / NaOH:
Na2O2 + H2O / CO2: KClO3+HCl(浓):
NO2+H2O: Fe+Cl2/S: Cu+Cl2/S:
第3页 -1-+2-
用惰性电极电解AgNO3溶液: (单选)5、设NA表示阿伏加德罗常数,下列说法正确的是( )
A.标准状况下,22.4 L己烷中共价键数目为19NA
B、12.4g白磷晶体中含有的P—P键数是0.1NA
C、2mol SO2和1mol O2混合在V2O5存在的条件下,密闭容器中加热反应后,容器 内物质的分子数大于2NA
D、将NO2和N2O4分子共NA个降温至标准状况下,其体积为22.4 L
【总结】⑥、注意共价键键数的求法
若为分子晶体——数 如:NH3—3,CO2—4,P4—6等 若为原子晶体——算
如:晶体硅——2个Si—Si,金刚石—2个C—C,晶体SiO2—4个Si—O ⑦、注意常见的可逆反应及可逆反应的特点
合成氨反应,SO2和O2生成SO3,NO2和N2O4之间的转化,Cl2和H2O的反应
(单选) 6、下列叙述正确的是 ( )
A、在同温同压下,相同体积的任何气体所含的原子数相同
B、相同条件下,N2和O2的混合气体与等体积的N2所含原子数相等
C、等物质的量的NH4+ 和OH-所含质子数相等且电子数也相等
D、1mol 乙基中含有的电子数为18NA
【总结】⑧、注意特殊物质的摩尔质量、中子数、质子数和电子数: 电子数的求法:若不带电荷 电子总数=质子总数
若带电荷 aAn+:电子数=a-n; bBm-:电子数=b+m
【注意】求核外电子数与电子式无关,电子式只代表最外层电子数
(单选)7、下列叙述正确的是
A、常温下,18g 重水所含中子数为10NA
B、标准状况下,22.4L辛烷完全燃烧,生成的二氧化碳的分子数肯定大于8NA
C、电解精炼铜时,若阴极得到电子数为2NA个,则阳极质量减少64g
D、1molFeCl3完全水解转化为氢氧化铁胶体后能生成NA个胶粒 E、1mol甲烷中的氢原子被完全取代,需要Cl2分子数为2NA
【总结】⑨、注意分散系的变化导致微粒数目的变化
如FeCl3溶液转化为Fe(OH)3胶体,因为胶体微粒是分子的集合体,所以胶 原溶液中Fe3+
第4页
