醋酸电离度和电离常数的测定
——pH计的使用
[实验目的]
测定醋酸的电离度和电离常数。进一步掌握滴定原理,滴定操作及正确判断滴定终点。学习使用pH计。
醋酸(CH3COOH或HAc)是弱电解质,在水溶液中中存在以下电离平衡:
HAc?
?H+??Ac-?
?其平衡方程式为K????
i
?HAc?
+
H+Ac
+-
-
+
-
c为HAc的起始浓度,[H]、[Ac]、[HAc]分别为H、Ac、HAc的平衡浓度,α为电离度,Ki为电离平衡常数。
在纯的HAc溶液中,[H+]=[Ac-]=cα,[HAc]=c (1-α)。
???
则???H??100%
c
2
?H???Ac??????Ki??
HAcc???
?H??
???
c
2
?H??
??
?H????
当α<5%时,c-[H+]≈c,故K
i
根据以上关系,通过测定已知浓度的HAc溶液的pH,就知道其[H+],从而可以计算该HAc溶液的电离度和平衡常数。
[思考题]
1.若所用的醋酸浓度极稀,醋酸的电离度>5%时,是否还能用K
常数?为什么?
2.实验中[HAc]和[Ac-]浓度是怎样测定的?
3.同温度下不同浓度的HAc的溶液的电离度是否相同?电离平衡常数是否相同? [实验用品]
仪器:碱式滴定管、吸量管(10mL)、移液管(25mL)、锥形瓶(50mL)、烧杯(50mL)、pH计。 液体药品:HAc (0.20mol·L)、NaOH (0.20mol·L)标准溶液、酚酞指示剂 [基本操作]
1.滴定管的使用,参见第四章二。
2.移液管、吸量管的使用,参见第四章二。
3.容量瓶的使用,参见第四章二。 4.pH计的使用,参见第七章一。 [实验内容]
一、醋酸溶液浓度的测定
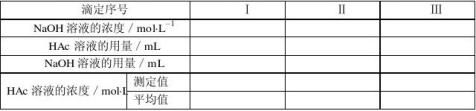
-1
-1
i
?H?????
c
…… …… 余下全文

 × 100%
× 100%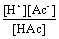 =
= 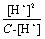


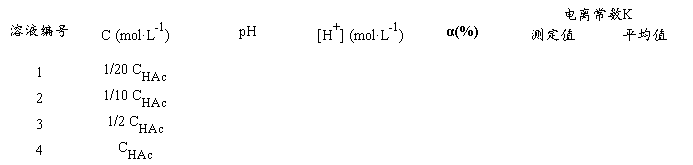
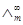 (S·m2·mol-1)
(S·m2·mol-1) H+ + Ac-
H+ + Ac-  =
= 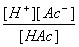 =
=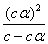 =
=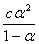 ,当α<5%时,1-α ≈1
,当α<5%时,1-α ≈1 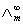 ,可以用离子的极限摩尔电导率相加而得。而一定浓度下电解质的摩尔电导率∧m与无限稀释的溶液的摩尔电导率
,可以用离子的极限摩尔电导率相加而得。而一定浓度下电解质的摩尔电导率∧m与无限稀释的溶液的摩尔电导率 (1)
(1)

 标准NaOH溶液
标准NaOH溶液
 待测25.00mLHAc溶液
待测25.00mLHAc溶液