专题二 化学用语(课前热身)
1.下列化学用语或模型表示正确的是( )
A.Cl-离子的结构示意图: B.CCl4分子的球棍模型:
B.CCl4分子的球棍模型:
C.乙烯的结构简式 CH2CH2 D.H2O2的结构式:H—O—O—H
2(2010上海卷改编)2.下列有关物质结构的表述正确的是
A.次氯酸的电子式 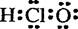 B.二氧化硅的分子式 SiO2
B.二氧化硅的分子式 SiO2
 C.氮元素和镁元素形成的相对分子质量为100的物质的化学式Mg3N2
C.氮元素和镁元素形成的相对分子质量为100的物质的化学式Mg3N2
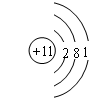
D.钠离子的结构示意图
3、下列各项表达中正确的是( )
A.乙烯的结构简式为CH2CH2
B.84g碳酸镁和碳酸氢钠的混合物与足量盐酸反应生成CO2的体积在标准状况下为22.4L
C.常温常压下28g氮气所含电子数约为6.02×1024
D.Cl—的结构示意图为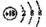
4(2010山东卷)9.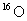 和
和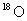 是氧元素的两种核素,
是氧元素的两种核素,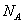 表示阿伏伽德罗常数,下列说法正确的是
表示阿伏伽德罗常数,下列说法正确的是
A.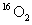 与
与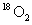 互为同分异构体
互为同分异构体
B. 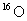 与
与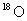 核外电子排布方式不同
核外电子排布方式不同
C.通过化学变化可以实现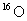 与
与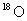 间的相互转化
间的相互转化
D.标准状况下,1.12L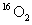 和1.12L
和1.12L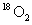 均含有0.1
均含有0.1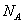 个氧原子
个氧原子
【考纲要求】
(1)熟记并正确书写常见元素的名称、符号、离子符号。
(2)熟悉常见元素的化合价。能根据化合价正确书写化学式(分子式),或根据化学式判断化合价。
…… …… 余下全文

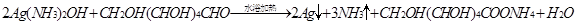 ;
; 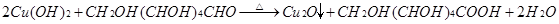 。
。 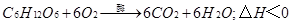 ;
; 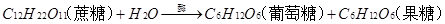
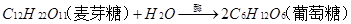
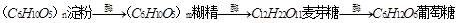 ,也可在酸的催化下逐步水解,其方程式
,也可在酸的催化下逐步水解,其方程式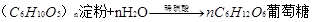 。 淀粉的特性:I2能使淀粉溶液变成蓝色。这是实验室检验淀粉或I2存在的重要原理。
。 淀粉的特性:I2能使淀粉溶液变成蓝色。这是实验室检验淀粉或I2存在的重要原理。 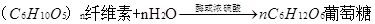 。纤维素不能作为人类的营养食物,但在人体内不可或缺,如:能刺激肠道蠕动和分泌消化液,有助于失误和废物的排泄……。
。纤维素不能作为人类的营养食物,但在人体内不可或缺,如:能刺激肠道蠕动和分泌消化液,有助于失误和废物的排泄……。 