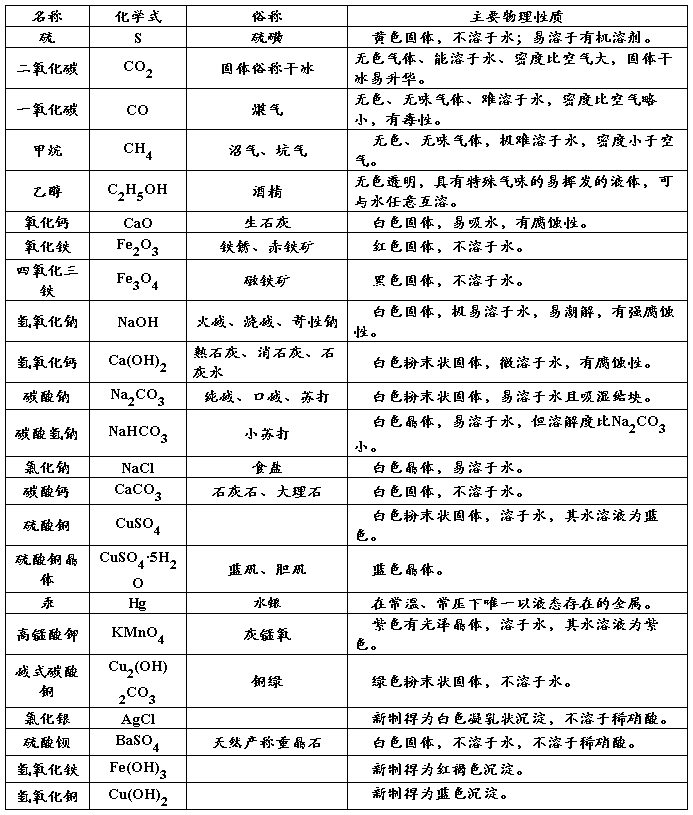
初三化学方程式总结
与氧有关的化学方程式:
(1)2Mg+O2点燃====2MgO 现象:
(2)S+O2 点燃====SO2 现象:
(3)C+O2(充足)点燃====CO2 现象:
(4)2C+O2(不充足)点燃====2CO
(5)4P+5O2点燃====2P2O5 现象:
(6)3Fe+2O2点燃====Fe3O4 现象:
(7)2H2+O2点燃====2H2O 现象:
(8)2HgO△====2Hg+O2↑ 现象:(9)实验室制取氧气的三种方法:
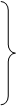 2H2O2MnO2====2H2O+O2↑ (“固+液”不加热型------制氧气)
2H2O2MnO2====2H2O+O2↑ (“固+液”不加热型------制氧气)
2KClO3MnO2====2KCl+3O2↑ (“固+固”加热型------制氧气) 实验室制氧气的三种方法
2KMnO4△====K2MnO4+MnO2+O2↑ (“固+固”加热型------制氧气)
…… …… 余下全文

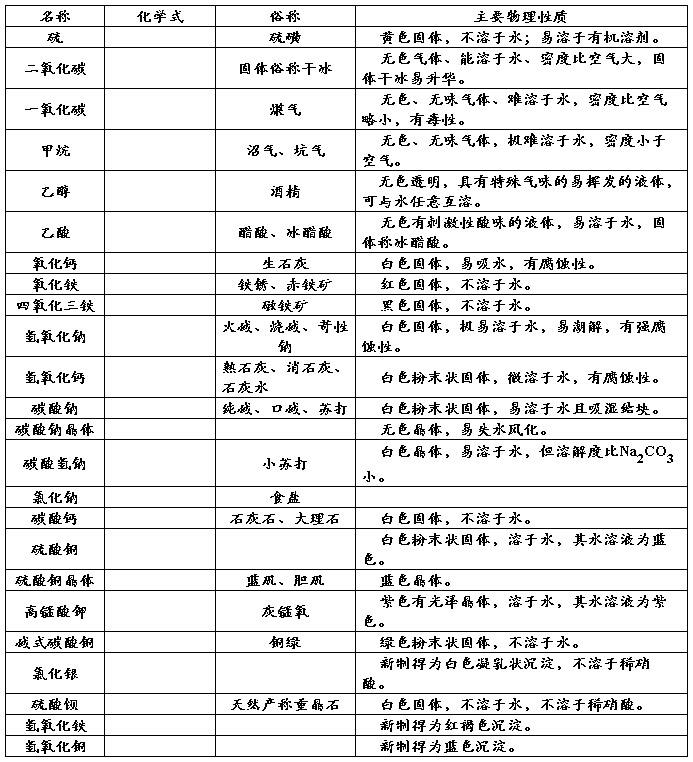

 (二)物质的分类 金属单质
(二)物质的分类 金属单质
 物 混合物 单质 非金属单质 酸性氧化物
物 混合物 单质 非金属单质 酸性氧化物