班别 小组 姓名
高中有机化学方程式汇总

…… …… 余下全文
天堂de果冻专业贡献
高中有机化学方程式汇总
1. CH4 + Cl光照
CH3Cl + HCl 2. CH3Cl + Cl光照 CH2Cl2 + HCl
3. CH光照
2Cl + Cl CHCl3 + HCl 4. CHCl光照
3 + Cl CCl4+ HCl 5. CH高温
C +2H2
6. C 催化剂 16H34加热、加压
C8H18 + C8H16
7. CH3CaO △ CH4↑+ Na2CO3
8. CH2 = CH2 + Br CH2Br—CH2Br 9. CH2 = CH22OH
10. CH2 = CH23—CH2
Br 11. CH2 = CH2CH3 12. nCH2 = CH
2
13. nCH22-CH=CH-CH 14. 2CH
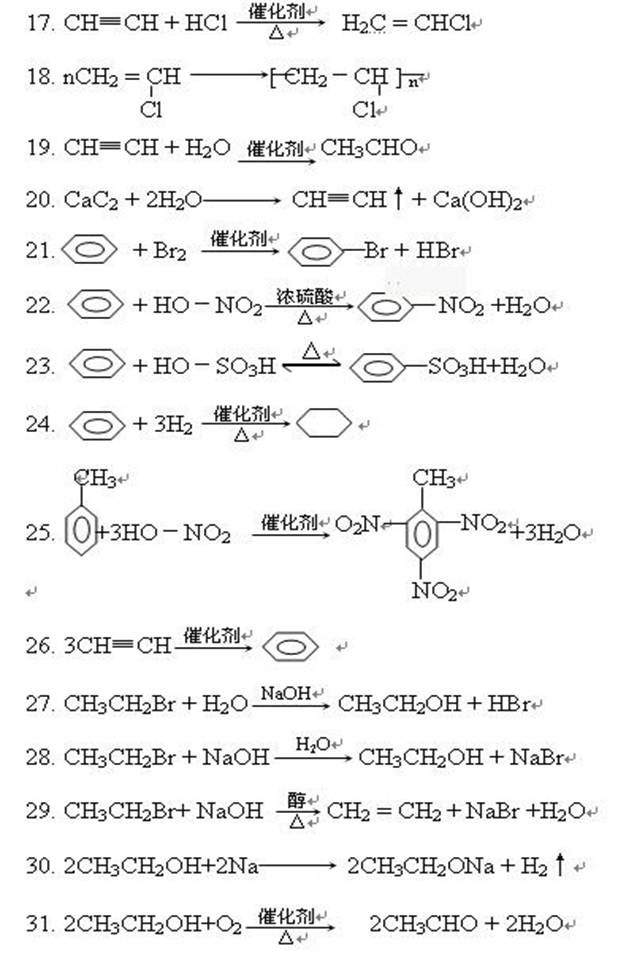
23CHO 15. CH≡CH + Br2CHBr = CHBr 16. CHBr = CHBr+ Br CHBr2-CHBr2 17. CH≡CH + HCl 催化剂 △ H2C = CHCl 18. nCH22- Cl Cl 19. CH≡CH + H2O 催化剂
CH3CHO
20. CaC2 + 2H2CH≡CH↑+ Ca(OH)2 + Br
2+ HO
2 +H2O 23. + HO3H+H2O 24. + 3H
2
O
26. 3CH≡
27. CH3CH228. CH3CH2
29. CH3CH2
2O
30. 2CH3CH22CH3CH2ONa + H2↑
31. 2CH3CH2OH+O2 催化剂
△
2CH3CHO + 2H2O
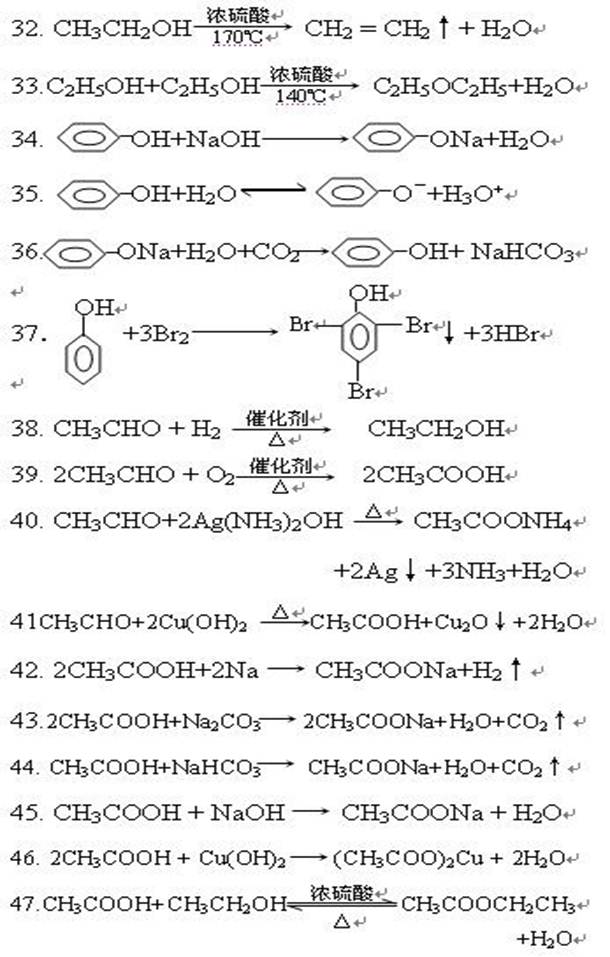
32. CH浓硫酸
3CH2170℃ CH2 = CH2↑+ H2O 33.C2H5OH+C2H5浓硫酸140℃
C2H5OC2H5+H2O 2O 2-
…… …… 余下全文
高中有机化学方程式总结
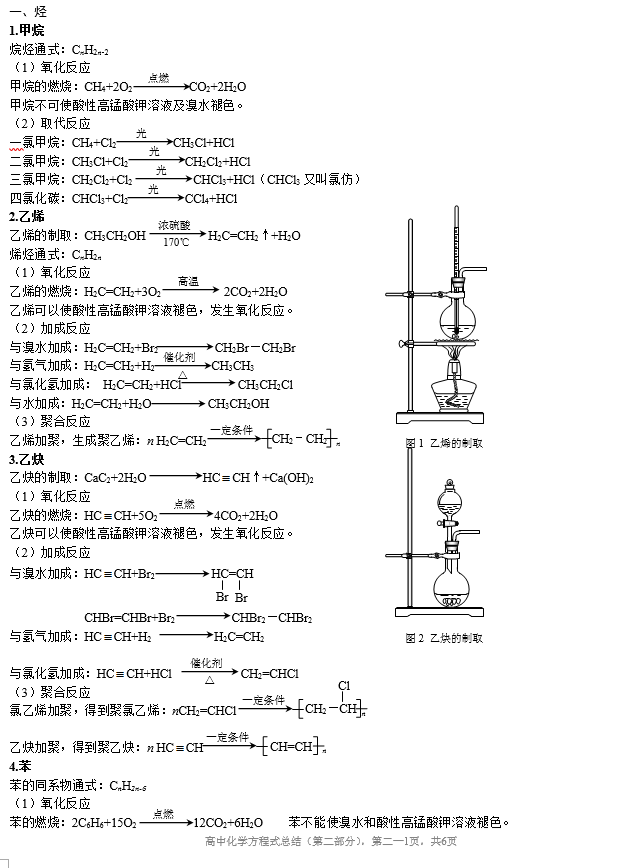
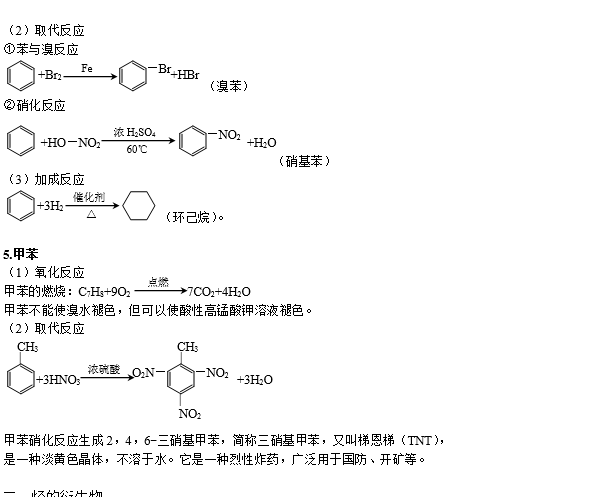
二、烃的衍生物
烃的衍生物的重要类别和主要化学性质:

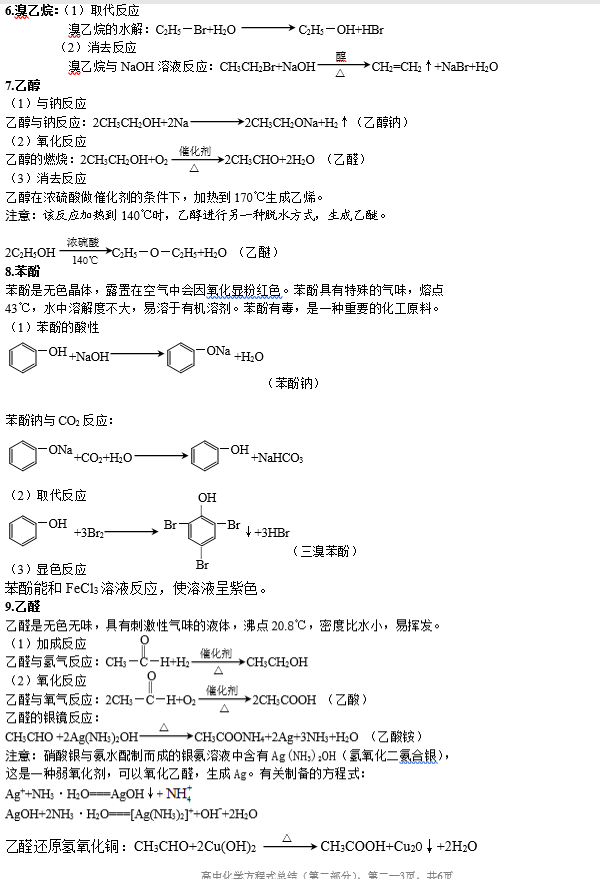
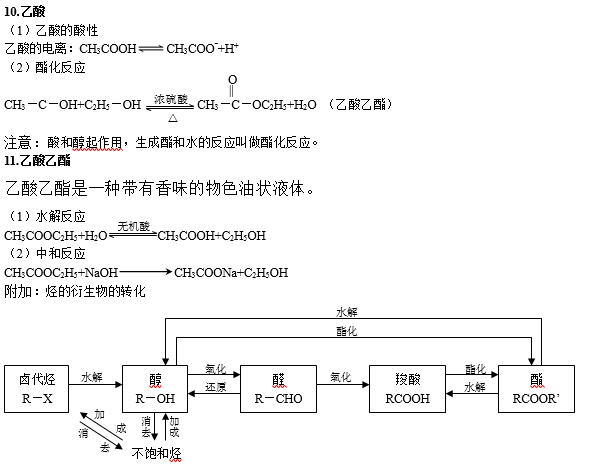
高中有机化学知识点总结
1.需水浴加热的反应有: (1)、银镜反应(2)、乙酸乙酯的水解(3)苯的硝化(4)糖的水解 (5)、酚醛树脂的制取(6)固体溶解度的测定 凡是在不高于100℃的条件下反应,均可用水浴加热,其优点:温度变化平稳,不会大起大落,有利于反应的进行。
2.需用温度计的实验有: (1)、实验室制乙烯(170℃) (2)、蒸馏 (3)、固体溶解度的测定 (4)、乙酸乙酯的水解(70-80℃) (5)、中和热的测定 (6)制硝基苯(50-60℃) 〔说明〕:(1)凡需要准确控制温度者均需用温度计。(2)注意温度计水银球的位置。
3.能与Na反应的有机物有: 醇、酚、羧酸等——凡含羟基的化合物。
4.能发生银镜反应的物质有: 醛、甲酸、甲酸盐、甲酸酯、葡萄糖、麦芽糖——凡含醛基的物质。
5.能使高锰酸钾酸性溶液褪色的物质有: (1)含有碳碳双键、碳碳叁键的烃和烃的衍生物、苯的同系物 (2)含有羟基的化合物如醇和酚类物质 (3)含有醛基的化合物 (4)具有还原性的无机物(如SO2、FeSO4、KI、HCl、H2O2等)
6.能使溴水褪色的物质有: (1)含有碳碳双键和碳碳叁键的烃和烃的衍生物(加成) (2)苯酚等酚类物质(取代) (3)含醛基物质(氧化) (4)碱性物质(如NaOH、Na2CO3)(氧化还原――歧化反应) (5)较强的无机还原剂(如SO2、KI、FeSO4等)(氧化) (6)有机溶剂(如苯和苯的同系物、四氯甲烷、汽油、已烷等,属于萃取,使水层褪色而有机层呈橙红色。)
…… …… 余下全文
高中有机化学方程式总结


二、烃的衍生物
烃的衍生物的重要类别和主要化学性质:



高中有机化学知识点总结
1.需水浴加热的反应有: (1)、银镜反应(2)、乙酸乙酯的水解(3)苯的硝化(4)糖的水解 (5)、酚醛树脂的制取(6)固体溶解度的测定 凡是在不高于100℃的条件下反应,均可用水浴加热,其优点:温度变化平稳,不会大起大落,有利于反应的进行。
2.需用温度计的实验有: (1)、实验室制乙烯(170℃) (2)、蒸馏 (3)、固体溶解度的测定 (4)、乙酸乙酯的水解(70-80℃) (5)、中和热的测定 (6)制硝基苯(50-60℃) 〔说明〕:(1)凡需要准确控制温度者均需用温度计。(2)注意温度计水银球的位置。
3.能与Na反应的有机物有: 醇、酚、羧酸等——凡含羟基的化合物。
4.能发生银镜反应的物质有: 醛、甲酸、甲酸盐、甲酸酯、葡萄糖、麦芽糖——凡含醛基的物质。
5.能使高锰酸钾酸性溶液褪色的物质有: (1)含有碳碳双键、碳碳叁键的烃和烃的衍生物、苯的同系物 (2)含有羟基的化合物如醇和酚类物质 (3)含有醛基的化合物 (4)具有还原性的无机物(如SO2、FeSO4、KI、HCl、H2O2等)
6.能使溴水褪色的物质有: (1)含有碳碳双键和碳碳叁键的烃和烃的衍生物(加成) (2)苯酚等酚类物质(取代) (3)含醛基物质(氧化) (4)碱性物质(如NaOH、Na2CO3)(氧化还原――歧化反应) (5)较强的无机还原剂(如SO2、KI、FeSO4等)(氧化) (6)有机溶剂(如苯和苯的同系物、四氯甲烷、汽油、已烷等,属于萃取,使水层褪色而有机层呈橙红色。)
…… …… 余下全文
高中有机化学方程式总结


二、烃的衍生物
烃的衍生物的重要类别和主要化学性质:



高中有机化学知识点总结
1.需水浴加热的反应有: (1)、银镜反应(2)、乙酸乙酯的水解(3)苯的硝化(4)糖的水解 (5)、酚醛树脂的制取(6)固体溶解度的测定 凡是在不高于100℃的条件下反应,均可用水浴加热,其优点:温度变化平稳,不会大起大落,有利于反应的进行。
2.需用温度计的实验有: (1)、实验室制乙烯(170℃) (2)、蒸馏 (3)、固体溶解度的测定 (4)、乙酸乙酯的水解(70-80℃) (5)、中和热的测定 (6)制硝基苯(50-60℃) 〔说明〕:(1)凡需要准确控制温度者均需用温度计。(2)注意温度计水银球的位置。
3.能与Na反应的有机物有: 醇、酚、羧酸等——凡含羟基的化合物。
4.能发生银镜反应的物质有: 醛、甲酸、甲酸盐、甲酸酯、葡萄糖、麦芽糖——凡含醛基的物质。
5.能使高锰酸钾酸性溶液褪色的物质有: (1)含有碳碳双键、碳碳叁键的烃和烃的衍生物、苯的同系物 (2)含有羟基的化合物如醇和酚类物质 (3)含有醛基的化合物 (4)具有还原性的无机物(如SO2、FeSO4、KI、HCl、H2O2等)
6.能使溴水褪色的物质有: (1)含有碳碳双键和碳碳叁键的烃和烃的衍生物(加成) (2)苯酚等酚类物质(取代) (3)含醛基物质(氧化) (4)碱性物质(如NaOH、Na2CO3)(氧化还原――歧化反应) (5)较强的无机还原剂(如SO2、KI、FeSO4等)(氧化) (6)有机溶剂(如苯和苯的同系物、四氯甲烷、汽油、已烷等,属于萃取,使水层褪色而有机层呈橙红色。)
…… …… 余下全文
让我发疯的有机化学方程式和高中有机化学方程式总结


一、各类化合物的鉴别方法
1.烯烃、二烯、炔烃:
(1)溴的四氯化碳溶液,红色腿去
(2)高锰酸钾溶液,紫色腿去。
2.含有炔氢的炔烃:
(1) 硝酸银,生成炔化银白色沉淀
(2) 氯化亚铜的氨溶液,生成炔化亚铜红色沉淀。
3.小环烃:三、四元脂环烃可使溴的四氯化碳溶液腿色
4.卤代烃:硝酸银的醇溶液,生成卤化银沉淀;不同结构的卤代烃生成沉淀的速度不同,叔卤代烃和烯丙式卤代烃最快,仲卤代烃次之,伯卤代烃需加热才出现沉淀。
5.醇:
(1) 与金属钠反应放出氢气(鉴别6个碳原子以下的醇);
(2) 用卢卡斯试剂鉴别伯、仲、叔醇,叔醇立刻变浑浊,仲醇放置后变浑浊,伯醇放置后也无变化。
6.酚或烯醇类化合物:
(1) 用三氯化铁溶液产生颜色(苯酚产生兰紫色)。
(2) 苯酚与溴水生成三溴苯酚白色沉淀。
7.羰基化合物:
(1) 鉴别所有的醛酮:2,4-二硝基苯肼,产生黄色或橙红色沉淀;
(2) 区别醛与酮用托伦试剂,醛能生成银镜,而酮不能;
(3) 区别芳香醛与脂肪醛或酮与脂肪醛,用斐林试剂,脂肪醛生成砖红色沉淀,而酮和芳香醛不能;
(4) 鉴别甲基酮和具有结构的醇,用碘的氢氧化钠溶液,生成黄色的碘仿沉淀。
8.甲酸:用托伦试剂,甲酸能生成银镜,而其他酸不能。
9.胺:区别伯、仲、叔胺有两种方法
(1)用苯磺酰氯或对甲苯磺酰氯,在NaOH溶液中反应,伯胺生成的产物溶于NaOH;仲胺生成的产物不溶于NaOH溶液;叔胺不发生反应。
(2)用NaNO2+HCl:
脂肪胺:伯胺放出氮气,仲胺生成黄色油状物,叔胺不反应。
芳香胺:伯胺生成重氮盐,仲胺生成黄色油状物,叔胺生成绿色固体。
10.糖:
(1) 单糖都能与托伦试剂和斐林试剂作用,产生银镜或砖红色沉淀;
(2) 葡萄糖与果糖:用溴水可区别葡萄糖与果糖,葡萄糖能使溴水褪色,而果糖不能。
(3)麦芽糖与蔗糖:用托伦试剂或斐林试剂,麦芽糖可生成银镜或砖红色沉淀,而蔗糖不能。
…… …… 余下全文
高中有机化学方程式总结


二、烃的衍生物
烃的衍生物的重要类别和主要化学性质:



高中有机化学知识点总结
1.需水浴加热的反应有: (1)、银镜反应(2)、乙酸乙酯的水解(3)苯的硝化(4)糖的水解 (5)、酚醛树脂的制取(6)固体溶解度的测定 凡是在不高于100℃的条件下反应,均可用水浴加热,其优点:温度变化平稳,不会大起大落,有利于反应的进行。
2.需用温度计的实验有: (1)、实验室制乙烯(170℃) (2)、蒸馏 (3)、固体溶解度的测定 (4)、乙酸乙酯的水解(70-80℃) (5)、中和热的测定 (6)制硝基苯(50-60℃) 〔说明〕:(1)凡需要准确控制温度者均需用温度计。(2)注意温度计水银球的位置。
3.能与Na反应的有机物有: 醇、酚、羧酸等——凡含羟基的化合物。
4.能发生银镜反应的物质有: 醛、甲酸、甲酸盐、甲酸酯、葡萄糖、麦芽糖——凡含醛基的物质。
5.能使高锰酸钾酸性溶液褪色的物质有: (1)含有碳碳双键、碳碳叁键的烃和烃的衍生物、苯的同系物 (2)含有羟基的化合物如醇和酚类物质 (3)含有醛基的化合物 (4)具有还原性的无机物(如SO2、FeSO4、KI、HCl、H2O2等)
6.能使溴水褪色的物质有: (1)含有碳碳双键和碳碳叁键的烃和烃的衍生物(加成) (2)苯酚等酚类物质(取代) (3)含醛基物质(氧化) (4)碱性物质(如NaOH、Na2CO3)(氧化还原――歧化反应) (5)较强的无机还原剂(如SO2、KI、FeSO4等)(氧化) (6)有机溶剂(如苯和苯的同系物、四氯甲烷、汽油、已烷等,属于萃取,使水层褪色而有机层呈橙红色。)
…… …… 余下全文
