无机推断题题眼归纳
一、据特殊的物理性质
1常见的有颜色的物质:
S:黄;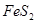 :黄;
:黄; :浅黄;
:浅黄;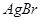 :浅黄;
:浅黄;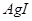 :黄色;
:黄色;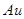 :黄:
:黄: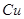 :黄;TNT:淡黄。
:黄;TNT:淡黄。
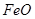 :黑;
:黑;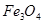 (磁性物质):黑色晶体;
(磁性物质):黑色晶体; :黑色;
:黑色;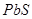 :黑色;
:黑色;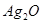 :棕黑色;
:棕黑色;
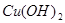 :蓝色;氢氧化铁:红褐色;氧化铁:红棕色
:蓝色;氢氧化铁:红褐色;氧化铁:红棕色
白色腊状固体:白磷;
离子颜色: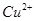 :蓝;
:蓝; :紫红;
:紫红;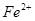 :浅绿;
:浅绿;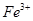 棕黄;
棕黄;
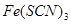 :血红;
:血红;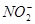 :浅黄;
:浅黄;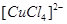 黄色;
黄色;
氯水浅黄绿色、 溴水橙黄色、 碘水棕黄色
溴的有机溶液:橙红—红棕、碘的有机溶液:紫红
氯气:黄绿色;二氧化氮:棕红;溴:蒸气红棕色;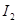 :蒸气紫色;
:蒸气紫色; :暗蓝;
:暗蓝;
2.物质的状态、气味硬度等:
呈液态的金属单质:Hg;呈液态的非金属单质:Br2
常温呈气态的单质:氢气、氧气、氯气、氮气、氟气、稀有气体等。
臭鸡蛋气味的气体:硫化氢
刺激性气味的气体:氯气,二氧化硫,氯化氢,氨气;
地壳中元素的含量:O Si Al Fe
硬度最大的单质:金刚石
形成化合物种类最多的元素:C
易升华的物质:碘和萘;
3.依据焰色反应判断元素:
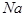 :黄色;Li 紫红、 Rb 紫、Ca 砖红、 Ba 黄绿、 Rb 紫、Sr 洋红。
:黄色;Li 紫红、 Rb 紫、Ca 砖红、 Ba 黄绿、 Rb 紫、Sr 洋红。
二、特殊的实验现象:
1.遇酚酞显红色或湿润红色石蕊试纸变蓝的气体: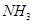 (碱性气体)
(碱性气体)
2.遇空气变为红棕色的气体: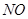
3.加碱产生白色沉淀,迅速变成灰绿色,最终变成红褐色,必有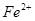
4.加苯酚显紫色或加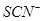 显血红色或加碱产生红褐色沉淀,必有
显血红色或加碱产生红褐色沉淀,必有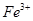
5.遇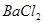 生成不溶于硝酸的白色沉淀,可能是:
生成不溶于硝酸的白色沉淀,可能是: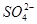 、
、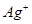 、
、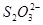
6.遇HCl生成沉淀,可能是: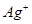 、
、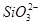 、
、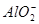 、
、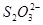
7.遇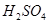 生成沉淀,可能是:
生成沉淀,可能是: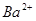 、
、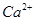 、
、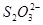 、
、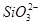 、
、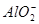
8.与硫化氢反应生成淡黄色沉淀的气体有 、
、 、
、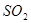 、
、
9.电解时阳极产生的气体一般是: 、
、 ,阴极产生的气体是:
,阴极产生的气体是: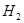
10.能使品红溶液褪色的气体可能是: 、
、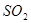 ;加热恢复原颜色的是
;加热恢复原颜色的是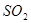 ,不恢复的是
,不恢复的是
11.能使品红溶液褪色的物质可能有: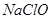 、
、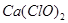 、氯水、过氧化钠、过氧化氢、活性碳;
、氯水、过氧化钠、过氧化氢、活性碳;
12.遇到淀粉碘化钾试纸变蓝的气体有: 、
、 、溴蒸气、碘蒸气
、溴蒸气、碘蒸气
三、特殊的反应条件和特征反应:
1.与碱反应产生气体
①铝:
②铵盐:
2.与酸反应产生气体
①活泼金属;
②弱酸盐;
③ 与酸反应既产生沉淀又生成气体:
与酸反应既产生沉淀又生成气体:
3.与水反应产生气体
①单质
②化合物:
③强烈双水解: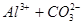 (
(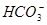 );
);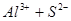 (
(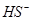 );
);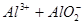 ;
;
4.与过氧化钠反应
5.既能酸反应,又能与碱反应
两性化合物: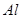 ,
,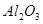 ,
, ,氨基酸;
,氨基酸;
弱酸的酸式盐: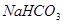 、
、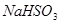 、
、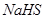 ;
;
弱酸的氨盐: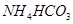 、
、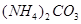 、
、 、
、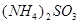 ,
,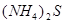 、
、 ;
;
6.电解
7.置换反应:
①金属→金属
②金属→非金属
③非金属→非金属
④非金属→金属
8.受热分解产生2种或3种气体的反应:
①铵盐:②硝酸盐:
③硝酸: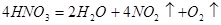 ;
;
④碱式碳酸铜: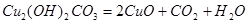 ;
;
10.同一元素的气态氢化物和气态氧化物反应,生成该元素的单质和水的元素可能是硫和氮
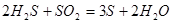 ;
;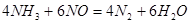
同一元素的气态氢化物和最高价氧化物对应的水化物生成盐的元素一定是氮
11.两种溶液混合生成沉淀和气体,这两种溶液的溶质可能是
①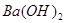 与
与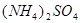 或
或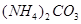 或
或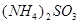
②可溶性铝盐与可溶性金属硫化物或可溶性碳酸盐或碳酸氢盐强烈双水解
③可溶性铁盐与可溶性碳酸盐或碳酸氢盐
④ 溶液与强酸
溶液与强酸
13.能使溴水褪色的物质:硫化氢和二氧化硫及它们相对应的盐、活泼金属、不饱和烃、醛、酚、碱;
14.两物质反应先沉淀后溶解的有:
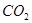 与
与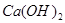 或
或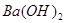 、
、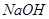 与铝盐、氨水与AgNO3、强酸与偏铝酸盐;
与铝盐、氨水与AgNO3、强酸与偏铝酸盐;
四、依据特征结构:
正四面体型分子: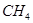 ,
,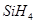 ,
,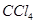 ,
,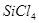 ,
,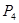 。
。
直线型分子:乙炔、二氧化碳、二硫化碳等。
平面型分子:苯、乙烯等;
常见的原子晶体:二氧化硅,硅,金刚石;
含有非极性共价键的离子化合物:过氧化钠( )、二硫化亚铁(
)、二硫化亚铁(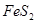 );
);
六、依据特殊工业制法:
●煅烧石灰石 ●工业合成氨●工业生产硝酸;●工业生产硫酸;●氯碱工业 ●电解水●高炉炼铁 ●工业上制取漂粉精;●工业制水煤气
七、依据题给数据:
相对分子质量为28:CO、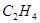 、
、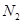 ; 相对分子质量为30: NO、
; 相对分子质量为30: NO、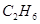 ;
;
相对分子质量为30: 、
、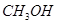 ;相对分子质量为44:
;相对分子质量为44: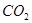 、
、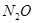 、
、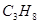 、
、 ;
;
相对分子质量为46: 、
、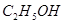 ;相对分子质量为78:
;相对分子质量为78: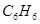 、
、 ;
;
相对分子质量为100: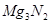 、
、 、
、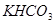
相对分子质量为120: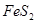 、
、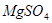 、
、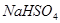 、
、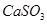 、
、
相对分子质量相差16一般是相差一个氧原子; 相邻同系物之间相差14
相同碳原子数目的饱和一元醇和饱和一元羧酸之间相差14
第二篇:高考化学_有机推断题眼总结
高中化学,有机推断题眼总结
性质
①能使溴水褪色的有机物通常含有“—C=C—”、“—C≡C—”或“—CHO”。
②能使酸性高锰酸钾溶液褪色的有机物通常含有“—C=C—”或“—C≡C—”、“—CHO”或为“苯的同系物”。
③能发生加成反应的有机物通常含有“—C=C—”、“—C≡C—”、“—CHO”或“苯环”,其中“—CHO”和“苯
环”只能与H2发生加成反应。
④能发生银镜反应或能与新制的Cu(OH)2悬浊液反应的有机物必含有“—CHO”。 ⑤能与钠反应放出H2的有机物必含有“—OH”、“—COOH”。
⑥能与Na2CO3或NaHCO3溶液反应放出CO2或使石蕊试液变红的有机物中必含有-COOH。
⑦能发生消去反应的有机物为醇或卤代烃。
⑧能发生水解反应的有机物为卤代烃、酯、糖或蛋白质。
⑨遇FeCl3溶液显紫色的有机物必含有酚羟基。
⑩能发生连续氧化的有机物是伯醇,即具有“—CH2OH”的醇。比如有机物A能发生如下反应:A→B→C,
则A应是具有“—CH2OH”的醇,B就是醛,C应是酸。
条件
1.光照 烷烃或烷基中的H被取代
2.浓硫酸,170℃ 乙醇脱水成乙烯
3.浓硫酸,140℃ 乙醇脱水成乙醚
4.浓硫酸加热 醇脱水成烯烃醇与羧酸反应成酯 酯的酸性水解
5.NaOH溶液 --X被取代成—OH
6.NaOH的醇溶液 --X消去成烯烃
7.H2,催化剂,△ 烯烃或者醛的加成反应
8.Cu,O2,△ 醇催化氧化成醛
9.[O] 醇氧化成醛或羧酸或醛氧化成羧酸
10.→,Fe 苯环上的氢被取代
11.Br2或Br2得CCl4溶液 加成反应
①当反应条件为NaOH醇溶液并加热时,必定为卤代烃的消去反应。
②当反应条件为NaOH水溶液并加热时,通常为卤代烃或酯的水解反应。
③当反应条件为浓H2SO4并加热时,通常为醇脱水生成醚或不饱化合物,或者是醇与酸的酯化反应。
④当反应条件为稀酸并加热时,通常为酯或淀粉的水解反应。
⑤当反应条件为催化剂并有氧气时,通常是醇氧化为醛或醛氧化为酸。
⑥当反应条件为催化剂存在下的加氢反应时,通常为碳碳双键 、碳碳叁键、苯环或醛基的加成反应。
⑦当反应条件为光照且与X2反应时,通常是X2与烷或苯环侧链烃基上的H原子发生的取代反应,
而当反应条件为催化剂存在且与X2的反应时,通常为苯环上的H原子直接被取代。 数据
①根据与H2加成时所消耗H2的物质的量进行突破:1mol—C=C—加成时需1molH2,1mol—C≡C—
完全加成时需2molH2,1mol—CHO加成时需1molH2,而1mol苯环加成时需3molH2。 ②1mol—CHO完全反应时生成2molAg↓或1molCu2O↓。
③2mol—OH或2mol—COOH与活泼金属反应放出1molH2。
④1mol—COOH与碳酸钠或碳酸氢钠溶液反应放出1molCO2↑。
⑤1mol一元醇与足量乙酸反应生成1mol酯时,其相对分子质量将增加42,1mol二元醇与足量乙酸
反应生成酯时,其相对分子质量将增加84。
⑥1mol某酯A发生水解反应生成B和乙酸时,若A与B的相对分子质量相差42,则生成1mol乙酸,
若A与B的相对分子质量相差84时,则生成2mol乙酸。
结构
①具有4原子共线的可能含碳碳叁键。 ②具有4原子共面的可能含醛基。 ③具有6原子共面的可能含碳碳双键。 ④具有12原子共面的应含有苯环。 通式
符合CnH2n+2为烷烃,符合CnH2n为烯烃,符合CnH2n-2为炔烃,符合CnH2n-6为苯的同系物,符合
CnH2n+2O为醇或醚,符合CnH2nO为醛或酮,符合CnH2nO2为一元饱和脂肪酸或其与一元饱和醇生成
的酯。
物理性质
在通常状况下为气态的烃,其碳原子数均小于或等于4,而烃的衍生物中只有CH3Cl、CH2=CHCl、
HCHO在通常情况下是气态。
特殊性
1.能与Na反应 醇羟基,酚羟基,羧基
2.能与NaOH溶液反应 酚羟基,羧基;卤代烃;酯基
3.能与Na2CO3溶液反应 酚羟基,羧基
4.能与Na2CO3溶液反应放↑ 羧基
5.能与NaHCO3溶液反应 羧基
颜色变化
1.苯酚遇氯化铁溶液 紫色
2.苯酚遇浓溴水 白色↓
3.蛋白质遇浓硝酸 黄色
4.苯酚在空气中被氧气氧化为红色
