大学生创办企业房租补贴申请表0903
序号: 申请时间:

此表一式三份
第二篇:大创表格
一、国内外研究现状、趋势
大约在1600年,中世纪杰出的医生Parcelsus用一种植物的春提取物还原氯金酸制备得到“饮用金”,这就是纳米金。而在20世纪80年代初德裹科学家H.Gleiter教授提出纳米晶体材料的概念并首次获得了纳米金属银、铜、铝等块体材料,引起了国际上的关注。
1857年,法拉第对纳米金作了系统的科学研究,他制备的金颗粒可以在数十年仍然保持原有的性质,极为稳定,并且发现在其中加入少量电解质后,可是它有红色变成蓝色,终至凝集为无色,而加明胶等大分子物质后便可以组织这种变化,之一重大发现奠定了纳米金颗粒在实际应用中的科学基础。
在纳米材料的研究热潮中,金属纳米材料独特的光、电、催化等特性及其在新能源研究、光电信息存储、生物医疗等领域的应用收到相关研究领域的广泛关注。贵金属(尤其是Au、Pd和Ag)纳米材料呈现出较为丰富的光学和电学特性。它们良好的稳定和广阔的应用前景也引起国际上物理、化学、材料等众多领域研究人员的广泛关注。目前很多科研组应用多羟基过程合成了贵金属纳米棒、纳米片、多面体、空壳等纳米结构,研究了它们的可调制光吸收特性、催化活性及局域场增强效应与形貌的结构相关性。

图示1:一些新奇形貌Au微米片的透射电镜图像及衍射分析
贵金属纳米结构的性质与其尺寸和形状有很大关系,因此,发展简便的、形状和尺寸可控的合成方法尤其重要。目前,研究人员可以通过多种化学方法合成不同形貌、不同成分及多功能的纳米材料。由于化学合成是从分子层器对物质进行操作,因而可以得到好的化学均匀性;而溶液反应法对粒子尺寸、形状较易控制,所以目前贵金属纳米粒子的制备广泛采用基于液相的化学方法。化学方法包括末班辅助沉积方法,化学还原方法,种子调制生长方法和光还原方法等。
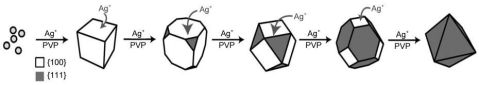
图示2:多面体形状的Ag纳米晶体的演化过程
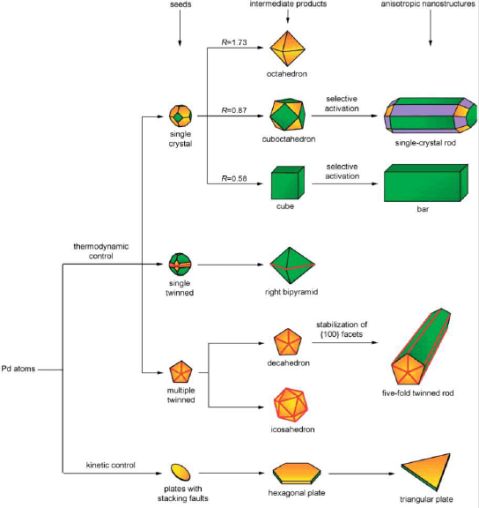
图示3:形成不同形状Pd纳米结构的反应过程示意图
1、模板法
模板法常用来合成棒状、线状和管状的贵金属纳米结构. 在这种方法中, 金属离子在局限的模板中被还原, 这些受限的空间结构可以控制颗粒的成核与生长, 从而形成特定形貌的纳米颗粒. 模板通常分为软模板和硬模板. 软模板包括胶束, 微乳剂,DNA等.例如, 以十六烷基三甲基溴化铵(CTAB)分子有序组合形成的棒状胶束作为模板来合成直径和纵横比可控的Au 或Ag 的纳米棒或纳米线.硬模板包括碳纳米管, 有孔薄膜, 介孔材料等.这种方法通常用来合成高密度、整齐排列的纳米棒、纳米线和纳米管. 例如, Martin最早用这种方法合成了Au纳米棒.
2、晶种法
晶种法起始于上世纪90 年代, 目前已被广泛应用于合成贵金属纳米颗粒. 晶种法制备金属纳米颗粒可以分为两步(以Au为例): 第一步是利用少量的强还原剂还原Au3+成微小的Au颗粒作为晶种; 第二步则是在含有Au3+的生长溶液中, 采用弱还原剂使Au3+还原成Au+, 再与晶种结合, Au+在已经形成的晶种上被进一步还原而生长成Au 颗粒. 用这种方法,在室温下能够制备Au 纳米棒、纳米线、立方体, Ag纳米片和Pd 的立方体. 例如, Smith 等利用晶种法合成了Au 纳米棒. 这种方法最大的优势是避免了二次成核, 很容易得到不同形状和尺寸可控的纳米颗粒.
3、电化学沉积法
电化学沉积法是通过外加电场在电解质溶液里诱导化学反应来制备纳米颗粒的方法. 在电化学沉积法中又可通过有模板法和无模板法来制备纳米颗粒. 在有模板法中, 通过特定的模板利用电化学沉积可以得到不同形貌的贵金属纳米颗粒, 如纳米线、纳米棒、纳米管等. 例如Wang小组最早通过电化学沉积方法得到Au 纳米棒. 模板的合成与选择是电化学沉积法合成贵金属纳米颗粒和纳米结构的关键. 纳米颗粒的尺寸和形貌可以通过调节实验参数(包括沉积过程中的电压、温度、沉积时间、通过的电量、适当的表面活性剂等)来控制.与此同时, 人们也在不断地探索各种无模板存在下的合成方法, 例如Yu 等以及后来的其他研究人员已经在无模板条件下利用电化学沉积法制备出不同纵横比的纳米棒.
4、化学还原法
最常用的化学方法是多羟基还原法. 在室温下, 乙二醇(通常作为溶剂和还原剂), 柠檬酸和聚乙烯吡咯烷酮(PVP)或聚乙烯醇(PVA)等表面活性剂的还原性较低. 然而, 这些化学试剂在高温下具有较强的还原性, 所以多羟基方法一般都是在高温下进行. 最近, 我们在室温条件下研究了PVP 对金属离子的还原作用及对纳米结构生长的影响.在多羟基方法中, 通过引入表面活性剂PVP、PVA、CTAB等来限制晶核的某一晶面在一定尺寸范围内生长, 并通过调节反应参数获得形态丰富的纳米结构. 除此之外, 葡萄糖, 二甲基甲酰胺(DMF)等弱还原剂也用于合成贵金属纳米颗粒.
5、光化学合成法
许多贵金属离子在电磁波(可见光、高能射线、高能电子束、紫外光)作用下能够发生还原反应而得到贵金属单质.例如, 紫外光已经成功地用于制备形貌可控的Au、Ag纳米颗粒.除此之外, Jin等也用光化学合成法实现了球形的Ag纳米颗粒向三角形的Ag纳米棱柱体的转化
6、超生辐射法
超声波技术在化学特别是材料化学领域中的应用是一门新兴的学科. 其基本原理是利用超声空化作用, 即液体中的空化气泡在声场的作用下发生振动生长并且崩溃闭合; 在这一绝热过程中泡内的气体或蒸汽迅速被压缩而产生瞬态的局域高温、高压, 诱发溶液体系发生电离和激发, 使其产生溶剂化电子、离子和自由基.在水溶液或有机溶剂中,超声的空化作用使水溶液或有机溶液中产生H·和 OH·等还原性自由基, 从而还原相应的金属盐制备纳米材料. 这里以HAuCl4水溶液制备金纳米粒子为例,说明超声还原的机理. 水分子吸收超声能量产生H·和HO·自由基, 使溶液中Au3+还原为Au原子,进而形成金纳米粒子, 反应式如下: H2O→H·+HO·
Au3++3H·→Au+3H+
nAu→(Au)n
利用超声还原法主要是制备贵金属纳米颗粒及其复合结构,颗粒尺寸或结构可以通过改变前驱体中贵金属离子的浓度与添加顺序来调节。
另外,研究者也发现纳米贵金属颗粒在电化学催化方面也有很多的应用。由于贵金属本身就具有优良的催化活性,如果将其制成具有特殊形貌的纳米颗粒
后,它的表面积能够大大增加,且具有丰富的悬空键,因此是活性更高、选择性更好的催化剂。
金以其独特的化学性质,很早就被人们广泛地应用于生产生活的各个领域。但是长期以来进一直被认为是催化惰性的金属元素。自从19xx年Huber等人报道了金在30-40K时对CO氧化具有反应活性以来,金催化剂开始受到广泛关注,随之开展了大量金催化剂在多相或者均相催化中的应用研究,并且取得许多可贵的科研成果。Haruta 等用共沉淀法制备高分散担载金催化剂, 用于对一氧化碳的低温消除, 取得了极好的效果。而Pt 和Pd 修饰的金催化剂Au-Pt/ Co3O4 和Au-Pd/ Co3O4 ,对CH4 的低温燃烧有着很好的活性并且是富氧条件下H2和CO共氧化最有效的催化剂。Au/ NiFe2 O4催 化 剂 对 三 甲胺((CH3)3N) 的消除效果也比Pt、Pd 强。金催化剂在均相催化反应中的应用研究也取得了很好的结果,例如均相催化Aldol 缩合制备氨基酸、催化醇炔加成以及催化胺羰化制备氨基甲酸酯和己二酰胺等。这些都表明金催化剂在基础研究领域和工业应用中都具有巨大潜力, 客观上也为金催化剂的工业应用奠定了一定的基础。
与此同时,由于许多反应所用的催化剂均属贵金属催化体系,用价格相对低廉的金催化剂代替价格昂贵的Pd、Rh等贵金属在科学研究和工业生产上均具有重要的意义。在工业化进程中,金催化剂已经在日本成功地应用于化学传感器、燃料电池和厕所异味的消除等等。金催化剂催化甲醇氧化、以及催化葡萄糖氧化部分的研究结果并不尽如人意。Biella 等人采用金溶胶浸渍法制备了Al2O3、TiO2 及活性炭担载的金催化剂, 将之用于氨基醇、醛、D 葡萄糖的选择氧化, 并与商业Pd/ C、Pt / C 催化剂进行了比较
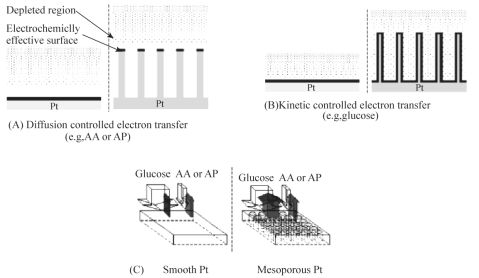
。实验以O2 为氧源, 在碱性条件下进行, 获得了非常好的效果。Au/ C 催化剂对于底物的转化率和产物的选择性都非常高, 催化效果和催化剂循环实验都比Pd/ C 和Pt / C 催化剂好。随着各种新型结构和形态的纳米材料的出现以及对特定反应分子在各种具有纳米结构的电极上电化学催化机理的深入探索,高灵敏度,高选择性和高稳定性的无酶传感器的制备,可望实现在实际中的应用。我们将具体在这些方面对特定晶型金的催化性能展开更具体深入的研究。
在这些前人的基础探究和应用探索的驱动下,我们小组将发展并改进多种
贵金属纳米结构的制备方法,通过比较同一晶型不同形貌的贵金属的催化能力,不仅分析其在光电传感器等光电方面的应用,同时尽可能将其理论知识进行完善,指导和致力于未来的实际生产中。
参考文献:
【1】 Wang, F.; Li, C. H.; Sun, L. D. ; Wu, H. S.; Ming, T .; Wang, J.F.; Yu, J. C.; Yan,
C. H. J.
【2】 Am. Chem. Soc. 2011, 133, 1106
【3】 Zijlstra, P.; Chon, J.W. M.; Gu , N. Nature 2009, 459, 410.
【4】Anker, J. N.; Hall, W . P.; Lyandres, O.; Shah, N. C.; Zhao, J. ;Van Duyne, R. P. Nature Materials 2008, 7, 442.
【5】Zhang, Q.; Ge, J. P.; Pham, T.; Goebl, J.; Hu, Y. X.; Lu, Z. D ; Yin, Y. D. Angew. Chem. 2009, 121, 3568.
【6】Kim, F.; Song, J. H.; Yang, P. J. Am. Chem. Soc. 2002, 124, 14316.
【7】Zhou, Z. Chinese Bulletin of Life Sciences 2009, 21, 461.
【8】Zijlstra, P.; Chon, J.W. M.; Gu, N. Nature 2009, 459, 410.
【9】Anker, J. N.; Hall,W. P.; Lyandres, O.; Shah, N. C.; Zhao, J.;Van Duyne, R. P. Nature Materials 2008, 7, 442.
【10】Huber H, McIntosh D, O zin G A. Inorg. Chem. , 1977, 16( 5) : 975—979
【11】 Bond G C, Thompson D T. Catal. Rev. -Sci. En g. , 1999, 41: 319—324
【12】王桂英( Wang G Y) , 余加佑( Yu J Y) , 廉红蕾( Lian H L) 等. 高等学校化学学报( Chem. J. Chinese Universities ) , 2000, 21( 5) : 752—756
【13】Sanchez A, Abbet S , Heiz U. J. Phys. Ch em. A, 1999, 103: 9573—9578
【14】Haruta M, Yamada N, Kobayashi T , et al. J . Cat al . , 1989, 115( 2) : 301—309
【15】Miao S , Deng Y. Ap pl Cat al. B, 2001, 31( 3) : L1—L4
【16】 Miao S, Deng Y. International Catalysis Workshop f or Young Scienst s , Beijing September, 2001
【17】缪少军( Miao S J) , 邓友全( Deng Y Q) . 催化学报( Chinese J. Cat al. ) , 2001, 5( 22) : 461—464
【18】Ueda A, Haruta M, Shigen K. Resources and Environment , 1992, 28: 1035
【19】Golunsk i S. International Conference on Catalytic Gold, Cape Town, South Africa, 2-5 Apri 2001
【20】 Biella S , Castiglioni G L, Fumagalli C , et al. Ca tal. Today , 2002, 72 : 43 — 49
