实验二 多管发酵法测定水中大肠菌群总数
一.实验目的和要求
1.掌握多管发酵法测定水中大肠菌群的技术。
2.巩固细菌学检验法的内容。
二.原理
总大肠菌群可用多管发酵法或滤膜法检验。多管发酵法的原理是根据大肠菌群能发酵乳糖、产酸、产气,以及具备革兰氏染色阴性,无芽孢,呈杆状等有关特性,通过三个步骤进行检验求得水样中的总大肠菌群数。试验结果以最可能数(most probable number),简称MPN表示。
三.仪器
(1)高压蒸气灭菌器。
(2)恒温培养箱、冰箱。
(3)生物显微镜、载玻片。
(4)酒精灯、镍铬丝接种棒。
(5)培养皿(直径100mm)、试管(5×150mm),吸管(1、5、10mL)、烧杯(200、500、2000mL)、锥形瓶(500、1000mL)、采样瓶。
四.测定步骤
1.生活饮用水:
①初发酵试验:在两个装有已灭菌的50mL三倍浓缩乳糖蛋白胨培养液的大试管或烧瓶中(内有倒管),以无菌操作各加入已充分混匀的水样100mL。在10支装有已灭菌的5mL三倍浓缩乳糖蛋白胨培养液的试管中(内有倒管),以无菌操作加入充分混匀的水样10mL混匀后置于37℃恒温箱内培养24h。
②复发酵试验:上述涂片镜检的菌落如为革兰氏阴性无芽孢的杆菌,则挑选该菌落的另一部分接种于装有普通浓度乳糖蛋白胨培养液的试管中(内有倒管),每管可接种分离自同一初发酵管(瓶)的最典型菌落1~3个,然后置于37℃恒温箱中培养24h,有产酸、产气者(不论倒管内气体多少皆作为产气论),即证实有大肠菌群存在。根据证实有大肠菌群存在的阳性管(瓶)数查附表1“大肠菌群检数表”,报告每升水样中的大肠菌群数。
2.水源水
①于各装有5mL三倍浓缩乳糖蛋白胨培养液的5个试管中(内有倒管),分别加入10mL水样;于各装有10mL乳糖蛋白胨培养液的5个试管中(内有倒管),分别加入1mL水样;再于各装有10mL乳糖蛋白胨培养液的5个试管中(内有倒管),分别加入1mL 1∶10稀释的水样。共计15管,三个稀释度。将各管充分混匀,置于37℃恒温箱内培养24h。
②根据证实总大肠菌群存在的阳性管数,查附表2“最可能数(MPN)表”,即求得每100mL水样中存在的总大肠菌群数。我国目前系以1L为报告单位,故MPN值再乘以10,即位1L水样中的总大肠菌群数。
例如,某水样接种10mL的5管均为阳性;接种1mL的5管中有2管为阳性;接种1∶10的水样1mL的5管均为阴性。从最可能数(MPN)表中查检验结果5~2~0,得知100mL水样中的总大肠菌群数为49个,故1L水样中的总大肠菌群数为49×10=490个。
对污染严重的地表水和废水,初发酵试验的接种水样应做1∶10、1∶100、1∶1000或更高倍数的稀释,检验步骤同“水源水”检验方法。
如果接种的水样量不是10mL、1mL和0.1mL,而是较低或较高的三个浓度的水样量,也可查表求得MPN指数,再经下面公式换算成每100mL的MPN值:

附表1 大肠菌群检数表
接种水样总量300mL(100mL2份,10mL10份)
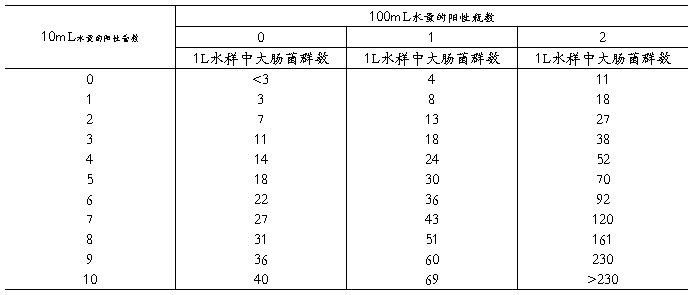
附表2 最可能数(MPN)表
(接种5份10mL水样、5份1mL水样、5份0.1mL水样时,不同阳性及阴性情况下100mL水样中细菌数的最可能数和95%可信限值)
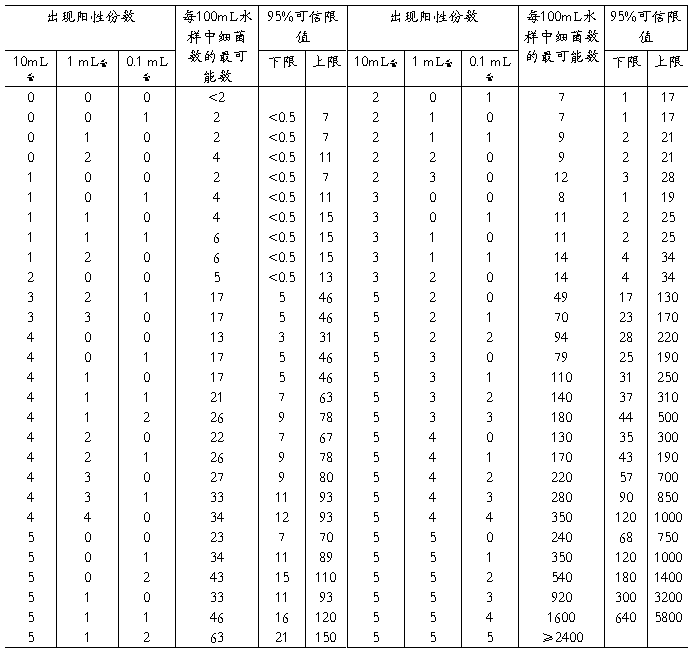
五、试验结果计算及分析。
第二篇:多管发酵法测定水中大肠菌群 实验报告
多管发酵法测定水中大肠菌群
摘要:初步发酵实验中将水样接种与乳糖蛋白胨液体培养基的发酵管内,37度下培养,24内小管中有气体形成,并且培养基浑浊,颜色改变,说明水中存在大肠杆菌,为阳性如果,如果出现产生气泡但不变色或者变色但不产气的情况,应该延长培养至48小时,若仍不的为阴性反应。平板分离实验中把初实验产期产酸的试管的菌接到伊红美兰琼脂平板上然后培养24小时。复发酵实验中将以上大肠杆菌阳性菌落,经涂色染色为革兰阴性无芽孢杆菌,通过次试验进一步证实
原理:初发酵实验:发酵管内装有乳糖蛋白胨液体培养基,并倒置一个杜氏小管。乳糖能其选着作用,因为很多细菌不能发酵乳糖,而大肠杆菌能发酵乳糖而产气产酸。为便于观察细菌的产酸情况,培养基内加有溴甲酚紫作为指示剂,细菌产酸后培养基由原来的紫色变为黄色。
初步发酵实验中将水样接种与乳糖蛋白胨液体培养基的发酵管内,37度下培养,24内小管中有气体形成,并且培养基浑浊,颜色改变,说明水中存在大肠杆菌,为阳性如果,如果出现产生气泡但不变色或者变色但不产气的情况,应该延长培养至48小时,若仍不产气的为阴性结果。
平板分离:伊红美兰琼脂培养基有伊红和美兰两种染料,在此作为指示剂,大肠杆菌发酵乳糖造成酸性环境时,该两种染料及结合,使培养基产生有金属光泽的深紫色菌落。
复发酵实验:以上大肠杆菌阴性菌落,经涂片染色为革兰氏阴性无芽孢的,通过此试验进一步证实。原理与初发酵实验相同,经24小时培养产酸产气的,最后确定为大肠杆菌阴性结果。
材料与用具:
1. 培养基
乳糖蛋白胨发酵管(内有倒置杜氏小管) 三倍浓缩乳糖蛋白胨发酵管(内有杜氏小管) 伊红美兰琼脂平板
2.无菌水
3. 用具
载玻片 灭菌带玻璃塞空瓶 灭菌试管 灭菌吸管
方法:
1水样的采取
从不同水体(自来水、河水)中采集样品
2自来水检查
(1)初发酵实验在2个含有50ml三倍浓缩的乳糖蛋白胨发酵烧瓶中,各加入100ml水样。在10支含有5ml三倍浓缩乳糖蛋白胨发酵管中,各加入10ml水样。混匀后,37度培养24小时,24小时候没产气的继续培养至48小时。
(2)平板分离经24小时培养后,将产气产酸及48小时产酸产气的发酵管,分别划线接种于伊红美兰琼脂平板上,再与37度下培养18到24小时,将符合一下特征的菌落
的一小部分,进行涂片,革兰染色,镜检。
1 深紫黑色、有金属光泽
2 紫黑色、不带或带金属光泽
3 但紫黑色、中心颜色较深
(3)复发酵实验进涂片、染色、镜检,如果为革兰阴性无芽孢杆菌,则挑去该菌落的另一部分,从新接种于普通浓度的乳糖蛋白胨发酵管中,每管可接种来自同一初发酵管的同类型菌落1到3个,37度培养24小时,结果若产气又产酸,即证明有大肠杆菌存在。
证实有大肠杆菌存在后,再根据初发酵实验的阳性管数查表1及可得大肠杆菌群数。
3河水的检查
(1)将水稀释成1:10与1:100.
(2)分别吸取1ml 1:10、1:100的稀释水样和1ml原水样,各入装有10ml普通浓度乳糖蛋白胨发酵管中。另外取10ml和100ml原水样,分别注入装有5ml和50ml三倍浓缩乳糖蛋白胨发酵液的试管中。
(3)以下步骤同上述自来水的平板分离和复发酵实验。
(4)将100ml、10ml、1ml、0.1ml水样的发酵管结果查表2
结果:自来水检查实验的结果为10ml水量的阳性管数为10 支,100ml水量的阳性管数为2支,经查表可知每升自来水样中大肠菌群数为>230.
河水检查实验结果为接种水样总量111.1ml试管中100ml、10ml、1ml、0.1ml的发酵情况为阳性,而接种水量为11.11试管中10ml、1ml、0.1ml的发酵情况为阳性,而0.01的发酵情况为阴性,查表可知每升河水的大肠菌群数为23800.
结果讨论:
1.水样的采集不具有代表性,可能会给实验结果带来误差。
2.自来水检测试管实验中没有发酵烧瓶故用三角瓶代替,而加入杜氏小管后气不能直立,如果结果产气的话不能很好的判断,因而会给实验结果带来误差。
3.在进行革兰氏染色时可能会引入其他的革兰氏阴性菌,使结果出现误差。
4.河水检查试管中水样稀释不均匀,也会给实验结果带来误差。
参考文献:全桂静,雷晓燕,李辉,微生物学实验指导,北京,化学工业出版社,2010.



图1 5ml三倍浓缩乳糖蛋白 图2培养24小时后河水的产气和 图3培养24小时后自来
胨发酵管培养前颜色 颜色变化情况 水的产气和颜色变化情况


图4 图5
平板分离实验的伊红美兰培养基的长菌情况



图6复发酵实验中普通浓度 图7 24h培养后自来水的颜 图8 24h培养后河水的颜
乳糖蛋白胨发酵管培养前颜色 色变化和产气情况 色变化和产气情况


图924h培养后接种100ml河水的 图1024h培养后接种100ml自来水的
颜色变化和产气情况 颜色变化和产气情况
