米氏常数是酶的特征性常数,可用来表示酶和底物亲和力的大小。米氏常数与底物浓度和酶浓度无关,而受温度和pH值的影响,竞争性抑制剂米氏常数增大,最大反应速度不变;非竞争性抑制剂米氏常数不变,最大反应速度减小;反竞争性抑制剂米氏常数减小,最大反应速度减小。
Km:米氏常数,是研究酶促反应动力学最重要的常数。它的意义如下: 它的数值等于酶促反应达到其最大速度Vm一半时的底物浓度〔S〕,图示以及公式推导。 它可以表示E与S之间的亲和能力,Km值越大,亲和能力越强,反之亦然。 它可以确定一条代谢途径中的限速步骤:代谢途径是指由一系列彼此密切相关的生化反应组成的代谢过程,前面一步反应的产物正好是后面一步反应的底物,例如,EMP途径。限速步骤就是一条代谢途径中反应最慢的那一步,Km值最大的那一步反应就是,该酶也叫这条途径的关键酶。 它可以用来判断酶的最适底物,某些酶可以催化几种不同的生化反应,叫多功能酶,其中Km值最小的那个反应的底物就是酶的最适底物。 Km是一种酶的特征常数,只与酶的种类有关而与酶的浓度无关,与底物的浓度也无关,这一点与Vm是不同的,因此,我们可以通过Km值来鉴别酶的种类。但是它会随着反应条件(T、PH)的改变而改变。
米氏常数是酶的特征性常数,可用来表示酶和底物亲和力的大小。米氏常数与底物浓度和酶浓度无关,而受温度和pH值的影响,竞争性抑制剂米氏常数增大,最大反应速度不变;非竞争性抑制剂米氏常数不变,最大反应速度减小;反竞争性抑制剂米氏常数减小,最大反应速度减小。
Km:米氏常数,是研究酶促反应动力学最重要的常数。它的意义如下: 它的数值等于酶促反应达到其最大速度Vm一半时的底物浓度〔S〕,图示以及公式推导。 它可以表示E与S之间的亲和能力,Km值越大,亲和能力越强,反之亦然。 它可以确定一条代谢途径中的限速步骤:代谢途径是指由一系列彼此密切相关的生化反应组成的代谢过程,前面一步反应的产物正好是后面一步反应的底物,例如,EMP途径。限速步骤就是一条代谢途径中反应最慢的那一步,Km值最大的那一步反应就是,该酶也叫这条途径的关键酶。 它可以用来判断酶的最适底物,某些酶可以催化几种不同的生化反应,叫多功能酶,其中Km值最小的那个反应的底物就是酶的最适底物。 Km是一种酶的特征常数,只与酶的种类有关而与酶的浓度无关,与底物的浓度也无关,这一点与Vm是不同的,因此,我们可以通过Km值来鉴别酶的种类。但是它会随着反应条件(T、PH)的改变而改变。
Michaelis & Menten 于19xx年推导出了上述矩形双曲线的数学表达式,即米氏方程: ν= Vmax[S]/(Km+[S])。其中,Vmax为最大反应速度,Km为米氏常数。
传统上,米氏方程动力学描述的是分子数量为1015的集体分子的行为,米氏方程在单分子水平上也是有效的。
⑶Km和Vmax的意义:
①当ν=Vmax/2时,Km=[S]。因此,Km等于酶促反应速度达最大值一半时的底物浓度。
②当k-1>>k+2时,Km=k-1/k+1=Ks。因此,Km可以反映酶与底物亲和力的大小,即Km值越小,则酶与底物的亲和力越大;反之,则越小。
③Km可用于判断反应级数:当[S]<0.01Km时,ν=(Vmax/Km)[S],反应为一级反应,即反应速度与底物浓度成正比;当[S]>100Km时,ν=Vmax,反应为零级反应,即反应速度与底物浓度无关;当0.01Km<[S]<100Km时,反应处于零级反应和一级反应之间,为混合级反应。
④Km是酶的特征性常数:在一定条件下,某种酶的Km值是恒定的,因而可以通过测定不同酶(特别是一组同工酶)的Km值,来判断是否为不同的酶。
⑤Km可用来判断酶的最适底物:当酶有几种不同的底物存在时,Km值最小者,为该酶的最适底物。
⑥Km可用来确定酶活性测定时所需的底物浓度:当[S]=10Km时,ν=91%Vmax,为最合适的测定酶活性所需的底物浓度。
⑦Vmax可用于酶的转换数的计算:当酶的总浓度和最大速度已知时,可计算出酶的转换数,即单位时间内每个酶分子催化底物转变为产物的分子数。
⑷Km和Vmax的测定:主要采用Lineweaver-Burk双倒数作图法和Hanes作图法。
第二篇:分光光度法测定蔗糖酶的米氏常数
分光光度法测定蔗糖酶的米是常数
一.实验目的:
1. 用分光光度法测定蔗糖酶的米是常数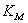 和最大反应速率
和最大反应速率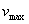 。
。
2. 了解底物浓度与酶反应速率之间的关系
3. 掌握分光光度计的使用方法
二.实验原理:
酶是由生物体内产生的具有催化活性的蛋白质。它表现出特异的催化功能,因此叫生物催化剂。酶具有高效性和高度选择性,酶催化反应一般在常温、常压下进行。
在酶催化反应中,底物浓度远远超过酶的浓度,在指定实验条件时,酶的浓度一定时,总的反应速率随底物浓度的增加而增大,直至底物过剩此时底物的浓度不再影响反应速率,反应速率最大。
Michaelis应用酶反应过程中形成中间络合物的学说,导出了米氏方程,给出了酶反应速率和底物浓度的关系:
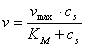
米氏常数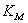 是反应速率达到最大值一半时的底物浓度。测定不同底物浓度时的酶反应速率,为了准确求得
是反应速率达到最大值一半时的底物浓度。测定不同底物浓度时的酶反应速率,为了准确求得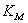 ,用双倒数作图法,可由直线方程:
,用双倒数作图法,可由直线方程:
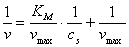
以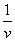 为纵坐标,
为纵坐标,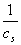 为横坐标,作图,所得直线的截距是
为横坐标,作图,所得直线的截距是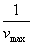 ,斜率是
,斜率是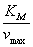 ,直线与横坐标的交点为
,直线与横坐标的交点为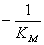 。
。
本实验用的蔗糖酶是一种水解酶,它能使蔗糖水解成葡萄糖和果糖。该反应的速率可以用单位时间内葡萄糖浓度的增加来表示,葡萄糖与3,5-二硝基水杨酸共热后被还原成棕红色的氨基化合物,在一定浓度范围内,葡萄糖的量和棕红色物质颜色深浅程度成一定比例关系,因此可以用分光光度计来测定反应在单位时间内生成葡萄糖的量,从而计算出反应速率。所以测量不同底物(蔗糖)浓度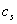 的相应反应速率
的相应反应速率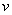 ,就可用作图法计算出米氏常数
,就可用作图法计算出米氏常数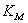 值。
值。
三.仪器与试剂:
高速离心机一台;分光光度计一台;恒温水浴一套;比色管(25ml)9支;称液管(1ml)10支;称液管(2ml)4支;试管(10ml)10支;3,5-二硝基水杨酸试剂(即DNS);0.1mol.dm-3醋酸缓冲溶液;蔗糖酶溶液;蔗糖(分析纯);葡萄糖(分析纯)。
四.实验步骤:
1.蔗糖酶的制取。在50ml的锥形瓶中加入鲜酵母10g,加入0.8g醋酸钠,搅拌15-20min后使块团溶化,加入1.5ml甲苯,用软木塞将瓶口塞住,摇动10min,放入37℃的恒温箱中保温60h。取出后加入1.6ml的4mol/L的醋酸和5ml水,使PH为4.5左右。混合物以每分钟3000转的离心机离心灶小时,混合物形成三层,将中层移出,注入试管中,为粗制酶液。
2.溶液的配制。
(1)0.1%葡萄糖标准液(1mg/mL):先在90℃下将葡萄糖烘1h,然后准确称取1g于100ml烧杯中,用少量蒸馏水溶解后,定量移至1000ml容量瓶中。
(2)3,5-二硝基水杨酸试剂(即DNS):6.3gDNS和262ml的 2mol/LNaOH加到酒石酸钾钠的热溶液中(182g酒石酸钾钠溶于500ml水中),再加5g重蒸酚和5g亚硫酸钠,微热搅拌溶解,冷却后加蒸馏水定容到1000ml,贮于棕色瓶中备用。
(3)0.1mol/L的蔗糖液:准确称取34.2g蔗糖溶解后定容至1000容量瓶中。
3.葡萄糖标准曲线的制作。在9个50ml的容量瓶中,加入不同量0.1%葡萄糖标准液及蒸馏水,得到一系列不同浓度的葡萄糖溶液。分别吸取不同浓度的葡萄糖溶液1.0ml注入9支试管内,另取一支试管加入1.0ml蒸馏水,然后在每支试管中加入1.5mlDNS试剂,混合均匀,在沸水浴中加热5min后,取出以冷水冷却,每支内注入蒸馏水2.5ml,摇匀。在分光光度计上用540nm波长测定其吸光度。由测定结果作出标准曲线。
4.蔗糖酶米氏常数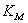 的测定。在9支试管中分别加入0.1mol/L蔗糖液、醋酸缓冲溶液,总体积达2ml,于35℃水浴中预热,另取预先制备的酶液在35℃水浴中保温10min,依次向试管中加入稀释过的酶液各2.0ml,准确作用5min后,按次序加入0.5ml 2mol/L的NaOH溶液,摇匀,令酶反应中停止,测定时,从每支试管中吸取0.5ml酶反应液加入装有1.5mlDNS试剂的25ml比色管中,加入蒸馏水,在沸水中加热5min后冷却,用蒸馏水稀至刻度,摇匀,540nm波长测定其吸光度。
的测定。在9支试管中分别加入0.1mol/L蔗糖液、醋酸缓冲溶液,总体积达2ml,于35℃水浴中预热,另取预先制备的酶液在35℃水浴中保温10min,依次向试管中加入稀释过的酶液各2.0ml,准确作用5min后,按次序加入0.5ml 2mol/L的NaOH溶液,摇匀,令酶反应中停止,测定时,从每支试管中吸取0.5ml酶反应液加入装有1.5mlDNS试剂的25ml比色管中,加入蒸馏水,在沸水中加热5min后冷却,用蒸馏水稀至刻度,摇匀,540nm波长测定其吸光度。

实验所需仪器设备
五.数据处理:
由各反应液测得的吸光度值,在葡萄糖标准曲线上查出对应的葡萄糖浓度,结合反应时间计算其反应速率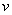 ,并将对应的底物(蔗糖)浓度
,并将对应的底物(蔗糖)浓度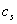 ,一并用表格形式列出,将
,一并用表格形式列出,将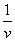 对
对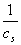 作图,以直线斜率和截距求出
作图,以直线斜率和截距求出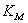 和
和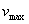 。
。
六.思考题
1.为什么测定酶的米氏常数要采用初始速度法?为什么会产生过冷现象?
2.试讨论本实验对米氏常数的测定结果与底物浓度、反应温度和酸度的关系。
