ѡ��4�����¡�ˮ��Һ�еĵ���ƽ�⡷��Ԫ������
1.��һ֧50mL��ʽ�ζ�����ʢ���ᣬҺ��ǡ����amL�̶ȴ����ѹ���Һ��ȫ���ų���ʢ����Ͳ�ڣ�����Һ�����һ���ǣ� ��
A. a mL B.��50�Da��mL C. ���ڣ�50�Da��mL D. ����a mL
2.��ˮϡ��0.1mol/L��ˮʱ����Һ������ˮ�������Ӷ���С���ǣ� ��
A. B.
B.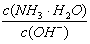 C.c(H+)��c(OH-)�ij˻� D.OH-�����ʵ���
C.c(H+)��c(OH-)�ij˻� D.OH-�����ʵ���
3.ijѧ����ʵ�鱨�����г������������к������ǣ� ��
A.��10mL��Ͳ��ȡ7.13mLϡ���� B.��������ƽ����25.20g NaCl
C.�ù㷺pH��ֽ���ij��Һ��pHΪ2.3
D.��25mL�ζ������к͵ζ�ʱ����ȥijŨ�ȵļ���Һ21.70mL
4.������Һ�������ɺ����������ʹ�����ǣ� ��
A.AlCl3 B.KHCO3 C.Fe2(SO4)3 D.NH4HCO3
5.��pH������9��NaOH��CH3COONa������Һ�У�����ˮ���������OH- ����Ũ�ȷֱ�ΪAmol/L��Bmol/L����A��B��ϵΪ�� ��
A. A>B B. A=10��4 B C. B=10��4 A D. A=B
6.һ��������������������۷�Ӧʱ��Ϊ�˼�����Ӧ�ٶȣ��Ҳ�Ӱ���������������������������м��������ģ� ��
��NaOH���� ��H2O ��NH4Cl���� ��CH3COONa����
��NaNO3���� ��KCl��Һ
A.�ڢܢ� B.�٢� C.�ڢۢ� D.�ڢܢݢ�
7.1���pH��2.5��������10���ijһԪǿ����Һǡ����ȫ��Ӧ����ü���Һ��pH���ڣ� ��
A. 9.0 B. 9.5 C. 10.5 D. 11.5
8.�������ʵ���NaOH����Һ�ֱ���pHΪ2��3��CH3COOH��Һ�кͣ�������CH3COOH��Һ���������Ϊ �������ߵĹ�ϵ��ȷ���ǣ� ��
�������ߵĹ�ϵ��ȷ���ǣ� ��
A.  B.
B. 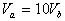 C.
C.  D.
D. 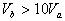
9.��pH��3������Һ��pH��11�ļ���Һ�������Ϻ���Һ�����ԣ���ԭ������ǣ� ��
A.������һ��ǿ�������� B.������Һ��ǿ����Һ��Ӧ
C.ǿ����Һ��������Һ��Ӧ D.һԪǿ����Һ��һԪǿ����Һ��Ӧ
10.������Һ��һ�������Ե��ǣ� ��
A. c(H+)��1×10-7mol/L����Һ B. pH��pOH ����Һ
C. pH��14��pOH ����Һ
D. �ɵ�����������ʵ���Ũ�ȵ�һԪ�������������Һ��Ϻ����γɵ���Һ
11������˵���в���ȷ���� �� ��
A��Kspֻ�����ܵ���ʱ��������ʺ��¶��й�
B����һ���¶��£���AgCl������Һ�м�������ʱ��Kspֵ���
C����һ���¶��µ�AgCl������Һ�У�C��Ag+����C��Cl�����ij˻���һ������
D������Ksp��FeS����Ksp��CuS��������FeS������һ�������¿���ת��ΪCuS����
12�������йصζ�������˳����ȷ���ǣ��� �����ñ���Һ��ϴ�ζ��ܣ� �����ζ�����ע�����Һ�� �����ζ����Ƿ�©ˮ�� ���ζ��� ��ϴ��
A���ۢݢ٢ڢ� B���ݢ٢ڢۢ� C���ݢڢۢ٢� D���ڢ٢ۢݢ�
13.�����ᣨHCN��������������,����֤������������ʵ��ǣ� ��
A. 1mol/L������Һ��pHԼΪ3 B. HCN������ˮ
C. 10 mL1mol/LHCNǡ����10 mL 1mol/L NaOH��Һ��ȫ��Ӧ
D. ����ͬ�����£�HCN��Һ�ĵ����Ա�ǿ����Һ����
14����20mL0��1mol·L��HCl��Һ�м���ͬ�����ͬ���ʵ���Ũ�ȵ�NH3·H2O��Һ����Ӧ����Һ�и�����Ũ�ȵĹ�ϵ������ǣ� ��
A��C��H������C��NH4������C��OH������C��Cl����
B��C��H����= C��OH����+ C��NH 3·H2O��
C��C��Cl-����C��NH4+����C��OH������C��H����
D��C��Cl-����C��NH4+��+ C��NH 3·H2O��
15.��40��ı���ʯ��ˮ��ȴ��10�棻���������CaO�����¶��Ա���40�棬������������¾�δ�ı���ǣ� ��
A.Ca(OH)2���ܽ�ȡ��ܼ������� B.��Һ�����ʵ���������
C.��Һ��������ˮ�ĵ���ƽ�� D.��Һ��Ca2+����Ŀ
16.��pH��11 NaOH��Һ��pH��3�ļ�����Һ�Ե������Ϻ�������Һ�������ж�һ����ȷ���ǣ� ��A��c(HCOO��)�� c(Na+) B��c(HCOO��)�� c(Na+)
C��c(OH������ c(HCOO���� D��c(OH������ c(HCOO����
17��������������ˮ���������c(H+)H2O=10��12mol/ L����Һ����һ���ܴ��������������������������A��NH4����Ba2����Cl����NO3�� B��Na����K����SO42����NO3��
C��Fe3����Cu2����SO42����Cl�� D��Mg2+��K����ClO����I��
18��25��ʱ����֪��Ksp(AgCl ) =1.8×10��10��Ksp(AgI) ��1.0×10��16�����й��ڲ�����֮��ת����˵���д������ ���������� A��AgCl������ˮ��������ת��ΪAgI
B��AgI��AgCl��������ˮ������AgCl����ת��ΪAgI
C�����ֲ������Ksp���Խ�������Խ����ת��Ϊ�����ܵIJ����� D��25��ʱ��AgCl��Ҫ��KI��Һ��ת��ΪAgI����C��KI��������×10��11 mol/L
19�����ñ�������Һ�ζ���������������Һʱ�����в����л�ʹ�ⶨ���ƫ�͵ģ�������
A������ʽ�ζ��ܵ����յ�ʱ�����ӵζ��ܶ���
B������Һ������ƿ����10 ml����ˮ�ٵζ�
C����ʽ�ζ���������ˮ��ϴ��δ�ñ�������Һ��ϴ
D����ʽ�ζ���ע����Һʱ�����촦�������ݣ���ζ��յ�ʱ������ʧ
20�������£�pH��ͬ�����ͬ�Ĵ��������������Һ�ֱ��ȡ���д�ʩ���й�������ȷ���ǣ�����A. ��ˮϡ��2��������Һ��pH����С
B. ʹ�¶ȶ�����20�������Һ��pH������
C. �������Ĵ����ƾ��������Һ��pH������
D. ��������п��ַ�Ӧ��������������������
21����1��Al2(SO4)3��ˮ��Һ�� �����������������������������ԣ�����ʱ��pH 7������>������=������<������ԭ���ǣ������ӷ���ʽ��ʾ���� ��ʵ����������Fe2(SO4)3����Һʱ������Fe2(SO4)3���������ڽ�Ũ�� �У�Ȼ����������ˮϡ�͵������Ũ�ȣ��� �������ٽ�����������������ˮ�⡣
��2���������أ�K2S����Һʱ��Ϊ�˷�ֹ����ˮ�⣬���Լ��������� ��
22����1��������������ʵ���Ũ�ȵĴ��������������Һ��Ϻ���Һ�� ��������������������������������������Һ��c(Na��) c(CH3COO��)������ >�� ������������<�� ����
��2��pH��3�Ĵ����pH��11������������Һ�������Ϻ���Һ�� ����������������������������������������Һ��c(Na��) c(CH3COO��) ������ >�� ������������<�� ����
��3�����ʵ���Ũ����ͬ�Ĵ��������������Һ��Ϻ���Һ�д�������Ӻ�������Ũ����ȣ����Ϻ���Һ�� ��������������������������������������������� ����������Һ����������� >�� ������������<�� ����
23.�ñ���NaOH�ζ�δ֪Ũ�ȵ����ᣬѡ�÷�̪Ϊָʾ������ɲⶨ���ƫ�ߵ�ԭ������� �� A. ���Ʊ���Һ�����������л���Na2CO3����
B. �ζ��յ����ʱ�����ӵζ��ܵĿ̶ȣ�������������ȷ
C. ʢװδ֪Һ����ƿ������ˮϴ����δ�ô���Һ��ϴ
D. �ζ����յ����ʱ���ֵζ��ܼ��촦����һ����Һ
E. δ�ñ�Һ��ϴ��ʽ�ζ���
24��0.1mol/Lij��Һ��pHֵΪ5.1������Һ�е����ʿ����� (������ )
A���Ȼ��� B��BaCl2 C���Ȼ�� D����������
25������֪:������ˮ������ˮ�д����ܽ�ƽ�⣬�����Ȼ�����ˮ�е��ܽ�ƽ��Ϊ�� AgCl��s�� Ag+(aq) + Cl��(aq)����һ���¶�����ˮ��Һ��������(Ag+)��������(Cl-)�����ʵ���Ũ�ȵij˻�Ϊһ����������Ksp��ʾ��Ksp = [Ag+]·[Cl-] = 1.8 × 10-10���ְ������Ȼ�������ֱ���룺��50mL 0.1mol·L-1��������Һ�У���50mL0.1 mol·L-1���Ȼ�����Һ�У�
Ag+(aq) + Cl��(aq)����һ���¶�����ˮ��Һ��������(Ag+)��������(Cl-)�����ʵ���Ũ�ȵij˻�Ϊһ����������Ksp��ʾ��Ksp = [Ag+]·[Cl-] = 1.8 × 10-10���ְ������Ȼ�������ֱ���룺��50mL 0.1mol·L-1��������Һ�У���50mL0.1 mol·L-1���Ȼ�����Һ�У�
��50mL 0.1 mol·L-l���Ȼ�����Һ�У���50mL����ˮ�С�
��ֽ��������ͬ�¶��£�������Ũ��������(����Żش�) ��������Ũ����С����(����Żش�) ����0��1mol·L-l�Ȼ�����Һ�У������ӵ�Ũ�����ɴﵽ mol·L-1��
26����Na2S��Һ��c(Na+)��c(S2-)�ı�ֵ����( )
A ��2 B�� ��2 C������2 D��1��2
27���ʵ���Ũ����ͬ�����и���Һ����ˮ�������������Ũ���ɴ�С��˳���� ��
��NaHSO4 �� NaHCO3 �� Na2CO3 �� Na2SO4
A �ܢۢڢ� B �٢ڢۢ� C �ۢڢܢ� D �ۢܢڢ�
28������˵���д�����ǡ� (������ )��Na2S��Һ�е����̪��Һ���ʺ�ɫ��
����B�������¶���ʹFeCl3��Һ�е�H+Ũ������
C��һ�м��Ρ����Ρ������ζ�������ˮ�� D������������ˮ�ܷ���ˮ��
29����ͬ�¶��£���ͬ���ʵ���Ũ�ȵ�������Һ����CH3COONa����NaHSO4����NaCl���� ����pHֵ�ɴ�С˳��������ȷ���� (������ )
����pHֵ�ɴ�С˳��������ȷ���� (������ )
A���ܢ٢ۢ� B���٢ܢۢ� C���٢ڢۢ� D���ܢۢڢ�
30����ʹ0.1mol/LCH3COONa��Һ��pHֵ����ķ����ǡ��� (������ )
A����ˮ B�������� C������ D���Ӵ����ƾ���
31����NaHCO3��Ϊ���ͷ�ʹ��ʱ����������������������������Ϊ (������ )
A������������� B���������ر�̼�����Ƹ��ֽ�
C���������ȷֽ�ų����� D��������ˮ�������������
32�������м��ȵĴ����Ʊ�����Һ���ȣ���Һ����ɫ�ǡ� (������ )
A����ɫ���� B����ɫ���ɫ C����ɫ���ɫ D����ɫ����
33������NH4Cl��NH3·H2O��ɵĻ����Һ������pH=7�������Һ��c��NH4+��___c��Cl-��;
��pH��7�������Һ��c��NH4+��______c��Cl-����(�����������������=��).
34���Ƚ�������Һ��pH (�����������������=����
(1)0.1mol/LNH4Cl��Һ______0.01mo1/L NH4Cl��Һ��
(2)0.1mol/LNa2CO3��Һ______0.1mol/L NaHCO3��Һ��
(3)25�桢1mol/LFeCl3��Һ_____80�桢1mol/LFeCl3��Һ��
(4)0.1mol/L(NH4)2CO3��Һ______0.1mol/L Na2CO3��Һ��
35��25��ʱ��pH=12.0��KOH��Һ�У���ˮ������ģ�OH-��=_________mol/L��
pH=12.0��KCN��Һ�У���ˮ��������ģ�OH-��________mol/L��
36��������Mg(OH)2����Һ�м��������ı���NH4Cl��Һ�����������ȫ�ܽ⡣�Դ˼ס�����ͬѧ���������Լ��Ľ��ͣ�����Mg(OH)2(s)  Mg2++2OH�� ��NH4++H2O
Mg2++2OH�� ��NH4++H2O NH3·H2O+H+����
NH3·H2O+H+����
H++OH-=H2O ����������Ӧ�ķ�����ʹƽ����������Mg(OH)2�ܽ⡣
����Mg(OH)2(s)  Mg2++2OH�� �� NH4++ OH-
Mg2++2OH�� �� NH4++ OH- NH3·H2O ��
NH3·H2O ��
���ڢڷ�Ӧ�ķ�����ʹƽ������ƣ������ܽ⡣
��1����ͬѧ���ܿ϶���λͬѧ�Ľ��ͺ����������������һ���Լ������˸�ʵ�飬֤���ס��ҵĽ���ֻ��һ����ȷ�����õ��Լ��� ��
A��NH4NO3 B��CH3COONH4 C��(NH4)2SO4 D����ˮ
��2����ͬѧ����ѡ�Լ�����Mg(OH)2����Һ�У�Mg(OH)2�ܽ⣻�ɴ���֪��������λͬѧ�Ľ�������___________����ס����ҡ��������NH4Cl������ҺʹMg(OH)2�����ܽ�����ӷ���ʽ_________________��
��7�������Ȼ�����Һ�����ֻ���������ԭ����___________________________��
��β����ȿɵõ�����Һ���ֲ�������������_________________ ___ ��
��8����1 mol·L��1 Na2CO3��Һ�У���ʹCO32-��Ũ�Ⱦ����ӽ�1mol·L��1����Ӧ����Һ�м���������_______��_________ԭ���� ��
��9��ijͬѧ��ʹ���Ȼ�����Һ��������Һ��ȡ�������壬����Ϊ����Ŀ���ܴﵽ�� Ϊʲô�������ӷ���ʽ��ʾ ���������ȡ�������壬�㽫���ʲô���������û�ѧ����ʽ��ʾ��
��������һ�������£�x A��y B z C�ķ�Ӧ�ﵽƽ�⡣
z C�ķ�Ӧ�ﵽƽ�⡣
��1����֪A��B��C�������壬�ڼ�ѹ��ƽ�����淴Ӧ�����ƶ�����x��y��z֮��Ĺ�ϵ��____ ��2����֪C�����壬��x ��y ��z��������ѹǿʱ�����ƽ�ⷢ���ƶ�����ƽ��һ����______ ____�ƶ�����3����֪B��C�����壬�������������䣬����A�����ʵ���ʱ��ƽ�ⲻ�����ƶ�����A��_____________̬���ʡ�
��4�������Ⱥ�C�������������٣�������Ӧ��_________���������������������� ����Ӧ��
�ڶ�ƪ����ˮ��Һ�еĵ���ƽ�⡷����(���˽̰�ѡ��4)
ѡ��4�����¡�ˮ��Һ�еĵ���ƽ�⡷��Ԫ������
�����õ������ԭ��������H 1 C 12 N 14 O 16 Na 23 Al 27 S 32 Cl 35.5
��һ���� ѡ����(��90��)
һ��ѡ����(�������10С�⣬ÿС��4�֣���40�֡�ÿС��ֻ��һ��ѡ���������)
1. ��һ֧50mL��ʽ�ζ�����ʢ���ᣬҺ��ǡ����amL�̶ȴ����ѹ���Һ��ȫ���ų���ʢ����Ͳ�ڣ�����Һ�����һ����
A. a mL B.��50�Da��mL
C. ���ڣ�50�Da��mL D. ����a mL
2. ��ˮϡ��0.1mol/L��ˮʱ����Һ������ˮ�������Ӷ���С���� c(NH3?H2O)c(OH?)A. B. ?c(NH3?H2O)c(OH)
C.c(H+)��c(OH-)�ij˻� D.OH-�����ʵ���
3. ijѧ����ʵ�鱨�����г������������к�������
A.��10mL��Ͳ��ȡ7.13mLϡ����
B.��������ƽ����25.20g NaCl
C.�ù㷺pH��ֽ���ij��Һ��pHΪ2.3
D.��25mL�ζ������к͵ζ�ʱ����ȥijŨ�ȵļ���Һ21.70mL
4. ������Һ�������ɺ����������ʹ������
A.AlCl3 B.KHCO3 C.Fe2(SO4)3 D.NH4HCO3
5. ��pH������9��NaOH��CH3COONa������Һ�У�����ˮ���������OH- ����Ũ�ȷֱ�ΪAmol/L��Bmol/L����A��B��ϵΪ
A. A>B B. A=104 B C. B=104 A D. A=B ����
6. һ��������������������۷�Ӧʱ��Ϊ�˼�����Ӧ�ٶȣ��Ҳ�Ӱ���������������������������м���������
��NaOH���� ��H2O ��NH4Cl���� ��CH3COONa���� ��NaNO3���� ��KCl��Һ
A.�ڢܢ� B.�٢� C.�ڢۢ� D.�ڢܢݢ�
7. 1���pH��2.5��������10���ijһԪǿ����Һǡ����ȫ��Ӧ����ü���Һ��pH����
A. 9.0 B. 9.5 C. 10.5 D. 11.5
8. �������ʵ���NaOH����Һ�ֱ���pHΪ2��3��CH3COOH��Һ�кͣ�������CH3COOH��Һ���������ΪVa��Vb�������ߵĹ�ϵ��ȷ����
A. Va?10Vb B. Va?10Vb
C. Vb?10Va D. Vb?10Va
9. ��pH��3������Һ��pH��11�ļ���Һ�������Ϻ���Һ�����ԣ���ԭ�������
A.������һ��ǿ�������� B.������Һ��ǿ����Һ��Ӧ
C.ǿ����Һ��������Һ��Ӧ D.һԪǿ����Һ��һԪǿ����Һ��Ӧ
10. ������Һ��һ�������Ե���
A. c(H+)��1��10-7mol/L����Һ
B. pH��pOH ����Һ
C. pH��14��pOH ����Һ
D. �ɵ�����������ʵ���Ũ�ȵ�һԪ�������������Һ��Ϻ����γɵ���Һ
����ѡ���⣨�������10С�⣬ÿС��5�֣���50�֣�ÿС����һ��������ѡ��������⣩
11. 25��ʱ����ij���ʵ���Һ�У���ˮ�������c(H+)��1��10a mol/L������˵������ȷ���� ��
A��a��7ʱ��ˮ�ĵ����ܵ����� B��a��7ʱ��ˮ�ĵ����ܵ�����
C��a��7ʱ����Һ��pHһ��Ϊa D��a��7ʱ����Һ��pHһ��Ϊ14��a
12. �������ӷ���ʽ����ȷ����
A. ����������Һ���չ����Ķ�����̼ OH��CO2 �� HCO3
B. �����������Һ����������������Һ��Ӧ HSO3�� OH�� SO32�� H2O ����������
C. ����ͨ����ˮ�� Cl2 ��H2O �� Cl ��ClO ��2H+ ����
D. ̼��þ����Һ�мӴ��� CO32��2CH3COOH �� 2CH3COO��CO2����H2O ����
13. �����ᣨHCN��������������,����֤������������ʵ���
A. 1mol/L������Һ��pHԼΪ3
B. HCN������ˮ
C. 10 mL1mol/LHCNǡ����10 mL 1mol/L NaOH��Һ��ȫ��Ӧ
D. ����ͬ�����£�HCN��Һ�ĵ����Ա�ǿ����Һ����
14. ��֪��NH4Cl��Һ��Ũ��С��0.1mol/Lʱ����pH��5.1������0.1mol/L������ζ�10mL0.05mol/L�İ�ˮ���ü�����ָʾ���ﵽ�յ�ʱ�����������Ӧ��
A.10mL B.5mL C.����5mL D.��5mL
15. ��40��ı���ʯ��ˮ��ȴ��10�棻���������CaO�����¶��Ա���40�棬�������������
��δ�ı����
A.Ca(OH)2���ܽ�ȡ��ܼ������� B.��Һ�����ʵ���������
C.��Һ��������ˮ�ĵ���ƽ�� D.��Һ��Ca2+����Ŀ
16. ��pH��11 NaOH��Һ��pH��3�ļ�����Һ�Ե������Ϻ�������Һ�������ж�һ��
��ȷ����
A��c(HCOO)�� c(Na+) B��c(HCOO)�� c(Na+) ����
C��c(OH���� c(HCOO�� D��c(OH���� c(HCOO��
c(OH?)17. �����£�0.1 mol/LijһԪ�ᣨHA����Һ��=1��10-8������������ȷ���� ?c(H)��������
A����Һ��ˮ�������c(H+)��10-10 mol/L
B����Һ��c(H+)��c(A-)��0.1 mol/L
C����Һ�м���һ����CH3COONa������ˮϡ�ͣ���Һ��c(OH-)������
D����0.05mol/L NaOH��Һ�������Ϻ�������Һ������Ũ�ȴ�С��ϵΪ
c(A-)��c(Na+)��c(OH-)��c(H+)
18��ij�¶��£�0.1 mol��L������Һ��pH��3�������¶���0.2 mol��L������Һ��0.2mol��L
��������Һ�������Ϻ��Һ��pH��4.7������˵����ȷ����
A.���¶��£�0.0l mol��L������Һ��pH��4
B.���¶��£���0.1 mol/L�����0.01 mol/L����ֱ���ȫ�к͵����0.1 mol/L��NaOH��Һ������������������Ϊ1��10
C.���¶��£�0.2 mol��L������Һ��0.4 mol��L��������Һ�������Ϻ��Һ��pH��4.7
D.���¶��£�0.2 mol��L������Һ��0.4 mol��L��������Һ�������Ϻ��Һ��pH=4.7
19. ������pH��3�Ķ�Ԫ����H2R��Һ��a L pH��11��NaOH��Һ��Ϻ��Һ��pH�պ�
����7�����跴Ӧǰ��������䣩����Է�Ӧ����Һ��������ȷ����
A. c(R2)+ c(OH)��c(Na)+c(H) B��c(R2)��c(Na)��c(H)��c(OH) ����������������
C. 2c(R2)+ c(HR)��c(Na) D. ��Ϻ���Һ�����Ϊ2a L ������
20�������£�pH��ͬ�����ͬ�Ĵ��������������Һ�ֱ��ȡ���д�ʩ���й�������ȷ����
A. ��ˮϡ��2��������Һ��pH����С
B. ʹ�¶ȶ�����20�������Һ��pH������
C. �������Ĵ����ƾ��������Һ��pH������
D. ��������п��ַ�Ӧ��������������������
�ڶ����� ��ѡ����(��60��)
����(�������3С�⣬��34��)
21.��16��)
��1��AgNO3��ˮ��Һ�� ����ᡱ�����С���������ԣ�����ʱ��pH 7���>������=������<������ԭ���ǣ������ӷ���ʽ��ʾ���� ��ʵ����������AgNO3����Һʱ������AgNO3���������ڽ�Ũ�������У�Ȼ����������ˮϡ�͵������Ũ�ȣ��� ����ٽ����������ơ�����ˮ�⡣
��2���Ȼ���ˮ��Һ�� �� ��ԭ���ǣ������ӷ���ʽ��ʾ����
_____________________________ ��
��AlCl3��Һ���ɣ����գ����õ�����Ҫ��������� ��
��3��������������Һʱ��Ϊ�˷�ֹ����ˮ�⣬���Լ��������� ��
22����12�֣�
��1��������������ʵ���Ũ�ȵĴ��������������Һ��Ϻ���Һ�� ������ԡ��������ԡ����ԡ�����ͬ������Һ��c(Na) (CH3COO)��� >�� ������<�� ����
��2��pH��3�Ĵ����pH��11������������Һ�������Ϻ���Һ�� ��
��Һ��c(Na) (CH3COO)
��3�����ʵ���Ũ����ͬ�Ĵ��������������Һ��Ϻ���Һ�д�������Ӻ�������Ũ����ȣ����Ϻ���Һ�� ��������� ����������Һ�����
��4����m mol/L�Ĵ����n mol/L������������Һ�������Ϻ���Һ��pH��7���������Һ��c(Hc(OH)��m��n�Ĵ�С��ϵ�ǣ��
23.��6��)�ñ���NaOH�ζ�δ֪Ũ�ȵ����ᣬѡ�÷�̪Ϊָʾ������ɲⶨ���ƫ�ߵ�ԭ
������� ��
A. ���Ʊ���Һ�����������л���Na2CO3����
B. �ζ��յ����ʱ�����ӵζ��ܵĿ̶ȣ�������������ȷ
C. ʢװδ֪Һ����ƿ������ˮϴ����δ�ô���Һ��ϴ
D. �ζ����յ����ʱ���ֵζ��ܼ��촦����һ����Һ
E. δ�ñ�Һ��ϴ��ʽ�ζ���
�ġ����������2С�⣬��26�֣�
24����8�֣�ˮ�ĵ���ƽ����������ͼ��ʾ����
��1������A���ʾ25��ʱˮ�ڵ���ƽ��ʱ������Ũ�ȣ� ��
�¶�����100��ʱ��ˮ�ĵ���ƽ��״̬��B�㣬���ʱˮ��
���ӻ��� ���ӵ� ��
��2���������µ�pH=8��Ba��OH��2��Һ�볣���µ�pH=5
��ϡ�����ϣ�������100��ĺ��£���ʹ�����ҺpH=7����Ba(OH)2������������Ϊ ��
��3����֪AnB�������ӻ�����c(A����������������)��n����c(Bn)�ݪ���ʽ��c(A��������)n��c(Bn)��ʾ���ӵ����
�ʵ���Ũ�ȡ���ij�¶��£�Ca(OH)2���ܽ��Ϊ0.74 g���䱥����Һ�ܶ���Ϊ1 g/mL�������ӻ�Ϊ ��
25����18�֣�
��1����25�������½�pH=11�İ�ˮϡ��100������Һ��pHΪ������ţ�__ __��
A��9 B��13 C��11��13֮�� D��9��11֮��
��2��25��ʱ����0.1mol/L�İ�ˮ�м��������Ȼ�粒��壬�������ܽ�����ҺpH��С����Ҫԭ���ǣ�����ţ�__ ___��
A����ˮ���Ȼ�立�����ѧ��Ӧ
B���Ȼ����Һˮ�������ԣ�������c(H+)
C���Ȼ������ˮ���������������ӣ������˰�ˮ�ĵ��룬ʹc(OH�D)��С
��3�������£������0.1mol NH4Cl��0.05mol NaOHȫ������ˮ���γɻ����Һ(��������ʧ)�� ��__ _��_ __�������ӵ����ʵ���֮�͵���0.1mol��
��_ __��_ __�������ӵ����ʵ���֮�ͱ�OH�D��0.05mol��
��4����֪ij��Һ��ֻ����OH��H+��NH4+��Cl�������ӣ�ijͬѧ�Ʋ����Һ�и�����Ũ�ȣ���
��С˳��������������ֹ�ϵ��
A��c(Cl)��c(NH4+)��c(H+)��c(OH) B��c(Cl)��c(NH4+)��c(OH)��c(H+) ��������
C��c(Cl)��c(H+)c(NH4+)��c(OH) D��c(NH4+)��c(Cl)��c(OH)��c(H+) ��������
������Һ��ֻ�ܽ���һ�����ʣ������ʵ������� ����������Ũ�ȴ�С˳���ϵ����ȷ���ǣ�ѡ����ţ� ��
����������ϵ��C����ȷ�ģ�����Һ�����ʵĻ�ѧʽ�� ��
��������Һ���������ȵ�ϡ����Ͱ�ˮ��϶��ɣ���ǡ�ó����ԣ�����ǰc��HCl�����>������<������=������ͬ�� c��NH3��H2O������Ϻ���Һ��c��NH4+����c��Cl���Ĺ�ϵc��NH4+�� ��
c��Cl����
��
ѡ��4�����¡�ˮ��Һ�еĵ���ƽ�⡷��Ԫ�������

�ڶ����� ��ѡ����(��60��)
����(�������3С�⣬��34��) 21����16�֣���ÿ��2�֣���16�֣� ��1���ᣬ�� ��Ag �� H2O ��2���ᣬAl3��3H2O
��
��

AgOH �� H ������ ��
��
��
Al(OH)3��3H�� Al2O3 ��
��3��NaOH��
22����12�֣���ÿ���3�֣��ֱ�1�֣�2�֣�
��1�����ԣ����� ��2 ��3�����ԣ����� ��4 23.��6�֣���ÿ��2�֣���ѡ12 A��D��E
�ġ����������2�֣� 24.��8�֣���ÿ��2 (1)10
��14
�� 10
��12
��2��2��9�� ��3��0.004��
25����18�֣� ��1��D��2�֣� ��2��C��2�֣�
��3����NH3?H2O��NH4+����2�֣�����Ը��֣���NH4+��H+����2�֣�����Ը��֣� ��4�� �� �Ȼ�� ��A ����2�֣�
�� NH4Cl��HCl ��2�֣� �� �� ���� ����2�֣�
2
