化学过新年——硝酸钾
 大家都有过在新年放过鞭炮的经验吗? 大家都了解鞭炮里面到底是甚么样的化学物质引发小型的爆炸吗?现在就让我们一起来揭晓吧。就是这不起眼的白色结晶-硝酸钾。这白色的结晶可不是砂糖啊,是会引起爆炸的硝酸钾唷!硝酸钾KNO3。外观为透明无色或白色粉末,无味,易溶于水,在20℃时,在水中的溶解度为31.6 g(温度越高,溶解度越大,80℃时溶解度是169g)。主要用途是制作火柴头及烟火以及黑火药、肥料、玻璃、灯蕊、腌肉,此外烟草、冶金、分析化学上亦常用之。对敏感牙齿有舒缓作用,所以有很多牙膏也含有硝酸钾。
大家都有过在新年放过鞭炮的经验吗? 大家都了解鞭炮里面到底是甚么样的化学物质引发小型的爆炸吗?现在就让我们一起来揭晓吧。就是这不起眼的白色结晶-硝酸钾。这白色的结晶可不是砂糖啊,是会引起爆炸的硝酸钾唷!硝酸钾KNO3。外观为透明无色或白色粉末,无味,易溶于水,在20℃时,在水中的溶解度为31.6 g(温度越高,溶解度越大,80℃时溶解度是169g)。主要用途是制作火柴头及烟火以及黑火药、肥料、玻璃、灯蕊、腌肉,此外烟草、冶金、分析化学上亦常用之。对敏感牙齿有舒缓作用,所以有很多牙膏也含有硝酸钾。
而爆竹又是怎么产生爆鸣声的呢?由于爆竹是中空的细管,里面充满空气,经过硝酸钾被点燃之后,内部的空气受热膨胀,会挤压爆竹的管壁,空气压力在短时间内迅速强化之后便会形成小型的爆炸压破管壁,就会听见许多霹霹啪啪的声音,这就是爆竹的来由。
 但中国历史上也有人曾经异想天开,将爆竹绑在椅子上,试图让自己藉由爆竹的喷发而升空,可惜最后不仅升空失败,还因为爆竹的爆炸而送上自己的一条小命,由此我们也可以了解在玩爆竹的当下,仍然有许多安全上的细节需要谨慎注意。例如保持适当的距离,保护好自己裸露的皮肤与双眼,这些都是过年时玩爆竹需要注意的重点。如此,我们才能在欢乐的气氛中,迎接新年的到来。
但中国历史上也有人曾经异想天开,将爆竹绑在椅子上,试图让自己藉由爆竹的喷发而升空,可惜最后不仅升空失败,还因为爆竹的爆炸而送上自己的一条小命,由此我们也可以了解在玩爆竹的当下,仍然有许多安全上的细节需要谨慎注意。例如保持适当的距离,保护好自己裸露的皮肤与双眼,这些都是过年时玩爆竹需要注意的重点。如此,我们才能在欢乐的气氛中,迎接新年的到来。
1. 化学兴趣小组设计的创新实验是“火龙生字”。在成果展示现场,某同学用硝酸钾的热饱和溶液先在白纸上书写“火”字,晾干后白纸上出现硝酸钾晶体(见图1).用带火星的木条接触硝酸钾晶体,就会观察到白纸上写过字的地方燃烧并迅速蔓延,留下“火”字的黑色痕迹(见图2).在场的同学对此产生了浓厚的兴趣,并进行了如下研究:
 【提出问题】为什么附有硝酸钾的白纸更容易燃烧?
【提出问题】为什么附有硝酸钾的白纸更容易燃烧?
【查阅资料】硝酸钾受热易分解,生成亚硝酸钾(KNO2)和一种常见的气体单质。
【猜想与假设】对于生产的是什么气体,四位同学有如下猜测:
甲:二氧化氮; 乙:氮气; 丙:氧气; 丁:氢气;
同学丙指出不可能是二氧化氮、氢气,理由是: 、
。
【进行实验】四位同学设计了实验对同学丙的猜想进行了验证,他们的操作方法是: ,观察到的现象是 ,说明同学丙的猜想正确.硝酸钾分解的化学方程式是 。
【解释与结论】白纸上写过字的地方更容易燃烧的原因是:
【反思与评价】为什么要用“硝酸钾的热饱和溶液”书写文字?
已知硝酸钾在不同温度时的溶解度如下表:
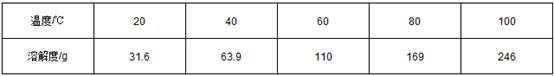
你对上述问题的解释是: 。
答案:
【猜想假设】二氧化氮不是单质 硝酸钾中不含氢元素
【进行实验】将少量硝酸钾晶体放入试管中加热,把带火星的木条深入试管中 带火星的木条复燃 2KNO3=2KNO2+O2↑
【解释与结论】硝酸钾晶体受热生成氧气,使得写过字的白纸附近氧气浓度增加
【反思与评价】硝酸钾的溶解度随温度的升高而增大,用热饱和溶液能使白纸附着较多的硝酸钾
1. 硝土中含有硝酸镁、硝酸钙、氯化钠等物质,草木灰的主要成分是碳酸钾,民间曾用硝土和草木灰作原料来制取硝酸钾。其主要生产流程如下:
硝土和草木灰(加水、搅拌、过滤 )①生成滤液和滤渣,滤液(加热蒸发、过滤)②生成热滤液和NaCI晶体,热滤液(冷却至室温、过滤)③生成KNO3晶体和滤液。如此重复使用④
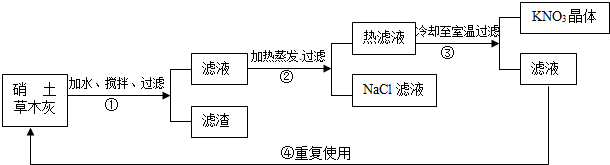
(1)写出步骤①中生成MgCO3沉淀的化学方程式:________________________________,反应类型:___________________________。
 (2)步骤④中滤液可重复使用的理由是____________________________________________
(2)步骤④中滤液可重复使用的理由是____________________________________________
_________________。
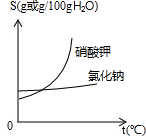
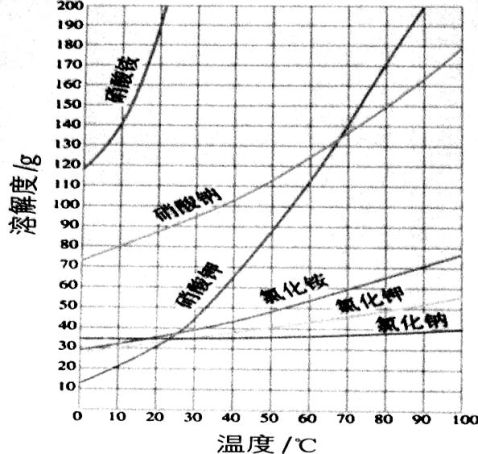
(3)参考右图,解释生产流程中用蒸发结晶得到NaCl晶体,而用冷却结晶得到KNO3晶体的原因:_____________________________________
_______________________。
(4)不同植物燃烧得到的草木灰中碳酸钾的含量不同.为测定玉米杆燃烧得到的草木灰中钾元素的质量分数,某同学称取了100g该草木灰,向其中加入足量的稀硫酸,待完全反应后,收集到6.6gCO2气体(假设草木灰中其它成分不与酸反应)。
求:①100g草木灰中K2CO3的质量.
答案:(1)由题意“硝土中含有硝酸镁、硝酸钙、氯化钠等物质,草木灰的主要成分是碳酸钾,民间曾用硝土和草木灰作原料来制取硝酸钾”则可知生成MgCO3沉淀的化学方程式Mg(NO3)2+K2CO3═MgCO3↓+2KNO3;反应符合“‘双交换,价不变’,内项结合,外项结合”,反应为复分解反应;
(2)步骤④中滤液可重复使用的理由是滤液中含有较多的KNO3;
(3)解释生产流程中用蒸发结晶得到NaCl晶体,而用冷却结晶得到KNO3晶体的原因:NaCl的溶解度受温度变化的影响较小,KNO3的溶解度受温度变化的影响较大;
(4)设碳酸钾的质量为x,其中钾元素的质量为y,.
K2CO3+H2SO4═K2SO4+H2O+CO2↑
138 44
x 6.6,x=20.7g
钾元素的质量为11.7g
钾元素在草木灰中的质量分数为11.7%
答:碳酸钾质量为20.7克,钾元素的质量分数为11.7%
故答为:(1)Mg(NO3)2+K2CO3═MgCO3↓+2KNO3,复分解反应
(2)滤液中含有较多的KNO3(或重复利用滤液中的KNO3,节约原料,提高原料的利用率)
(3)NaCl的溶解度受温度变化的影响较小,KNO3的溶解度受温度变化的影响较大.
(4)100g草木灰中碳酸钾质量为20.7克,该草木灰中钾元素的质量分数为11.7%
小军见到一种“化学爆竹”(见下图),只要用手拍打锡纸袋,掷在地上,锡纸袋随后就会突然爆开并伴随响声。他认为,这是锡纸袋中的物质发生化学反应生成气体造成的,于是想探究锡纸袋中的物质成分。

[提出问题]锡纸袋中的物质是什么?
[查阅资料]主要内容如下。
①过氧化氢分解生成氧气,化学方程式为___________________________。
②活泼金属与酸反应生成氢气,例如镁与稀硫酸反应生成氢气,化学方程式为____________________。
③含有碳酸根或碳酸氢根的盐与酸反应生成二氧化碳。
[猜想与验证]小军打开一个未用过的锡纸袋,内有一小包无色液体和一些白色固体。
(l)猜想:无色液体为酸。
验证:在两支试管中分别加入2mL水和该无色液体,各滴加3滴紫色石蕊试液。紫色石蕊试液遇水不变色,遇该无色液体变红。
实验的初步结论:无色液体为酸。 小军取两支试管进行实验的目的是__________________________。
(2)猜想:白色固体为含有碳酸根或碳酸氢根的盐。
验证:请你运用初中所学知识,帮助小军完成下列实验报告。
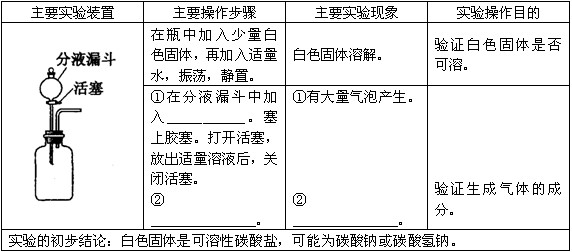 小军为进一步验证自己的初步结论,继续查找资料,得到下表。
小军为进一步验证自己的初步结论,继续查找资料,得到下表。
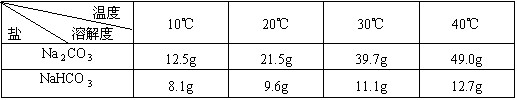
根据上表数据,该白色固体的检验方法是________________________________。
[反思]通过该探究实验,你还想学习的知识是__________________________。
[查阅资料]①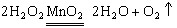
②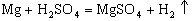
[猜想与验证](1)作空白实验:进行对比
(2)①稀盐酸
②将气体通入澄清石灰水;澄清石灰水变浑浊
方法:20℃时,在100g水中加入11g该白色固体,充分溶解后,若有白色固体剩余,为碳酸氢钠;否则为碳酸钠。
[反思]碳酸钠和碳酸氢钠化学性质上有哪些差异
烟花能够广受欢迎,流传至今,得益于它的绚烂多姿,流光溢彩以及在一瞬间爆发又一瞬间消逝带给人们的回味无穷。烟花之所以能够呈现出五颜六色,是因为在烟花的成分中,添加了特殊的元素,在燃烧过程中,这些特殊元素的火焰具有不同的颜色,在合适的控制之下,烟花就会变得五彩斑斓,令人陶醉。
烟花含有各种不同的化学药品,在燃烧时可以给火焰染色。铜燃烧时,火焰会变成绿色;硝酸锶、碳酸锶燃烧时,能使火焰变成红色;硝酸钠、草酸钠燃烧时火焰是黄色;将硝酸锶和硝酸钠按一定比例混合,燃烧时火焰是桔红色。只要把这些药品按不同的比例和次序放在烟花里,烟花在燃烧时,便能发出五彩缤纷的光。
烟花鞭炮在点燃时,发生化学反应,迅速燃烧,产生二氧化碳、一氧化碳、二氧化硫、一氧化氮、二氧化氮等气体及金属氧化物的粉尘,瞬时产生的大量气体,伴随着大量光和热,冲破炮纸的包裹,引起鞭炮的爆炸。二氧化硫和二氧化氮是酸雨的主要成分,二氧化碳会造成温室效应。新年集中燃放烟花和爆竹时,会释放的大量的有毒有害金属颗粒物,这些颗粒物的毒性来自于烟花和爆竹燃放时排放的金属元素。当它们被燃放时,颗粒物就被扩散到了更大的范围之内。“那些没有颜色的烟花可能毒性会小一些,” “但这不是大家想要的东西,人们喜欢五颜六色的烟花。” 在烟花爆竹燃放比较集中的大年三十晚上和初一早上,民众应该尽量远离燃放地点并避免户外活动,以减少有害颗粒物对个人身体健康的影响。
(烟花里装有燃烧剂、助燃剂、发光剂和发色剂。除了少部分发光剂和发色剂是直接放的金属粉末,最主要象铝粉、镁粉等,剩下的都不是直接放金属粉末的,而是放金属盐类。主要原因是多数金属单质的粉末化学性质不够稳定,一段时间后会氧化,甚至可能导致失效。
比较典型的盐类是硝酸锶(发出红光),硝酸钡(发出绿光),碳酸铜、硫酸铜(发蓝光),铝粉、镁粉(发白光),碳酸钠(发黄光)等。)
餐桌上的化学
又是一年庆新春,寒假的二十几天里,至少有一半是为了庆祝龙年春节的。
生活处处皆化学,特别是在春节期间,农历除夕、正月初一、初三、十五这几天,几乎家家户户都会以燃放烟花、爆竹的形式来传递心中的喜悦,而烟花、爆竹正是运用硫磺、硝石等易燃易爆的原理来制作的,美丽的、色彩斑斓的烟花也是加入了一些燃烧时有不同颜色的金属元素。同时在我们过大年的餐桌上也有化学知识可寻。
在一顿丰富的年夜饭上就有许多的化学细节。过春节了,家里免不了会做上一些卤菜和腌制品,其中就有关于盐的一些化学知识。亚硝酸类是一种人们普遍了解的物质,例如咸鱼产生的二甲基亚硝酸盐,在我们人体内可以转化为致癌物质二甲基亚硝酸胺,而且高盐食品是高血压、冠心病等人群的大忌,所以餐桌上卤菜、腌制品等还是少吃为好。
近几年,有些家庭会选择在饭店订一桌酒菜,而在家里不易做好的烧烤类食品是订餐中经常见到的,特别是烤羊腿和烤牛排等,这烧烤类食品中也有着很多化学知识,而且是不安全因素。如食品在烧烤前先要腌制,这会产生亚硝胺等,会影响我们的视力;在烧烤过程中,会产生苯并芘,可诱发胃癌、肠癌等。于此相差不远的油炸食品也算是餐桌上的宠儿,但煎炸过程中会产生丙烯酰胺,煎炸过焦,则会产生多环芳烃,而这类物质都是强致癌物,看来爱吃此类食品的朋友们该多注意注意啦! 餐桌上还有一样必不可少的东西——饮料,在大人们把盏品菜时,孩子们正在一杯一杯地灌着饮料呢,其中碳酸饮料最受欢迎,但每当看到饮料瓶内一个个上升的小泡泡时,我就不由想起二氧化碳和水反应后的效果,它们不正是基于此而制作出来的嘛!经科学家研究发现,饮料腐蚀牙齿,而且饮料含糖量高,是肥胖的原因之一。
新春佳节,我们在分享快乐、分享美食的同时,不要忘了多多注意我们餐桌上的化学,多多注意我们的健康。
烟花里装有燃烧剂、助燃剂、发光剂和发色剂。除了少部分发光剂和发色剂是直接放的金属粉末,最主要象铝粉、镁粉等,剩下的都不是直接放金属粉末的,而是放金属盐类。主要原因是多数金属单质的粉末化学性质不够稳定,一段时间后会氧化,甚至可能导致失效。
比较典型的盐类是硝酸锶(发出红光),硝酸钡(发出绿光),碳酸铜、硫酸铜(发蓝光),铝粉、镁粉(发白光),碳酸钠(发黄光)等。
第二篇:新高中化学苏教版选修6教案:1.3硝酸钾晶体的制备
课题3 硝酸钾晶体的制备
一 、课程标准、学科教学指导意见相关要求
学科教学指导意见对本实验的基本要求是:①理解
实验室中制取硝酸钾的原理——水溶液中利用离子相互
反应和溶解度的差异来制备无机化合物的一般原理和步
骤。②学会利用结晶或重结晶的方法提纯固态物质。③
学习减压过滤,了解热过滤.④进一步掌握并能熟练运用
溶解、过滤、加热蒸发、结晶等常用实验操作⑤加深对
制备实验的认识,初步体会科学研究的过程。
二 、实验原理
制备KNO3是利用不同物质的溶解度随温度改变
而发生不同变化的原理。在NaNO3和KCl的混合溶液
中,同时存在 Na+、K+、Cl- 和 NO3- 四种离子。升高温度,NaCl的溶解度几乎没有多大改变,而KNO3的溶解度却增大得很快。在高温下, 蒸发溶剂,达到饱和的NaCl先结晶分离。然后,冷却降温, KNO3达到饱和,析出晶体,得到粗产品。
初次结晶得到的晶体中常会混有些可溶性杂质。将所得晶体溶于少量溶剂中,然后进行蒸发(或冷却)、结晶、过滤,如此反复的操作称为重结晶。重结晶作为提纯固态物质的常用方法,在化学实验中占据着重要地位。
三、实验操作要点及主要实验现象
1. 过滤装置
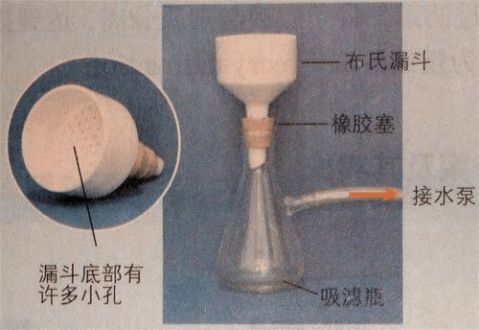
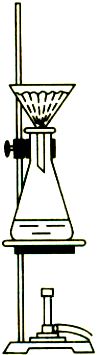
(1)减压过滤装置
抽滤也称减压过滤,是在较低压强下
将晶体析出,可以快速、充分地将晶体和
母液分离。抽滤使用特殊的漏斗——布氏
漏斗。使用时,将直径略小于漏斗内径的
圆形滤纸铺在漏斗中,先用少量溶剂润湿
滤纸并微启水泵,将其吸紧;然后小心地
将要过滤的悬浊液倒入漏斗中,开大水
泵,一直抽气到几乎没有液体滤出为止。
抽滤装置如图所示。 图3
结晶表面残留的母液,可用少量的溶剂洗涤。这时抽气应暂时停止,把少量溶剂均匀地洒在布氏漏斗内的滤饼上,以全部结晶刚好被溶剂覆盖为宜;并用玻璃棒搅松晶体,使晶体
润湿;然后抽气把溶剂抽干。热溶液和冷溶液都可选用减压过滤。若为热过滤,则过滤前应
将布氏漏斗放入烘箱(或用电吹风)预热。
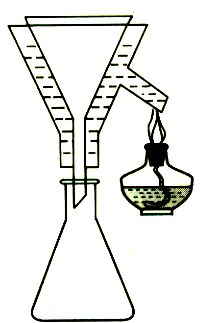
(2)热过滤装置
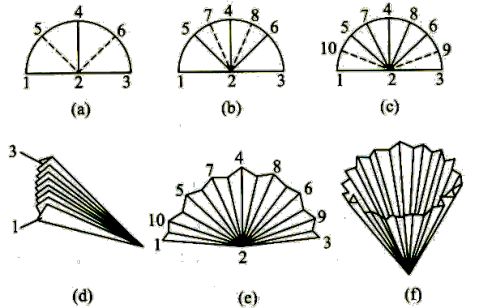
过滤热饱和溶液时,为防止溶液温度降低引起晶体析出,堵塞滤纸孔,降低产率,一般要热过滤。折叠滤纸的方法如图4。过滤少量热溶液可选一经过预热,颈短而粗的玻璃漏斗,用如图5所示装置过滤。过滤较多溶液则应选择保温漏斗,用图6所示装置过滤。热过滤时一般不要用玻璃棒引流,以免加速降温;接受滤液的容器内壁不要贴紧漏斗颈,以免滤液迅速冷却析出晶体,堵塞漏斗口。
图4 图5 图6
2. 实验操作要点
(1)制备KNO3粗品
称取20gNaNO3和17g KCl放入100mL小烧杯中,加35mLH2O(此时溶液体积约为50mL)。加热溶解后,继续加热蒸发至原溶液体积一半(建议改为约40mL)。这时烧杯中有晶体析出(NaCl晶体),趁热用热滤漏斗过滤。滤液盛于预置2mL蒸馏水(防止NaCl析出)的小烧杯中自然冷却、结晶。减压过滤,尽量抽干。称重。计算理论产量和产率。
(2)KNO3提纯
除保留少量粗产品供纯度检验外,按粗产品∶水=2∶1(质量比)的比例,将粗产品溶于蒸馏水中。加热、搅拌、待晶体全部溶解后停止加热。(若溶液沸腾时,晶体还未全部溶解,可再加极少量蒸馏水使其溶解。)待溶液冷却至室温后抽干。然后将KNO3晶体转移到表面皿上, 架于内盛沸水的烧杯上方,用水蒸气烘干,得到纯度较高的硝酸钾晶体。
(3)检验纯度:
分别取0.1g粗产品和重结晶后的KNO3晶体放入小试管中,各加2mL蒸馏水配成溶液,各加1滴稀HNO3酸化,再加2滴0.1mol/L AgNO3溶液,观察现象。
3. 实验产率:
粗产品的产率应以KNO3粗产品的干质量进行计算。由于粗产品需进行重结晶而不需干燥,可通过将压干后的产品质量扣除20%作为水的质量来估算干质量。(实验参考数据如下)
产量(粗):7.7g 产率(粗):33.5% 氯离子含量:较高
产量(精):5.1g 产率(精):22.3% 氯离子含量:微量

四、实验注意事项:
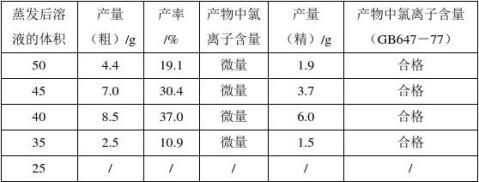
1. 水蒸发量对硝酸钾产率的影响 控制好水的蒸发量是决定产率和产品质量的主要因素,当溶液蒸发至40mL时,NaCl能最大限度的结晶析出,同时KNO3不结晶。若溶液蒸发至教材指定蒸发量,大量KNO3与NaCl一起析出,小烧杯中的溶液变成糊状固体,无法通过过滤除去NaCl。相关实验数据如下表 [摘自中学化学教学参考2007(1~2)]
1. 温度对硝酸钾产率的影响 硝酸钾冷却结晶的温度严重制约硝酸钾的产量,在气温较高的夏天,室温下冷却, 其冷却梯度较小,硝酸钾的析出量将大大减少,且冷却速度也慢。若在空气中冷却一段时间后放入冰水中冷却,产率会显著提高。
2. 过滤仪器对硝酸钾产率的影响 普通漏斗过滤时溶液会迅速冷却,在漏斗下端产生KNO3凝结,使过滤不能顺利进行且会造成KNO3损失。因此,建议采用热滤漏斗或经过预热的漏斗过滤。
3. 进行产品纯度检验时,应将粗产品和重结晶产品一起检验,进行对比观察。哪个溶液中的浑浊度浅,说明哪个溶液中的Cl较少。一次重结晶后的产物中还有少量Cl存在,甚至第二次重结晶后还能检出Cl。这主要是由于在KNO3晶体长大过程中,Na和Cl被包在晶体里,或长大过程中晶体表面不断吸附这些离子造成的,通过多次重结晶能在一定程度上除去杂质,提高产品纯度。
-
+
一
-
一
