实验七 化学反应速率、活化能的测定
实验目的
1.了解浓度、温度和催化剂对反应速率的影响。
2.练习恒温水浴操作。
实验原理
水溶液中(NH4)2S2O8 和KI的氧化还原反应为复合反应:
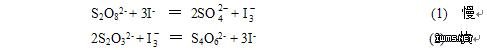
从不同浓度下测得反应速率,就可计算出该反应的反应级数m和n。
实验内容
1.浓度对反应速率影响,求反应级数(m=? 和n=?)
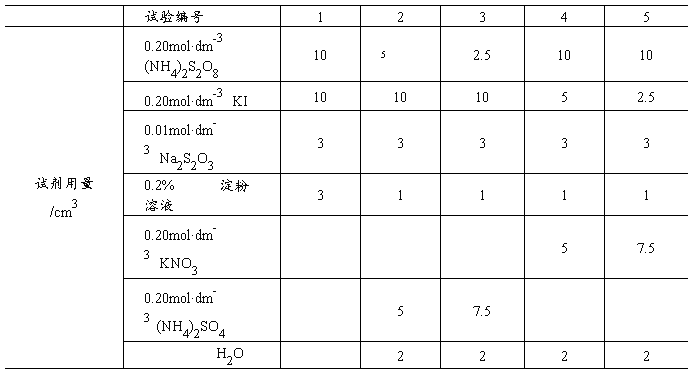
2.温度对反应速率的影响求活化能

实验纪录
1.浓度对反应速率影响,求反应级数。
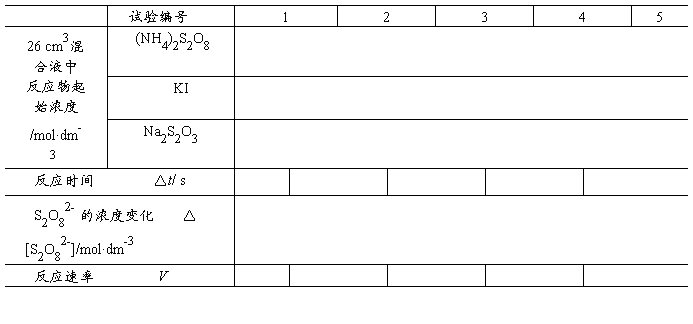
2.温度对反应速率的影响求活化能

实验思考
1.由反应方程式能否确定反应级数?为什么?试用本实验结果说明之。
2.对Na2S2O3用量过多或过少对实验结果有何影响?
3.2和3号中添加不同量的(NH4)2SO4溶液,在实验4和5中添加不同量KNO3溶液用意何在?如何选择添加试剂?
4.若不用S2O82- 而改用I- 或I3- 的浓度变化来表示反应速率,则反应速率常数k是否一样?
5.下列操作情况对反应结果有何影响?
(1)先加(NH4)2S2O8溶液,后加KI溶液。 (2)慢慢加入(NH4)2S2O8溶液。
第二篇:化学反应速率及活化能的测定







