一. 实验目的:
1. 无机化学实验是无机化学课程的重要组成部分,也是学习无机化学的一个重要环节,通过实验,使讲课中的重要理论和知识能进一步巩固、扩大和深化。
2. 掌握无机化学实验的基本操作和技能,学会正确地使用各种仪器。
3. 培养学生独立思考、分析问题、解决问题和创新能力。
4. 培养学生实事求是,严谨认真的科学态度,整洁卫生的良好习惯。为以后的学习和工作打下良好的基础。
二. 无机化学实验的考核方法:
1. 无机化学实验为单独设课。30学时, 10个实验,三次无故旷课或三次无故不交实验报告以不及格论。不及格必须重修。平时成绩占80%,两次小测验各占10%。
平时成绩有三部分组成:
①做好预习、写好预习报告:实验前要仔细阅读实验教材和教科书的有关内容。明确实验目的,弄懂实验原理,熟悉实验内容,写好预习报告。
②实验情况考察:认真操作,仔细观察并如实的记录实验现象,保证出勤严守课堂纪律。
③实验报告:实验报告是每次实验的记录概括总结,也是对实验者综合能力的考核。每位同学做完试验必须按时独立认真的完成实验报告。一份合格的实验报告要按实验室的要求去写。做到:记载清楚,现象真实,结论正确,文字简练,书写工整。
实验报告格式要求:
一.实验目的:
二.实验原理:
三.实验内容:
一.实验室规则:
1. 不迟到不旷课。要求同学们提前10分钟进实验室,刷洗本次实验所用的玻璃仪器。
2. 注意安全、保持室内卫生。
3. 节约用水、电、试剂。
4. 实验室规定了仪器破损赔偿制度。
实验一氯化钠提纯
下周实验:酸碱反应与缓冲溶液
一 实验目的:
1. 学会用化学的方法提纯粗盐。
2. 练习台秤的使用以及加热,溶解,常压过滤,减压过滤,蒸发浓缩,结晶干燥等基本操作。
3. 学习食盐中Ca2+,Mg2+ ,K+,SO42-的定性检验方法。
二. 实验原理:
粗食盐中含有泥沙等不溶性杂质及Ca2+ 、Mg2+ 、K+ 、SO42-等可溶性杂质,将粗食盐溶于水后,用过滤的方法可以除去不可溶性杂质;Ca2+ 、Mg2+ 、SO42-等离子可以用化学方法,即加沉淀剂使之转化为难溶性的沉淀物,再过滤除去,K+ 蒸发浓缩后不结晶,(NaCl溶解度是39.1,KCl溶解度是56.7)仍留在母液中。
相关离子反应方程式如下:
Ba2++SO42-= BaSO4(s)
Mg2+ +2OH- = Mg(OH)2(s)
Ca2+ +CO32-= CaCO3(s)
Ba2+ +CO32-= BaCO3(s)
三. 实验内容:
1. 粗食盐的提纯.
(1).食盐的称量和溶解:在台秤上称取4g粗食盐,放在50ml烧杯里加入20ml蒸馏水加热搅拌使食盐溶解。
台秤的使用方法:台秤上左边放重物,右边放砝码,并在秤盘上放上相等质量的纸。
酒精灯的使用方法:酒精灯里的酒精加入量不应超过容积的2/3。以免点燃受热膨胀而溢出,不能用点燃着的灯点燃另一个灯。熄灭时要用灯罩盖上,拿下再盖上,不用嘴吹灭。
(2)SO42-的除去:在煮沸(溶解度大,沉淀完全)的粗盐溶液中加入20滴1.0molL-1BaCl2溶液,待沉淀下降后,上层清水中滴加BaCl2检验沉淀是否完全,无混浊证明沉淀完全,然后在石棉网上小火加热三分钟,使沉淀颗粒长大,以便过滤。SO42-+Ba2+=BaSO4(s)
普通过滤方法:将滤纸两次对折,成扇形,滤纸边沿要低于漏斗边沿2~5mm,把滤纸润湿,赶走气泡,先将大部分溶液沿着玻璃棒慢慢地倾入漏斗中。玻璃棒要接触三层纸一边,然后在将剩下的溶液同沉淀一同倒在滤纸上,要用少量的蒸馏水冲洗烧杯内壁,将洗涤液与剩下的沉淀全部转入漏斗中。
(3)Mg2+、Ca2+、Ba2+ 等离子的除去:在滤液中加入10滴2.0mol/LNaOH和30滴1.0mol/LNa2CO3加热至沸,待沉淀下沉后,在上层清夜中加入1~2滴Na2CO3,检验沉淀是否完全,继续煮沸3分钟,然后过滤(滤液放在蒸发皿中)。
有关离子反应方程式如下:
Ba2++CO32-= BaCO3(s)
Mg2++2OH-= Mg(OH)2(s)
Ca2++CO32-= CaCO3 (s)
(4)调节溶液的PH值:在滤液中滴加HCl(1.0molL-1)直至PH=4~5为止。
为什么要调节溶液的PH值?是为了除去CO32-,中和过量的OH–
PH试纸的用法:将小片的PH试纸放在干燥并且洁净的点滴板上,用玻璃棒取少量待测溶液观察颜色的变化,与标准比色板进行对比。
(5)蒸发浓缩:在泥三角上用小火加热,将溶液蒸发至稀粥状为止,切不可将溶液蒸干,为什么不可将溶液蒸干?以上实验过程中将Mg2+、Ca2+、SO42-都已除去,唯独K+没有除,因为NaCl和KCl的化学性质比较相似,也就是说用化学方法不能除掉K+,只有用物理性质上的差异除去K+,也就是溶解度的不同,在100度时KCl的溶解度为56.7g,NaCl的溶解度为39.1g,所以NaCl结晶出来,而K+仍留在母液中通过减压过滤的方法把K+除掉。
(6)结晶、减压过滤、干燥:让浓缩液冷却至室温,用布氏漏斗放在真空泵的吸滤瓶上减压过滤(滤纸把所有的孔都盖上为准)再将结晶物转移至蒸发皿中(切不可用水冲洗滤纸上的精盐),小火干燥称其质量,计算产率。((纯/不纯)×100% =产率)。
2.产品纯度的检验:称取粗盐和提纯后的精盐各1g分别溶于5ml的蒸馏水中,然后分别盛入3支试管中,检验它们的纯度。

实验二酸碱反应与缓冲溶液
下周实验:沉淀反应 把实验里所用到的Kθsp查出来,Kθsp(PbS)==9.0×10–29
一. 实验目的:
1. 进一步理解和巩固酸碱反应的有关概念和原理(如同离子效应,盐类的水解及其影响因素)。
2. 学习试管实验的一些基本操作。
3. 学习缓冲溶液的配置及其PH的测定,了解缓冲溶液的缓冲性能。
4. 进一步熟悉酸度计的使用方法。
二. 实验原理:
1. 同离子效应:
强电解质在水中会全部解离,弱电解质在水中部分解离,在弱电解质溶液中加入与弱电解质有相同的离子的强电解质,解离平衡向生成弱电解质的方向移动,使弱电解质的解离度下降。这种现象称为同离子效应。
2. 盐的水解:
一般是指化合物与水反应而起的作用,强酸强碱盐在水中不水解,强酸弱碱盐(NH4Cl)水解溶液显酸性;强碱弱酸盐(如NaAc)水解显碱性,弱酸弱碱盐,如(NH4Ac)水解溶液的酸碱性取决于相应弱酸弱碱的相对强弱如:
AC–+H2O=HAC+OH–、 NH4–+H2O=NH3•H2O+H+ CO32–+H2O=HCO3–+H2O
水解反应是酸碱反应的逆反应。中和反应是放热反应,水解反应是吸热反应,因此升高温度有利于盐类的水解。如:[Fe(H2O)6]3+=[Fe(H2O)5 OH]2++H+
3 缓冲溶液:
由弱酸(或弱碱)与弱酸(或弱碱)盐组成的溶液,具有保持溶液PH相对稳定的性质,这类溶液称为缓冲溶液。其特点是加入少量的酸和碱使其pH值基本保持不变。
三.实验步骤:
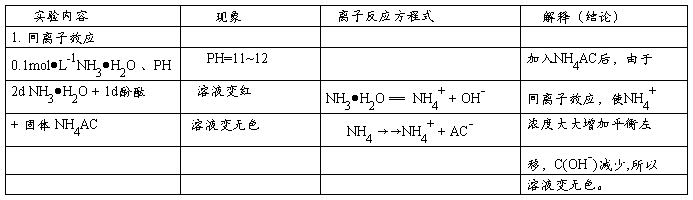
1.同离子效应
(1)用PH试纸检验0.1mol•L–1NH3•H2O的溶液的PH值为11~12
2d NH3•H2O + 1d酚酞→→溶液变红(因为0.1mol•L–1NH3•H2O的溶液的PH值为11~12,酚酞变色范围PH=8.0~10,所以加入酚酞后溶液变红色)+固体NH4AC→→溶液变无色
(由于同离子效应NH4+浓度增大,影响到了氨根离子的平衡,平衡向左移动,C(OH–)减小,所以由红色变无色)。
NH3•H2O→NH4++OH–
NH4AC→NH4+ + AC–
(2)用PH试纸检验0.1mol•L–1 HAC的溶液的PH值为2~3
2d HAC + 1d甲基橙→→溶液变红(因为0.1mol•L–1 HAC的溶液的PH值为2.88,甲基橙变色范围PH=3.1~4.4)+固体NH4AC→→溶液变黄色
(由于同离子效应AC–浓度增大,影响到了HAC得解离平衡,平衡向左移动,C(H+)减小,所以变黄色)。
HAC + H2O →H3O+ + AC–
NH4AC→NH4+ + AC–
结论:由于同离子效应,实质是浓度的因素对化学平衡的影响使其发生移动。
2.盐类的水解
(1)已知溶液0.1NaCl (PH=7)
可以观察到每一步试剂的PH值不一样为什么?因为:NaCl为强酸强碱盐不水解,所以显中性。
NaAC为强碱弱酸盐水解显碱性。
NH4Cl为强酸弱碱盐水解显酸性。
Na2CO3为强碱弱酸盐水解显碱性。
(2)2ml 水 + 3d Fe(NO3)2 →→溶液变黄 [Fe(H2O)6] 3+→[Fe(OH) (H2O)5]2+ +H+
加热条件下:2ml 水 + 3d Fe(NO3)2→→ 溶液变棕红色 [Fe(OH)3]
解释:水解反应是中和反应的逆反应,中和反应为放热反应,水解反应是吸热反应,因此温度升高有利于盐类的水解。
(3)2ml水 + 1d BiCl3→BiOCl(S)(白色↓)+ 5d HCl →→ 溶解
Bi3+ + Cl+ H2O → BiOCl(S)(白色↓)+2H+ (当温度一定时盐的浓度越小,水解程度越大,也就是说稀释可促进水解)。
Bi3+ + Cl– + H2O → BiOCl (S)+2H+ (为了防止水解可利用改变酸度的方法,使水解平衡发 生移动)。
生移动)。
(4)2d CrCl3 + 2d Na2CO3 →Cr(OH)3 (s) 灰绿色
Cr3+ + 3CO32– + 3H2O=Cr(OH)3 (s) + 3HCO3–
这是一个双水解反应。(一种水解显酸性的盐与一种水解显碱性的盐相混合时将加剧两种盐的水解)。
3.缓冲溶液:(由弱酸(或弱碱)与弱酸(或弱碱)盐组成的溶液,具有保持溶液PH相对稳定的性质,这类溶液称为缓冲溶液。其特点是加入少量的酸和碱使其PH值基本保持不变)。
编号 配制缓冲溶液 PH计算值 PH测定值
1 10ml 1.0 HAC --- 10ml 0.1NaAC 3.74
2 10ml 0.1 HAC---10ml 1.0 NaAC 5.74
3 10ml 0.1 HAC---10ml .01 NaAC 4.74
4 10ml 1.0 NH3•H2O --- 0.1 NH4Cl 10.26
往3号缓冲溶液中加10d 0.1M HCl 摇匀后测定PH=
往3号缓冲溶液中加20d 0.1NaOH 摇匀后测定PH=
PH—3C型酸度计的原理:它是用来测定溶液电动势的方法来测定溶液的pH值时要用到两个电极一个是玻璃电极,一个甘汞电极。
玻璃电极:它是用一种特殊的导电玻璃,含(72 %SiO2,22 %Na2O,6 %CaO)吹制成的空心小球,球内有0.1mol•L–1HCl和Ag—AgCl电极,玻璃电极的电极电势是随待测液的PH值不同而变化。
饱和甘汞电极:它是由金属汞,Hg2Cl2和饱和KCl溶液组成的电极,内玻璃管封接一根铂丝,铂丝插入纯汞中,纯汞下面有一层甘汞和汞的糊状物,外玻璃管中装入饱和的KCl溶液,下端用素瓷塞塞住,通过素瓷塞的毛细孔,可是内外溶液相通,甘汞电极的电极电势只与Cl–1浓度有关,当管装有饱和的KCl时,Cl–1浓度就一定了,那么E甘==0.2415V
将甘汞电极和玻璃电极同时插入被测溶液中组成原电池,有原电池就有电动势:
如果Eθ玻已知即可从电动势求出PH值,玻璃电极的电极电势随待测溶液PH值不同而变化,为此必须对玻璃电极进行标定,那么就可以用一个已知的PH值的标准缓冲溶液代替待测液而测定,(PH==6.86)酸度计上一般把测得的电极电势直接用PH值表示出来。
酸度计的使用:
1. 打开仪器开关先预热10分钟
2. 把mV---PH档调到PH档
3. 把温度补偿器调到室温
4. 把斜率调到最大
5. 把玻璃电极(—),甘汞电极(+)分别连接在仪器的正负极上
6. 用标准缓冲溶液定位
注意事项: 1. 用完标准缓冲溶液一定要放回原处,切不可倒掉。
2. 在整个测量过程中要特别爱护玻璃电极,(注意:玻璃电极要高于甘汞电极)
3. 将待测的数据让指导教师看一下,签字后方可有效。
实验三. 沉淀―溶解平衡
下周实验:氧化还原反应。 把实验里用到的 Eθ值和碘的元素电势图查出来。
一. 实验目的:
1. 加深理解沉淀—溶解平衡和溶度积的概念,掌握溶度积规则及其应用。
2. 初步学习利用沉淀法分离混合阳离子。
3. 学习离心机的使用,和固―液分离操作。
二.实验原理:
1.沉淀―溶解平衡.
在含有难溶强电解质晶体的饱和溶液中,难溶强电解质与溶液中相应离子间的多相平衡,称为沉淀―溶解平衡。用通式表示如下:
AmBn(s)==mA n+(aq) + nBm–(aq)
其溶度积常数为: Kθsp (Am Bn) ==[C(An+)/Cθ]m [C(Bm–)/C]n
沉淀的生成和溶解可以根据溶度积规则来判断:Jθ>Kθsp有↓析出.平衡向左移动。
Jθθsp无↓析出.平衡向右移动原来的沉淀溶解。
Jθ=Kθsp处于平衡状态,溶液为饱和溶液。
溶度积等于沉淀―溶解平衡时离子浓度幂的乘积。溶液PH值的改变,配合物的形成或发生氧化还原反应,往往会引起难溶电解质溶解度的改变。
对于相同类型的难溶电解质可以根据其Kθsp的相对大小判断沉淀的先后顺序。
对于不相同类型的难溶电解质则要根据计算所需沉淀试剂浓度的大小来判断沉淀的先后顺序。
两种沉淀间相互转化的难易程度要根据沉淀反应的标准平衡常数确定。
利用沉淀反应可以分离溶液中的某些离子。
三. 实验内容:
1.沉淀的生成与溶解:
(1)A管:2d Pb(AC)2 + 2d KI →→ PbI2(S) 桔黄色 + 5 ml水→→↓ 溶解。
B管:2d Pb(AC)2 + 2d KI →→ PbI2(S) 桔黄色 +NaNO3 →→↓ 溶解。
PbI2(S)=Pb2+ + 2I– Kθsp(PbI2)=8.4 ×10–9
① 解释:加入5ml水后,J< Kθsp,∴无↓ 。
C(Pb2+)=0.01 / 5.2 == 1.92×10–4 C(I-) =0.02 / 5.2 == 3.85× 10–4
J=C(Pb2)×C(I-)2 ==1.92×10–4×(3.85×10–4)=2.85×10-11
2.85×10-11<Kθsp(PbI2)=8.4×10-9 ∴↓溶解 .
②在试管中加入NaNO3固体,↓也溶解。因为盐效应
什么是盐效应:将易溶强电解质加入难溶电解溶液中,使难溶电解质的溶解度比在纯水中的溶解度大,是因为加入易溶强电解质溶液后溶液中各种离子总浓度增大了,增强了离子间的静电作用,在阳离子(Pb2+)周围有更多的阴离子,形成了离子氛。在阴离子(I-)周围有更多的阳离子也形成了离子氛,使Pb2+、I-受到较强的牵制作用,降低了它们的有效浓度,因而在单位时间内与沉淀表面碰撞次数减少,沉淀过程变慢,实际上是盐效应破坏沉淀与溶解的平衡,使沉淀溶解了。
(2) 1d Na2S + 1d Pb(NO3) →→ PbS (s) (黑色)
PbS(s)
A管:PbS(s)+2HCl=[PbI4]2-+H2S(g)+ 2H+ (PbAC 试纸检验变黑、配位溶解)
B管:PbS(s)+2NO-+8H+=3Pb2++2NO(g)+3S(s)+4H2O (氧化还原溶解)
Pb2+ + S2- == PbS (s) Kθsp ==9.0 × 10–29
(3) 5d MgCl2 + 3d NH3H2O →→ Mg(OH)2(s) (白色) Mg2+ + 2NH3•H2O == Mg(OH)2(s) + 2NH4+
A管:+2HCl →→↓溶解 Mg(OH)2(s) + 2HCl == MgCl2 + 2H2O (酸碱中和反应)
B管:+NH4Cl→→↓溶解 Mg(OH)2(s) + 2NH4+ + 2NH3•H2O (同离子效应)
2.分步沉淀:
(1)离心试管中加1d Na2S + 1d K2CrO4 (用水稀释至5ml)+1dPb(NO3)2→→PbS(s)(黑)离心分离,在向清清液中继续滴加Pb(NO3)2→→PbCro4(s)(黄色)
∵Kθsp(Pbs ) ==9.0×10–29θsp(pbCro4) ==2.8×10–13,Kθsp小的先沉淀,Kθsp大的后沉淀。
∴Pb2+ + S2–== PbS(s) (先黑) Pb2+ + CrO42–== pbCro4(s)(后黄)
沉淀的顺序同样是根据溶度积规则来判断:对于同一类型难溶电解质,Kθsp小的先沉淀、Kθsp大的后沉淀。
(2)在试管中加2d AgNO3 +1d Pb(NO3)2 + 用水稀释至5ml,在逐滴加入K2C2O4(注意:每加一滴都要充分振荡)先生成黄色PbCrO4(s),后生成A砖红色gCrO4(S)(生成不同类型的难溶电解质,离子积J首先达到溶度积的难溶电解质先析出沉淀)。
Pb2+ + CrO42 == pbCro4(s) (先黄色) 2Ag+ + CrO42–== AgCro4(S) (后砖红色 )
解:C(Ag+) == 0.1×0.1 /5.0 ==0.002 C(pb2+)== 0.1×0.05 /5.0 ==0.001
C(CrO42–) == 2.8×10–13/1×10–3 ==2.8×10–10 C(CrO42–)==1.1×10–12/(2×10–3)== 2.75×10–7
通过计算可知:对于不同类型的难溶电解质来说,所需沉淀剂浓度小得先沉淀。
3.沉淀的转化:(把一种难溶电解质转化为另一种难溶电解质,然后再使其溶解)。
6d AgNO3 +3d K2CrO4 →→Ag2CrO4(s)(砖红色)在逐滴加NaCl→→有AgCl(s)(白)
2Ag+ + CrO42–= Ag2CrO4(s) Ag2CrO4 + 2Cl–=2AgCl(s) + CrO42–
∵Kθ= (Ag2CrO4)/Kθsp(AgCl) == 1.1×10–12/(1.8×10–10)2=3.4×107>>1
∴可以由砖红色的Ag2CrO4转化为白色的AgCl↓ 。
4.沉淀法分离混合离子:
(1)某溶液中含有 Ba2+ 、 Al3+ 、 Fe3+ 、 Ag+ 等离子,试设计方法分离之。写出有关反应方程式。
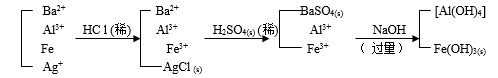
有关的离子反应方程式: Ag+ + Cl–= AgCl (s) Ba2+ + SO42– =BaSO4 (S)
Fe3+ + 3OH–=Fe(OH)3(s) Al3+ + 4OH–=[Al(OH)4]–
(2). 某溶液中含有 Ba2+ 、 Pb2+ 、 Fe3+ 、 Zn+ 等离子,自己设计方法分离之。图示分离步骤,
写出有关反应方程式。
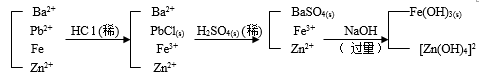
写出有关反应方程式:Pb2+ + 2Cl–=PbCl2(s) Ba2+ + SO42–=BaSO4 (S)
Fe3+ + 3OH–=Fe(OH)3(s) Zn2+ + 4OH–=[Zn(OH)4]2–
实验四. 氧化还原反应
下周实验:配合物形成时性质的改变。
一.实验目的:
1. 加深理解电极电势与氧化还原反应的关系。
2. 了解介质的酸碱性对氧化还原反应方向和产物的影响。
3. 了解反应物浓度和温度对氧化还原反应速率的影响。
4. 掌握浓度对电极电势的影响。
5. 学习使用酸度计测定原电池电动势的方法。
二.实验原理:
1. 物质的氧化还原能力的大小可以根据相应电对电极电势的大小来判断。
2. 根据电极电势的大小可以判断氧化还原反应的方向。
3. 有电极电势反应的能斯特方程式,可以看出浓度对电极电势的影响。
E = Eθ + 0.0592/2 lg C(氧化型)/C(还原性)
4. 介质的酸碱性也会影响某些氧化还原反应的产物。
5. 酸度计可以测定原电池的电动势,当沉淀或配合物形成时会引起电极电势或和电池电动势的改变。
三.实验步骤:
1.比较电对Eθ值的相对大小.:
(1)2d KI +2d FeCl3 + 4d CCl4 →→ CCl4层上有紫色的I2 2Fe3+ +2I– ==2Fe2++I2
∵Eθ Fe3+/ Fe2+ == 0.769> Eθ I2/I– ==0.5345 (所以反应可以进行)
(2)2d KBr + 2d FeCl3 + 4d CCl4→→ CCl4层上没有橙红色的Br2,Fe3+ +2Br– ≠不反应
∵Eθ Fe3+/Fe2+ == 0.769θBr2/2Br– == 1.0774(所以反应不可以进行)
由实验(1)(2)比较:EθBr2/2Br– =1.077 > EθFe3+/Fe2+=0.769 > EθI2/2I– =0.5345
结论:最强的氧化剂是 Br2单质, 最强的还原剂是 I–离子。
(3)2d KI +2d H2O2 +2d H2SO4 + 4d CCl4 →→ CCl4 层上有紫色的I2
2I– +H2O2 + 2H+ == I2 + 2H2O ∵Eθ H2O2/H2O == 1.73 > Eθ I2/I– == 0.5345
(4)1d KMnO4 +2d H2O2 +1d H2SO4 →→ 紫红色退去并有O2↑产生.
2MnO4–+5H2O2+6H+ = 2Mn2++O2(g) +8H2O EθMnO4–/ Mn2+ =1.512>Eθ O2/ H2O2 =0.6945
结论:H2O2在(3)中.遇到强还原剂它起氧化剂的作用。
H2O2在(4)中遇到强氧化剂它起还原剂的作用。
(5)1dK2Cr2O7 + 5dNa2SO3 +1d H2SO4 (2) →→ 由橙黄色变绿(Cr3+)的颜色
. Cr2O72– + 3SO32– +8 H2+= 2Cr3+ + 3SO42– +4H2O
∵Eθ Cr2O72–/Cr3+ == 1.33 > Eθ SO42–/SO32– == 0.1576 ∴反应可以进行.
(6)1d K2Cr2O7 + 5dFeSO4 +1d H2SO4 →→ 由橙黄色变绿(Cr3+)的颜色
Cr2O72– + 6 Fe2++14 H2+=2Cr3+ + 6 Fe3++7H2O
∵Eθ Cr2O72–/Cr3+ ==1.33 > EθFe3+/Fe2+ == 0.769 ∴反应可以进行.
2. 介质的酸碱性对氧化还原产物及反应方向的影响:
(1)对氧化还原产物的影响:
A孔:1d KMnO4 + 1d H2SO4 + Na2SO3 →→ 由紫色变无色、 产物:(Mn2+)
B孔:1d KMnO4 + 1d H2O + Na2SO3 →→ 由紫色变棕色 (MnO2)
C孔:1d KMnO4 +1d NaOH + Na2SO3 →→ 由紫色变绿色 (MnO42–)
酸:EθMnO4–/ Mn2+ = 1.512 > EθSO42–/SO32– =0.1576
中:EθMnO4–/ MnO2 =0.5965 > EθSO42–/SO32– =0.1576
碱:EθMnO4–/ MnO42– =0.5545 > EθSO42–/SO32– = –0.93
2MnO4– + 5SO32– + 6H+ == 2Mn2+ + 5SO42– +3H2O
2MnO4– + 3SO32– +H2O == 2MnO2(s) + 3SO42– +2OH–
2MnO4– + SO32– + 2OH– == 2MnO42– + 3SO42– +H2O
介质不同,氧化还原产物不同
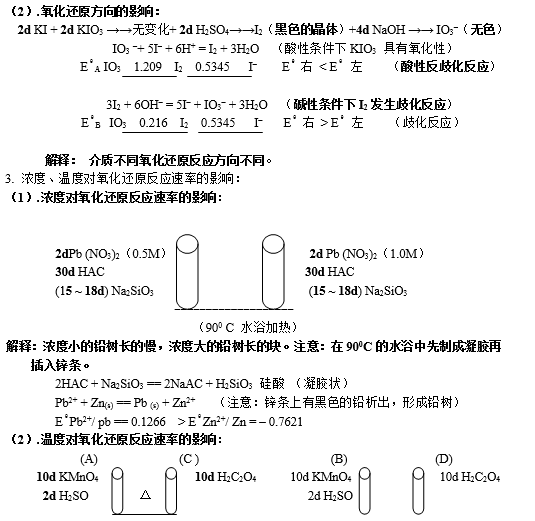
现象是C管的先褪色, 因为温度升高,反应速率加快。
2MnO4+5H2C2O4 +6H+=2Mn2++10CO2(g)+8H2O
EθCO2/ H2C2O4 =0.5950 θ MnO4–/ Mn2+ = 1.512
4. 浓度对电极电势的影响:.
(1)测定ZnSO4(1.0M)溶液中E Zn2+/ Zn 的值.
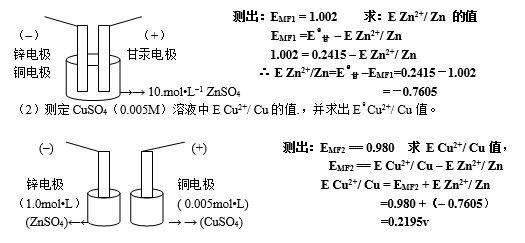
再根据能斯特方程式求: EθCu2+/ Cu(0.005) 值:E == Eθ+(0.0592/2)lgC(Cu2+) /1
= EθCu2+/ Cu + (0.0592/2)lg 0.005/1
EθCu2+/ Cu = E Cu2+/ Cu(0.005)—(-0.068)
EθCu2+/Cu =ECu2+/Cu(0.005)+0.06 =0.2195 +0.068=0.2875v
现在,我介绍一下酸度计的工作原理:酸度计是一种通过测量流液电动势的方法来测量流液的PH值,酸度计是由玻璃电极,甘贡电极仪器三部分组成,现在分别介绍玻璃电极和甘汞电极。待测流液和玻璃电极优关,甘贡电极为定值0.2415.
EMF=E甘-E玻
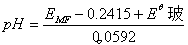
如果玻璃电极的标准电极电势已知,那么测一个流液的电动势就可以得出一个PH值,现在用已知pH=6.86的标准缓冲溶液代替待测溶液而确定Eθ玻。在仪器上用位旋钮定位,那么有一个被测流液就有一个电动势,有一个电动势就可以计算出一个pH值,仪器上可以直接用pH值表示不用再计算了。
实验五. 配合物的形成时的性质的改变
下周实验:氯、溴、碘,把实验里的所有的方程式写在预习报告里。
一. 实验目的:.
1. 了解配合物形成时几种性质的改变
2. 加深理解配合物的组成和稳定性
二. 实验原理:
1. 配位化合物与配位平衡。
配合物是由形成体(又称为中心离子或原子)与一定数目的配位体(负离子或中性分子)以配位键结合而形成的一类复杂化合物,是路易斯酸和路易斯碱的加合物。配合物的内层和外层之间以离子键结合,在水溶液中完全解离,配位个体在水溶液中分步解离,其行为类似于若电解质,在一定条件下,中心离子、配位体和配位体个体间达到配位平衡。
例如:Cu2++4NH3=[Cu(NH3)4]2+
相应反应的标准平衡常数Kθf称为配合物的稳定常数,对于相同类型的配合物, Kθf 数值愈大,配合物就愈稳定。
在水溶液中,配合物的生成反应主要有配合物配位体的取代反应和加合反应。
例如:,[Fe(SCN)n]3-n+6F–=[FeF6]3-+nSCN- , HgI2+2I–=[HgI4]2–
,配合物形成时往往伴随着溶液颜色、酸碱性(即PH)、难溶电解质溶解度、中心离子氧化还原性的改变等特征。
三. 实验步骤:
1. 配合物形成时与颜色的变化:
(1)1d FeCl3 + 1d KSCN →→ 血红色的 [Fe(NCS)]2+ + F–→→[ Fe F]2+(无色)
对于同一类型的配离子,Kθf越大,配合物越稳定
Fe3++ SCN- = [Fe(NCS)]2+ Kθf == 9.1×102
[Fe(NCS)]2++ F2+ =[FeF]2+ +SCN– Kθf == 7.1×106 。
解释:Kθf小的向Kθf大的转化。生成不同的配合物,所以颜色发生改变。由无色 →→血红色 →→无色。
(2). A孔:1d K3[Fe(CN )6] + 1d KSCN →→ 无变化。 [Fe(CN )6]3– + SCN–
B孔:1d NH4Fe(SO4)2+ KSCN +1dKSCN →→ 有血红色的[Fe(NCS)]2+生成。
Fe3+ + SCN- =[Fe(NCS)]2+
由于K3[Fe(CN )6]中的铁离子在配合物内层,不能完全电离出来,而NH4Fe(SO4)2中的铁离子完全电离。所以生成了配离子颜色发生改变由无色变成血红色。
(3). A孔:1d CuSO4+ 5d NH3H2O(过量) →→ 深蓝色的[Cu(NH3)4]2++ NaOH ≠
Cu2+ + 4NH3 ==[Cu(NH3)4]2+ 或:Cu2+ + 4 NH3H2O == [Cu(NH3)4]2++ 4.H2O
B孔:1d CuSO4+ 5d NH3H2O(过量) →→深蓝色的[Cu(NH3)4]2++ BaCl2 →→BaSO4 (s)
. CuSO4 + 4 NH3H2O == [Cu(NH3)4]SO4 + 4 H2O
由于[Cu(NH3)4]SO4中Cu2+在配合物内层,不能完全电离,而SO42-完全电离,所以A孔无反应,而B孔有白色沉淀产生。
(4)2d NiSO4 +1d NH3H2O (过量)→→蓝色的[Ni(NH3)6]2+ +丁二酮肟→→[Ni(DMG)2](s) (鲜红色)
Ni2+ + 6 NH3 ==[Ni(NH3)6] 2+
[Ni(NH3)6] 2+ + 2DMG == Ni(DMG)2(s)+4 NH3+2 NH4+
解释:由于生成了不同的配合物,所以颜色发生改变,由蓝色→→血红色的螯合物沉淀。
2. 配合物形成时难物溶解度的改变:
A离心管:3dNaCl + 3d AgNO3 →→AgCl (s) (白色)+ 3d NH3•H2O →→[Ag(NH3)2]+
AgCl +2 NH3 == [Ag(NH3)2]+ Cl– Kθ f =1.67×107
B离心管:3d KBr +3d AgNO3 →→AgBr (s)(浅黄色)+3dNa2S2O3→→[Ag(S2O3)2]3–
AgBr +2 S2O2–== [Ag(S2O3)2]3–+ Br– Kθ f =2.9×1013
C离心管:3d KI +3d AgNO3 →→AgI (s)(黄色)+ KI(过量)→→ [AgI2]–
AgI+ 2I– == [AgI2]– Kθ f = 4.8×1010
Ag + + Cl – = AgCl (s) Ag + + Br– = AgBr (s) Ag + + I–= AgI (s)
Kθsp=1.8×10-10 Kθsp=5.3×10-13 Kθsp=8.3×10-
解释:难溶化合物在配位剂的作用下,生成配离子而溶解。或由于生成配离子使难溶物的溶解度增大。
3. 配合物形成时溶液PH的改变:
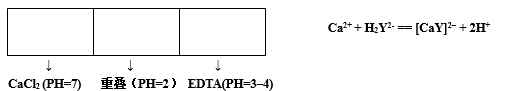
解释:(质子理论)生成配合物时,使弱酸H2Y2-的解离度增大,解理出两个H+。
配合物形成前,H2Y2-作为弱酸解离出来的H+有限,在生成[CaY]2–之后,H2Y2-中的2个H+ 作为游离离子完全留在外界,因此PH↓,C[H+]↑。也就是说配合物形成时部分H+转为外界,所以溶液酸性增强了。
4. 配合物形成时溶液中心离子氧化还原性的改变:
(1).CoCl2 + H2O2(3%) →→ 无变化. Eθ H2O2 / H2O==1.763 < Eθ Co3+ / Co2+==1.95
(2)CoCl2 +NH4Cl + NH3•H2O →→土黄色的[Co(NH3)6]2++ H2O2 →→红褐色的 2[Co(NH3)6]3+
Co2++ 6 NH3 === [Co(NH3)6]2+ 2[Co(NH3)6]2++H2O2==2[Co(NH3)6]3++2OH–
EθH2O2 / OH– ==0.867 > Eθ [Co(NH3)6]3+ / [Co(NH3)6]2+==0.17
解释:由于生成了配合物,使中心离子的氧化型的氧化能力下降,其还原型的还原能力增强。
实验六. 氯、溴、碘
下周实验:氮 、磷 。
一. 实验目的:
1. 掌握卤素单质氧化性和卤化氢的还原性的递变规律;
2. 掌握卤素含氧酸盐的氧化性;
3. 学会鉴定Cl– Br–、、I–的方法。
二. 实验原理:
氯、溴、碘氧化性的强弱次序为Cl 2>Br2 >I2 。卤化氢还原性强弱的次序HI >HBr > HCl。 HBr、HI分别将H2SO4(浓)还原为SO2和H2S;Br–能被Cl2氧化为Br2,在CCl4中显棕黄色。I–能被Cl2氧化为I2在CCl4中呈紫色,当Cl2过量时,I–被氧化为无色的IO3–。次氯酸及其盐具有强氧化性。在酸性条件下,卤酸盐都具有强氧化性,其强弱次序为ClO3–>BrO3–>IO3–。Br–,I-,Cl–与Ag+分别生成AgCl,AgBr,AgI沉淀,它们的溶度积依次减少,都不溶于稀HNO3。AgCl能溶于稀氨水,或(NH4)2CO3溶液,再加入HNO3时,AgCl会重新沉淀出来,由此可鉴定Cl–的存在。AgBr和AgI不溶于稀氨水或(NH4)2CO3溶液,它们在HAc介质中能被锌还原为Ag,可使Br–和I–转入溶液中,再用氨水将其氧化,可以鉴定Br–和I–存在。
三. 实验步骤:
1. 卤化氢的还原性:合作
分别用PH试纸 KI―淀粉试纸 Pb(AC)2试纸检验:
A孔:NaCl (s) + 1d H2SO4(浓) →→ HCl (湿润的PH试纸变红)
NaCl (s) +H2SO4(浓) == NaHSO4 + HCl ↑
B孔:KBr (s) +1d H2SO4(浓) →→ Br2↑ + SO2↑(湿润的KI―淀粉试纸变蓝,过一会蓝色褪去SO2有漂白作用)。
KBr (s) + H2SO4(浓) == KHSO4 + HBr 2HBr + H2SO4(浓) == Br2↑ + SO2↑ + 2H2O
C孔: KI (s) + 1d H2SO4(浓) →→H2S ↑ (湿润的Pb(AC)2试纸变黑)
KI (s) + H2SO4(浓) == KHSO4 + HI 8HI + H2SO4(浓) == 4I2 + H2S ↑ + 4H2O(试纸变黑)
结论: HCl < HBr < HI 还原性依次增大。
2. 氯 . 溴 . 碘含氧酸盐的氧化性:
(1)A孔: 3d Cl2 +1d 2OH–== Cl– + ClO– + H2O Eθ ClO– / Cl2==1.63 > EθCl2 / Cl–==1.36
ClO– +1d 2H– + Cl– == Cl2↑ + H2O (湿润的KI―淀粉试纸变蓝)
解释:ClO–在酸性条件氧化性强,能把Cl–氧化为Cl2↑ 。
B孔:3d Cl2 +1d 2OH–== Cl– + ClO– + H2O EθClO– / Cl–== 0.8902 〉EθI2 / I– ==0.5345
ClO– +2-3d 2I– + H2O == I2 + Cl– + 2OH– ( 加淀粉试液1d,溶液变蓝)
解释:ClO–能把I–氧化为I2,I2遇淀粉变蓝。
C孔:3d Cl2 +2 OH– == Cl– + ClO– + H2O ClO– +1d 品红→→品红褪色 。
解释:ClO–具有漂白性
Cl2 + OH–显弱碱性?
① 因为碱性太强ClO–的氧化性会降低。
② I2在强碱性溶液中会发生岐化反应,岐化为I–、IO3– ,加淀粉试液不变蓝。
(2)2d KClO3 +1d HCl(浓) →→ Cl2↑ KI―淀粉试纸变蓝.
ClO3– + 5Cl– + 6H+ == 3Cl2 ↑ + 3H2O Eθ ClO3– / Cl2==1.458 > Eθ Cl2 / Cl–==1.36
解释:ClO3–在酸性条件具有氧化性。
(3).2d KClO3(饱和)+ 1d KI + 逐滴H2SO4(1:1)→→ 边加边振荡试管,溶液由黄→→紫红→→无色。
① ClO3– + 9I– + 6H+ == 3I3– + Cl– + 3H2O (黄) Eθ ClO3– / Cl–==1.43 > Eθ I2/ I–==0.5435
由于加H+量少,这时ClO3–的氧化能力较弱,只能把部分I–氧化为I2。I2溶解在I–里,显I3–为黄色。
有时看不见I3–的黄色,直接看到的是I2,因为I–加得多。
② ClO3– + 6I3– + 6H+ ==9I2+ Cl– + 3H2O (紫红) Eθ ClO3– / Cl–==1.43 > Eθ I2/ I–==0.5435
随着H+加入量的增多,ClO3–的氧化能力增强。把所有的I–氧化为I2。
③ ClO3– + 3I2 + 3H2O == 6 IO3– + 5Cl– + 6H+ (无色) Eθ ClO3– / Cl–==1.43 > Eθ IO3–/ I2 ==1.209
酸性加强。ClO3–把I2氧化成无色的IO3–。
(有时溶液中出现绿色,是因为KClO3(饱和)把Cl–氧化成Cl2↑)
解释:在酸性条件下,KClO3具有较强的氧化性,I–具有还原性。
(4). 1d KIO3 + 2d NaHSO3 + 5d CCl4+1d H2SO4(酸化) →→ CCl4层有紫红色I2
2IO3– + 5HSO3– == I2 + 2SO42– 3HSO4– + H2O Eθ IO3– / I2==1.209 > Eθ SO42– / SO32– == 0.1576
3. Cl–、 Br–、I– 的鉴定:
(1). 1d NaCl +1d AgNO3 + 1d HNO3(酸化)→→ AgCl(白色)↓ + NH3•H2O→→+ HNO3→→ AgCl(白色)↓ Ag+ + Cl– == AgCl (s) AgCl +2NH3==[ Ag(NH3)2]+ + Cl– [ Ag(NH3)2]+ +2H+ + Cl–== AgCl (s)
解释:加NH3•H2O生成[ Ag(NH3)2]+,使Ag+ 浓度降低,平衡向生成[Ag(NH3)2]+的方向移动,AgCl转化为[ Ag(NH3)2]+,在加HNO3后降低了NH3的浓度,所以AgCl又重新析出。
鉴定Cl– 时为什么加HNO3? 因为:①生成的AgCl不溶HNO3。② 加HNO3为了酸化AgNO3,保证AgNO3的浓度,防止AgOH至Ag2O出现。③ 不加H2SO4的目的是防止生成白色Ag2SO2↓,不加HCl的目的是不引进相同离子。
(2). 2d KBr + 5d Cl2 + 1d H2SO4(酸化)+5d CCl4→→ CCl4 层中由无→→黄→→橙红
2Br– +Cl2=Br2 + 2 Cl– Br2+ Cl2(过量)==BrCl E θCl2 / Cl–==1.36 > Eθ Br2 / Br– ==1.077
解释:Br–于适量的Cl2水反应游离出Br2溶液显橙红色,在加入CCl4显红棕色,再加入过量的Cl2溶液显浅黄色。
(3). 1d KI +10d Cl2 + 1d H2SO4(酸化)+ 5dCCl4 →→CCl4 层中由无→→紫红→→无
2I– + Cl2 == I2+ 2 Cl– I2+ 5 Cl2(过量) +6 IO3– + 10 Cl– + 12 H+
解释:I–在酸性介质中被Cl2氧化为I2,I2在CCl4层中显紫红色,加入过量的Cl2将I2氧化为IO3–而颜色消失。
实验七. 氮 磷
下周实验:分光光度法测定[Ti(H2O)6]3+的分裂能。
一. 实验目的
1 掌握硝酸,亚硝酸及其盐的重要性质 ,
2 了解磷酸盐的主要性质,
3 NaNO3,NH4NO3,Na3PO4,NaNO2的鉴定方法。
二. 实验原理
鉴定NH4+的常用方法有两种。一是NH4+与OH–的反应,生成NH3(g)使红色石蕊试纸变蓝,二是NH4+与奈斯勒试剂的碱性溶液反应生成红棕色沉淀。
亚硝酸极不稳定。亚硝酸盐溶液与强酸反应生成的亚硝酸分解为N2O3和水,N2O3又分解为NO和NO2。
亚硝酸盐中氮的氧化值为+3,它在酸性溶液中作氧化剂。一般被还原为NO;与强氧化剂作用时则生成硝酸盐。
硝酸具有强氧化性,它与许多非金属反应。主要还原产物是NO。浓硝酸与金属反应,主要生成NO2,稀硝酸与金属反应通常生成NO。活泼金属能将稀硝酸还原为NH4+。
NO2–与FeSO4溶液在HAC介质中,反应生成棕色的[Fe(NO)(H2O)5]2+或[Fe(NO)]2+
NO2-+ Fe2++2 HAC== NO +Fe3++2AC-+ H2O 、 Fe2++NO→→[Fe(NO)]2+
NO3–与FeSO4溶液在浓H2SO4介质中反应生成棕色的[Fe(NO)]2+:
3Fe2++ NO3–+4 H+→→3Fe3++NO+2H2O Fe2++NO→→[Fe(NO)]2+
在试液与浓H2SO4层界面处生成的[Fe(NO)]2+,呈棕色环,此方法于鉴定NO3–,成为棕色环法。NO2–的存在干扰NO3–的鉴定,加入尿素并微热,可除去NO2– :
2NO2-+ CO(NH2)2+2 H+→→N2+ CO2+3H2O
碱金属(锂除外)和铵的磷酸盐、磷酸一氢盐易溶于水,其他磷酸盐难溶于水。大多数磷酸二氢盐,易溶于水。焦磷酸和三聚磷酸盐都具有配位作用。
PO43-与(NH4)2 MoO4溶液在浓硝酸介质中反应,生成黄色的磷钼酸铵沉淀。此反应可鉴定PO43-。
三. 实验步骤:
1.NH4+的鉴定:
(1)5d NH4Cl +5d NaOH →→ NH3↑ 用湿润的红色石蕊试纸变兰。
NH4+ + OH– == NH3↑+ H2O
(2). 5d NH4Cl + 5d NaOH →→ 用滴有奈斯勒试剂滤纸条放在试管口上,有棕红色斑点产生。说明有NH4+存在。
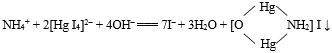
2. 硝酸的氧化性:
(1)Cu (片) + 10d HNO3(浓) →→(NO2)↑红棕色 Eθ NO3– / NO2==0.7989 >Eθ Cu2+ / Cu==0.3394
Cu + 4HNO3(浓)== Cu(NO3)2 + 2 NO2 ↑ + 2H2O
解释:浓HNO3与金属反应主要产物是NO2气体。
(2)Zn (粉) + 10d HNO3(2.0)→→ NH4+ (活泼金属与稀HNO3反应可得到NH4+)
4Zn + 10HNO3 == 4Zn (NO3)2 + NH4+ 3 H2O Eθ NO3– / NH4+==0.88 > Eθ Zn / Zn2+== –.07621
取清液检验是否有NH4+:NH4++ OH– = NH3↑ + H2O 用奈斯勒试剂的滤纸条检验。如果加OH–有白色的Zn(OH)2生成,然后再加过量的OH–,使Zn(OH)2转化为[Zn(OH)4]2–无色溶液。
3. 亚硝酸及其盐的性质:
(1)5d NaNO2 +1d H2SO4 (6M)→→在亚硝酸盐的溶液中加入强酸时可生成HNO2,溶液的液面上有红棕色NO2 ↑
NaNO2+ H2SO4==Na HSO4+ H NO2 亚硝酸极不稳定,只存在于很稀的冷溶液中,溶液浓缩或受热时就分解为N2O3 + H2O ,N2O3又分解为NO2 、NO,气相中有红棕色气体,液相中为浅蓝色。
2H NO2==N2O3(淡蓝色)+ H2O N2O3== NO2 ↑+ NO↑
(2).5d NaNO2 + 1d KI→→无变化+1dH2SO4(酸化)→→I2 +1d 淀粉溶液→→ 变蓝
2NO2-+ 2I-+4 H+==2 NO+ I 2+ 2H2O EθNO2-/ NO==1.04 > Eθ I 2/I-==0.5345
解释:亚硝酸在酸性介质中具有氧化性,把I-氧化成I2,本身被还原成NO↑。
(3)2-3d NaNO3 + 1d KMnO4 +1d H2SO4 →→Mn2+ NO3–
2MnO4-+5 NO2–+6 H+==2 Mn2++5 NO3– +3 H2O EθMnO4-/Mn2+==1.512>EθNO3-/ NO2-==0.94
解释:NO2– 与强氧化剂作用则生成NO3– 。(在酸性条件下)
4.NO3-和NO2-的鉴定 :
(1).2d KNO3 +1ml 水+2-3勺FeSO4•7H2O+20d H2SO4(浓)→→ [Fe(NO)(H2O)5]2+ (棕色环)
3Fe2++ NO3–+4 H+==3Fe2++ NO+ 2H2O [Fe (H2O)6]2+ + NO == [Fe(NO)(H2O)5]2+ + H2O
解释:在放有FeSO4和硝酸盐的混合溶液中,小心加入浓H2SO4,于溶液的接触面出现“棕色环”。这是由于生成了配合物[Fe(NO)(H2O)5]2+而显颜色,[Fe(NO)(H2O)5]2+不稳定,微热获振荡会立即消失。
(2).1d NaNO2 +1ml水先+20d HAC(防止FeSO4水解)+ FeSO4•7H2O→→[Fe(NO)(H2O)5]2(棕色溶液)。
Fe2++ NO2–+2 H+==Fe2++ NO+ H2O [Fe (H2O) 6 ] 2+ + NO == [Fe(NO)(H2O)5]2+ + H2O
(3).2d KNO3+2d NaNO2 +1ml水+尿素+2d H2SO4→→有气泡放出CO2 ↑+N2↑ 消除NO2-,
2NO2–+2 H+ CO(NH2)2== 2 N2↑+ CO2↑+3 H2O
解释:酸化后的KNO3、NaNO2溶液加尿素微热,NO2–与N2↑形式出来所以就排除了NO2–时鉴定NO3–的干扰等气泡冒完,在进行“棕色环”实验。
3Fe2++ NO3–+4 H+==3Fe2++ NO+ 2H2O [Fe (H2O) 6] 2+ + NO == [Fe(NO)(H2O)5]2+ + H2O
5. 磷酸盐的性质:
(1)用PH试纸分别测定Na3PO4,Na2HPO4,NaH2PO4
Na3PO4 PH值=12.57 PO43-+ H2O←→HPO42-+OH- 只水解显碱性。
Na2HPO4 PH值=10.10 HPO42-+ H2O←→H2PO4-+ OH- 以水解为主。
NaH2PO4 PH值=4.10 H2PO4-+ H2O←→HPO42-+H3O+ 以解离为主。
解释:磷酸的各钠盐均水解,水解程度大于解离程度,以水解为主。
(2).A孔: 2dCa2++ 2dNa3PO4→→白↓ Ca3(PO4)2↓ 磷酸正盐难溶。
B孔: 2dCa2++2d Na2HPO4→→白↓ Ca HPO4↓ 磷酸一氢盐难溶。
C孔:2dCa2++ 2dNaHPO4→→ 没有沉淀 磷酸二氢盐可溶。
3Ca2++ 2PO43-== Ca3(PO4)2 Ca2++HPO42-== Ca HPO4↓
(3). 2d 2Cu2++ P2O74– == Cu2 P2O7 (s) (浅蓝色) Cu2 P2O7+3 P2O74– == 2[Cu(P2O7)2]6- (蓝色溶液)
解释:焦磷酸盐具有配位作用。
(4). 2d Ca2++ 2d CO32 -== CaCO3 白↓ CaCO3↓+ 3-5d P3O10-5= Ca(P3O10)3-+ CO32-
解释:三聚磷酸具有配位作用。
6 . 磷酸的鉴定:
2d Na3PO4 +2d HNO3 +2-3d钼酸铵→→ 有黄色沉淀 ↓ 。
PO43–+3 NH4+12MoO42–+24 H+ == ( NH4)3 PO4·12 MoO3·6 H2O (s) + 6H2O
HNO3别多加,多了以后灰生成白色的钼酸。
7. 鉴定4种白色晶体的鉴别: NaNO2 ,NaNO3,NH4NO3;Na3PO4。
每个同学发放一包未知药品,用50ml蒸馏水溶液,大概溶度为0.1mol·L–1,取少量待测溶液放入试管中,首先用排除法把NH4+排除,然后再鉴定是否Na3PO4、NO 3- 、NO 2-。
(1). 待测溶液 + OH- == NH3 ↑ 。用奈氏试剂检验。
(2).待测溶液 + 钼酸铵 →→ 黄色↓ 。
(3). 待测溶液 + FeSO4•7H2O+ H2SO4→→ 棕色环。
(4). 待测溶液 + FeSO4•7H2O+ HAC→→棕色容液。
实验八. 分光光度法测定[Ti(H2O)6]3+的分裂能
下周实验: 铬 锰 。
3. 实验目的:
1. 了解配合物的吸收光谱。
2. 了解用分光光度法测定配合物分裂能的原理和方法。
3. 学习721型分光光度计的使用方法。
4. 实验原理:(略)
在课上老师给讲了实验原理,今天我主要讲一下721型分光光度计的工作原理及使用方法,用分光光度法测定[Ti(H2O)6]3+分裂能的测定方法。
721分光光度计的工作原理:当一束单色光(一定波长的光)通过溶液时,光的一部分被溶液吸收,一部分透过溶液。如果比色皿中装的是无色溶液如:蒸馏水,当一束单色光通过这无色溶液时,这束单色光100%通过,也就是说透光率100%。单色光透过溶液时,这束单色光一部分通过溶液,一部分被溶液吸收,吸收多少用吸光度A来表示,A的数值越大,测溶液对光的吸收程度也越大。
朗伯比尔定律总结了溶液对光的吸收规律:当一束单色光透过有色溶液时,有色溶液的吸光度A与溶液的浓度C和液层厚度L的乘积成正比,即A=ε·C·L 比例常数ε叫光密度系数,它与物质的性质,入射光的波长和溶液的浓度等因素有关。
三. 用分光光度法测定[Ti(H2O)6]3+的分裂能的方法。
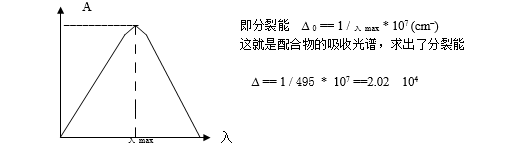
晶体场的分裂能△0大都是由配合物也就是络合物的吸收光谱求得的,例如 :[Ti(H2O) 6]3+的吸收光谱,配制一定浓度的 [Ti(H2O) 6]3+溶液,用分光光度计测出不同波长入下的吸光度A,以A为纵坐标,以入为横坐标作图,可得吸收曲线,曲线最高峰所对应的入max 为[Ti(H2O)]3+的最大吸收波长 。
四. 721型分光光度计的使用。
⑴ 接通电源,打开暗箱槽,预热15分钟。
⑵ 用泼长调节器调到所需泼长的位置。
⑶ 打开暗箱盖调调零点调节器,使指针为“0”。
⑷ 蒸馏水作参比液调透光率为100℅。
⑸ 将成水的比色皿放在比色槽架的第一格内,待测液放在第二、三格内,然后盖好暗箱盖。
⑹ 拉动拉杆,用蒸馏水调透光率为100℅,在拉一下使 待测液对准光路,表盘指针所指的读数就是该溶液在一定泼长下的光密度。
使用721分光光度计时的注意事项:
⑴使用比色皿使注意拿比色皿的麻面,别拿光面。用镜头纸擦,使用前,用别测溶液冲洗三遍。
⑵调波长、换溶液时都要打开暗箱盖。(只要不测就打开暗箱盖)使光电管休息。
⑶盖暗箱盖,打开暗箱盖,或旋转旋钮时动作要轻,(因为暗箱盖有两颗螺丝钉打弯后就盖不严)。
六. 实验步骤:
1. 配溶液.
(1) 用吸量管吸取5ml TiCl3 溶液(15~20%)于50ml容量瓶中。用去离子水稀释到刻度摇匀。
(2) 然后将此溶液转移到1公分的比色皿中。
(3) 蒋蒸馏水转移到另一个比色器中,调100% 用。
2.测定:以去离子水为参比液,用分光光度计在波长为460~550nm的范围内,每隔10mm测一次光密度,在接近峰值附近500nm附近每隔5nm各测一次。
5. 数据处理
(1). 测定纪录
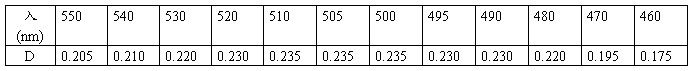
以入为横坐标,以D光密度为纵坐标作曲线图。
4. 计算:△0 在吸收曲线上找出最大高峰,所对应的波长计算[Ti(H2O) 6]3+的分裂能。
△0 = 1/ 入 *107 (cm–1)
注意:(1) 5ml吸管的使用。
(2) 50ml溶量瓶的使用。
实验九. 铬 锰
下周实验: 铁 钴 镍。
一 实验目的:
1 . 掌握铬、锰氢氧化物的酸碱性和氧化还原性。
2. 掌握铬、锰重要氧化态之间的转化反应及其条件。
3 . 掌握.铬硫化物的生成和溶解性。
4. 学习 Cr3+ 、 Mn2+ 的鉴定方法。
二. 实验原理
铬、锰是周期系第四周期,第VIB-Ⅷ族元素,它们都能形成多种氧化值的化合物,铬的重要氧化值为+3和+6;锰的重要氧化值为+2,+4,+6,+7。
Cr(OH)3是两性氢氧化物。Mn(OH)2易被空气中的氧气氧化为MnO(OH)2
Cr3+易发生水解反应,酸性溶液中的] Cr3+和Mn2+的还原性都较弱,只有用强氧化剂才能将它们分别氧化为Cr2O72–和MnO4-,在酸性条件下,利用Mn2+和NaBiO3的反应可以鉴定Mn2+。。
在重铬酸盐溶液中分别加入Ag+,Pb2+,Ba2+等都能生成相应的铬酸盐沉淀。
Cr2O72–和MnO4-都具有强氧化性,酸性溶液中Cr2O72–被还原为Cr3+。MnO4-在酸性,中性,碱性溶液中的还原产物分别为Mn2+,MnO2, MnO4-。在强碱性溶液中MnO4-与MnO2反应也能生成MnO4-。在酸性甚至近中性溶液中MnO4-,歧化为MnO2和MnO4-。在酸性溶液中MnO2也是强氧化剂。MnS能溶于稀酸,MnS还能溶于HAC溶液,这些硫化物需要在弱碱性溶液中制得。
三. 实验步骤:
1. 铬锰氢氧化物的生成和性质:①②③
(1).2d CrCl3 +1d NaOH →→Cr(OH)3(s) (灰绿色) Cr3+ + 3OH– == Cr(OH)3(s)
Cr(OH)3(s) + H+ →→ Cr3+ (兰绿色) Cr(OH)3 + 3 H+ == Cr3+ + 3H2O
Cr(OH)3(s) + OH– →→ [Cr(OH)4]– (亮绿色) Cr(OH)3+OH– == [Cr(OH)4]–
解释:Cr(OH)3显两性。
(2).A孔:2d MnSO4 +1d NaOH →Mn(OH)2 ↓ (肉色) Mn2+ + 2OH– == Mn(OH)2 ↓+2 H+ == Mn2++ H2O
B孔:2d MnSO4 +1d NaOH →→Mn(OH)2 ↓ (肉色) Mn2+ + 2OH– == Mn(OH)2 ↓+2 OH– ≠ 不溶。
C孔:2d MnSO4 +1d NaOH →→Mn(OH)2 ↓ (肉色) Mn2+ + 2OH– == Mn(OH)2 ↓+ O2 ==2 MnO(OH)2 (s) (褐色)
结论:Mn(OH)2是碱性氢氧化物,Mn(OH)2在碱性介质中还原性较强,空气中易被氧化。
2. Cr3+的还原性和Cr3+的鉴定:
2d CrCl3 + 3-4d NaOH →→ [Cr(OH)4]–(亮绿色)+ 5-6d H2O2 3%→→变为黄色的CrO42–+3d H2O2 3% +10d戊醇+5d HNO3→→CrO(O2)2(过氧化铬深蓝色)+ 5d HNO3 →→溶液变为兰绿色。
(1) Cr3+ +4OH– == [Cr(OH)4]– (2) . 2[Cr(OH)4]– + 3 H2O2 + 2 OH– == 2 CrO42– +8 H2O
(3)2 CrO42–+ 2H+ == + H2O (4).Cr2O72–4 H2O2 +2H+ ==2 CrO(O2)2 + 5 H2O。
(5)CrO(O2)2 +12H +==4Cr3++7O2+6H2O 。(溶液PH==2~3、如果PH < 1看不见CrO(O2)2深蓝色)
解释:在酸性条件下 [Cr(OH)4]–具有较强的还原性,能被过氧化氢氧化为CrO42–。
2[Cr(OH)4]– + 3 H2O2 + 2 OH– == 2 CrO42– +8 H2O
3. CrO42– 和Cr2O72– 的互相转化:
(1). 点滴板 2d K2CrO4+1d H2SO4 →→由橙红变为橙黄Cr2O72– +2d NaOH →→ 转变为橙红色CrO42–。
2CrO42–+2H+== Cr2O72–+H.2O. (PH<2溶液中以Cr2O72–占优势)
Cr2O72– +2OH– == 2CrO42–+ H.2O (PH<6溶液中以CrO42–占优势)
(2).A孔:1dK2CrO4 + 1dBaCl2→→ BaCrO4 ↓ (黄色) + HCl →→ 橙红色的Cr2O72– 。
CrO42– + Ba2+ == BaCrO4(s) 2 BaCrO4 + 2H+ == 2 Ba2+ + Cr2O72–+ H.2O
B孔:1d K2Cr2O7 + 1d BaCl2 == BaCrO4 ↓ (黄色) + HCl →→ 橙红色的Cr2O72– 。
Cr2O72– +2Ba2+ + H.2O == 2 BaCrO4(s) + 2H+ 2 BaCrO4 + 2H+ ==2 Ba2+ +Cr2O72–+ H.2O
解释:铬酸盐比重铬酸盐的溶解度小,所以可以相互转化。
4.Cr2O72–的氧化性和MnO4–的氧化性:
(1).2d K2Cr2O7+100d H2S(饱和) +5d H2SO4→→ 有S ↓(黄绿色混浊物)+ Cr3+(蓝绿色)。
Cr2O72– + 3 H2S +8 H+ == 3 Cr3+ +3 S(s)+ 7 H.2O EθCr2O72– / Cr3+ ==1.33 > Eθ S / H2S == 0.1442
解释:Cr2O72–在酸性条件下具,具有强氧化性,能把S2–氧化S↓,自身被还原为Cr3+。
(2).1d KMnO4 +1d MnSO4 + 1d H2SO4→→棕黑色的MnO2↓ (中性条件下)
2MnO4– +3 Mn2+ +2 H.2O==5 MnO2 (s) + 4H+ Eθ MnO4– / MnO2 =1.700>EθMnO2 / Mn2+==1.229
解释:MnO4–在中性条件下,把Mn2+氧化为棕黑色的MnO2↓ 。
(3).10d KMnO4 + MnO2 (s) +8d NaOH(40%)→ 上层清液为绿色的(MnO42–)取清液+8d H2SO4→→MnO4–
2MnO4–+ MnO2 (s) + 4OH– ==3MnO42–+2 H.2O
解释:在强碱性条件下,强氧化剂(MnO4– )能把MnO2氧化为MnO42–, MnO42–只有在(PH >13.5)溶液中才能稳定存在,酸性介质或接近中性中MnO42– 岐化。
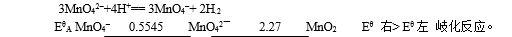
5. 铬 锰硫化物的性质:
(1).1d Cr(SO4)3 +1d Na2S →→ H2S ↑ 、Cr(OH)3 (s) 。
2Cr3+ + 3S2– + 6H2O == 2 Cr (OH)3 (s) + 3 H2S ↑ (湿润的Pb(AC)2试纸变黑)
解释: Cr3+在Na2S溶液中完全水解。
(2).2d MnSO4 +2-3d H2S(饱和)→→无 ↓ + NH3•H2O →→ 生成肉色的MnS ↓ + HAC→→ 沉淀溶解。
Mn2+ + H2S + 2 NH3•H2O == MnS (s) +2NH4+ + 2H2O MnS +2HAC== Mn2+ + H2S ↑ + 2AC–
解释:MnS 酸性条件下溶解度大,在碱性介质中才能存在。
实验十. 铁 钴 镍
一. 实验目的:
1. 掌握铁、钴、镍氢氧化物的酸碱性和氧化还原性。
2. 掌握铁、钴、镍配合物的生成和性质。
3. 掌握铁、钴、镍硫化物的生成和溶解性。
4. 学习Fe3+ 、Fe2+ 、CO2+ 、Ni2+的鉴定方法。
二. 实验原理:
铁、钴、镍是同期系第四周期第VIB-Ⅷ族元素,它们都能形成多种氧化值的化合物,铁 钴 镍的重要氧化值都是+2和+3,由于Co3+和Ni3+ 都具有氧化性,Co(OH)3、Ni(OH)3与浓HCl反应分别生成CO(II)和Ni(II),并放出氧气,Co(OH)3、Ni(OH)3通常分别由C CO(II)和Ni(II)的盐,在碱性条件下用强氧化剂氧化得到,例如:2Ni2++ 6OH– +Br2 →2Ni(OH)3(s)+2 Br– 。
Fe3+易发生水解反应,Fe3+具有一定的氧化性,能与强还原剂反应生成Fe2+ 。
FeS 、CoS 、NiS 都能溶于稀酸,这些硫化物需要在弱碱性溶液中制得,生成的CoS 、NiS沉淀由于晶体结构改变而难溶于稀酸。
铁 钴 镍都能形成多种配合物,Co2+ 和Ni2+都能与过量的氨水反应生成[Co(NH3)6]2+和[Co(NH3)6]3+ 。
[Co(NH3)6]2+溶被空气中的O2氧化为[Co(NH3)6]3+,Fe2+与[Fe(CN)6]–3反应,或Fe3+与[Fe(CN)6]–4反应都能生成蓝色的沉淀,分别用于鉴定Fe2+和Fe3+,酸性溶液中,Fe3+与SCN– 反应也用于鉴定Fe3+。Co2也与SCN–反应生成不稳定的[Co(NCS)4]2–,在丙酮等有机溶剂仲较稳定,此反应用于鉴定,Co2+、Ni2+与丁二酮肟在弱碱性条件下反应生成先红色的内配盐,此反应常用于鉴定Ni2+ 。
三. 实验步骤:
1. 铁 钴 镍氢氧化物的生成和性质:
(1). A管:2ml水 + 2d H2SO4 →→煮沸除氧 + FeSO4(s) (少量)。
B管:1mlNaOH →→ 煮沸除氧,Fe2+ +2OH– == Fe(OH)2(s)(白色)

解释:Fe(OH)3为碱性氢氧化物,氧化性较弱。
(5).2d CoCl2 + 2dBr2 +5-6d NaOH →→Co(OH)3 (s) 离心分离,在沉淀中加3-4d浓HCl →→CoCl2 +Cl2 ↑ 淀粉—KI试纸检验变 2Co2+ + Br2 +6OH– == 2Co(OH)3 (s) + 2 Br –
2Co(OH)3 + 6HCl (浓) == CoCl2 + Cl2 ↑ + 6 H2O EθA Co3+ / Co2+ == 1.95 > EθCl2 / Cl– == 1.36
解释:Co(OH)3 具有较强的氧化性。
(6).2d NiSO4 + 2d Br2 +5-6dNaOH →→ Ni(OH)3(s) (黑) 离心分离,在沉淀中3-4d HCl(浓)→→NiCl2 +Cl2 ↑ 淀粉—KI试纸检验变蓝。 2Ni2+ + Br2 +6 OH–== 2Ni(OH)3 (s) + 2 Br –
2Ni(OH)3 + 6HCl (浓) == NiCl2 + Cl2 ↑ + 6 H2O Eθ Ni3+ / Ni2+ == 1.68
解释:Ni(OH)3 具有较强的氧化性。
通过(4) (5) (6)得结论:氧化性Ni(OH)3 > Co(OH)3 > Fe(OH)3
2. Fe3+的氧化性与Fe2+的还原性:
(1).1d KMnO4 + 1d H2SO4 +1d FeSO4 →→ Mn2+ 、 Fe3+现象:紫红色退去
MnO4– + 5Fe2+ + 8H+ == 5 Fe3+ +Mn2+ + 4H2O Eθ MnO4– / Mn2+ == 1.517 > Eθ Fe3+ / Fe2+ == 0.769
解释:在酸性条件下,Fe2+具有还原性
(2).1d FeCl3 +1d SnCl →→ Fe2+ Sn4+
2 Fe3+ + Sn2+ == 2 Fe2+ + Sn4+ Eθ Sn4+ / Sn2+ == 1.539 < Eθ Fe3+ / Fe2+ == 0.769
解释:在酸性条件下, Fe3+ 为中强氧化剂。
3. 铁、钴、镍硫化物的性质:
(1).A孔:1d FeSO4+ 2d H2S →→ 无↓ +NH3•H2O→→ 黑色的FeS (s)
NH3•H2O
Fe2+ + H2S ======== FeS (s) +2H+ 、 FeS +2H+ == Fe2+ + H2S ↑
B孔:1dCoCl2 +2d H2S →→ 无↓ + NH3•H2O→→ 黑色的CoS (s)
NH3•H2O
Co2+ + H2S ======== CoS (s) +2H+ 、 CoS +H+ == 不溶解
C孔:1d NiSO4 +2d H2S →→ 无↓+ NH3•H2O→→ 黑色的NiS (s)
NH3•H2O
Ni2+ + H2S ======== NiS (s) +2H+ 、 NiS + 2H+ == 不溶解
解释: FeS 、CoS 、NiS都溶于稀盐酸,但加入(NH3•H2O后是非酸性条件下(弱碱性),CoS 、NiS发生了晶型改变。所以:CoS 、NiS 不溶于稀酸。
(2). 1dFeCl3+2-3d H2S →→ Fe2+ S (s) 有黄色浑浊物产生
2 Fe3+ + H2S == 2 Fe2+ + S(s) +2H+ 、 Eθ Fe3+ / Fe2+ == 0.769 > EθS / H2S == 0.1442
发生了氧化还原反应
4. 铁、钴、镍的配合物:
(1). 1d K4[Fe(CN)6] + 1d FeCl3 →→ 普鲁氏蓝 (K4[Fe(CN)6]3 ↓)
3[Fe(CN)6]4–+ 4 Fe3+ == Fe4[Fe(CN)6]3 ↓ (鉴定Fe3+的特征反应)
1d K3[Fe(CN)6] +1d FeSO4 →→ 腾 士 蓝 (K3[Fe(CN)6]2 ↓)
2[Fe(CN)6]3–+ 4 Fe2+ == Fe 3[Fe(CN)6]2↓ (鉴定Fe2+ 鉴的特征反应)
(2). 1d CoCl2 + 1d NH4Cl + 2d NH3•H2O →→ [Co(NH3)6]2+土黄色→→ 空气静置后变成红色
Co2+ 6 NH3 ===== [Co(NH3)6]2+ 4 [Co(NH3)6]2+ O2 + 2H2O == 4 [Co(NH3)6]3+ + 4OH–
生成配合物后中心离子的氧化还原性发生了变化
(3). 1d CoCl2 + 1d KSCN (饱和) + 1d丙酮 →→ 溶液变蓝
Co2+ + 4 NCS– == [Co(NCS)4]2– (鉴定Co2+ 的特征反应)。
