实验二十五 凯氏定氮法测定生物样品中有机氮的含量
一﹑实验目的
1.学习凯氏定氮法的基本原理和操作;
2.用凯氏定氮法测定生物样品中氮的含量。
二﹑实验原理
凯氏定氮法是使样品经硫酸和催化剂一同加热消化,使有机氮分解,其中有机氮素转化为氮,与硫酸化合为硫酸铵。然后加碱蒸馏,使铵游离出来,用硼酸吸收,再用标准硫酸或盐酸滴定,根据标准酸的消耗量,即可计算有机氮的含量。
三﹑主要仪器及试剂
1.凯氏定氮瓶及蒸馏装置 2.硫酸铜
3.硫酸钾 4.硫酸
5.2%硼酸溶液 6.40%氢氧化钠溶液
7.0.2%甲基红 8.0.2%溴甲酚绿
9.0.2%甲基红及0.2%溴甲酚绿的1+5混合指示剂
10.0.1mol/L的标准盐酸溶液(或1/2硫酸溶液):
0.1mol/LHCl的配制及标定:吸取9mL浓HCl注入大约1000mL无二氧化碳蒸馏水中,此溶液浓度约为0.1mol/L,用下述方法进行标定:准确称取于180℃烘2小时,并于干燥器内冷至室温的无水碳酸钠1~1.5g,置于250mL容量瓶中,定容后摇匀,用移液管吸取25mL放入锥形瓶内,加入无二氧化碳蒸馏水至100mL及4滴甲基橙指示剂,用待标的0.1mol/LHCl滴定至淡桔红色,记录用量。同时用无二氧化碳蒸馏水做空白滴定。计算盐酸标准溶液的浓度。
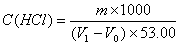
式中: m — 无水Na2CO3的重量,g;
V1— 滴定无水Na2CO3消耗HCl溶液体积,mL;
V0— 滴定无二氧化碳蒸馏水消耗HCl溶液体积,mL;
53.00— M(1/2 Na2CO3),g/mol。
四﹑实验操作步骤
精确称取固体试样1g(含氮总量约30-40mg)于500mL凯氏定氮瓶中,加研细的硫酸铜0.5g,硫酸钾10g,浓硫酸20mL,轻轻摇匀。于瓶口装好小漏斗,将凯氏瓶以45°角斜支于石棉网上,小火加热,使其全部碳化(泡沫消失)后,加强火,使溶液微沸,至液体变为蓝绿色透明再加热30min。冷后加200mL水再放冷。连接蒸馏装置,冷凝管下端插入接收瓶液面下。接收瓶内盛有2%硼酸溶液50mL及混合指示剂2-3滴。从漏斗放入40%氢氧化钠溶液70-80mL,摇动,瓶内物料变为深蓝色或产生黑色,自漏斗再加水100mL。加热蒸馏至氨全部蒸馏出来(250mL),使冷凝管下端离开吸收液,再蒸馏1min,停止加热。用水冲洗冷凝管下端的外部下端。吸收液用标准盐酸滴定至灰色为终点。同时做空白实验。
注意事项
1.消化时若不易呈透明溶液,可将试液放冷后慢慢加入30%过氧化氢2—3mL,以促进氧化。
2.消化过程以微火集中于凯氏瓶底部,保持缓慢沸腾,避免试样溅于瓶壁,难于消化使氨损失。
3.实验中要保证硫酸足量,否则过多的硫酸钾形成硫酸氢钾,而削弱了硫酸的消化作用。硫酸钾的作用是增加溶液的沸点,硫酸铜为催化剂,而且可做蒸氨时加入碱量的指示剂。
五﹑实验结果计算
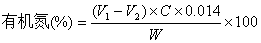
式中:V1—样品消耗标准酸的体积, mL;
V2—试剂空白消耗标准酸的体积,mL;
C—标准盐酸的物质的量浓度,mol/L;
0.014—每毫升1mol/LHCl相当于氮的克数
W—样品重量(或体积),g(或mL)。
数据列表表示如下:
1.盐酸浓度的标定:
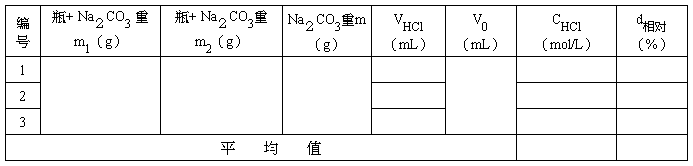
2.样品测定:
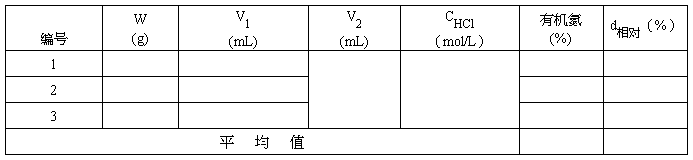
六﹑思考题
1.蒸氨时为什么蒸馏瓶内要加浓碱?吸收液为什么要用硼酸溶液?为什么要将冷凝管下端插入接收瓶液面下?能否用其它的酸代替硼酸?
2.试样消化过程中 加入浓硫酸、硫酸铜、硫酸钾的作用是什么?
3.为什么消化完全时试液呈兰绿色,而加入40%NaOH溶液变为深蓝色或棕黑色?
第二篇:01 生物化学实验--凯氏(Kjeldahl)微量定氮法测定血清蛋白质含量
凯氏( Kjeldahl )微量定氮法测定血清蛋白质含量
【目的】
1 .掌握微量凯氏定氮法的操作技术,包括未知样品的消化蒸馏、滴定及其含氮量的计算等。
2 .熟悉微量凯氏定氮法的原理。
【原理】
凯氏定氮法是蛋白质含量测定的经典方法,它是根据蛋白质分子中含氮量来测定的,各种蛋白质含氮量比较近似,平均约为 16 %,即 1g 氮相当于 6.25g 蛋白质。由测定出 的氮量即可换算出蛋白质含量。
血清蛋白质或其它有机含氮物与浓硫酸加热进行消化 ( 氧化 ) 时,其中碳、氢、氧元素分别被氧化为二氧化碳和水,而氮原子则转变成氨,后者与硫酸结合生成硫酸铵,留在溶液中,为了加速有机物质的氧化分解,在消化时加入硫酸铜做为催化剂,加入硫酸钾以提高消化液的沸点。硫酸铵与氢氧化钠作用,放出氨,通过水蒸气蒸馏将氨带入接收瓶中被硼酸溶液吸收,使溶液中氢离子浓度降低,指示剂颜色发生改变,用已知浓度的标准盐酸滴定,直至原来溶液中氢离子的浓度恢复,即指示剂变为原来的颜色。根据所消耗的标准盐酸量,即可计算出样品中的总氮量。化学反应式如下:
1 .消化
含氮化合物 +H 2 SO 4 —→CO 2 ↑+H 2 O +(NH 4 ) 2 SO 4 +SO 2 ↑
2 .蒸馏
(NH 4 ) 2 SO 4 + 2NaOH—→2NH 4 OH+Na 2 SO 4
NH 4 OH—→NH 3 ↑+ H 2 O
3NH 3 +H 3 BO 3 —→(NH 4 ) 3 BO 3
3 .滴定
(NH 4 ) 3 BO 3 +3HCl—→3NH 4 Cl+H 3 BO 3
以上测定为样品中的总氮量,由总氮量减去非蛋白氮,即为蛋白质含氮量,再乘以 6 . 25 即为血清蛋白质含量。
【器材】
1 .电炉
2 .铁三角架
3 .酒精灯
4 .锥形瓶
5 .消化管(凯氏烧瓶)
6 .滴定管
7 .微量凯氏定氮器
8 .刻度吸量管
9 .玻璃珠
10 .漏斗
11 .血清
【试剂】
1 .硫酸钾粉末
2 . 12 . 5 %硫酸铜水溶液
3 .浓硫酸
4 . 2 %硼酸水溶液
5 .混合指示剂
取 0 . 1 %溴甲酚绿乙醇溶液 10ml 与 0 . 1 %甲基红乙醇溶液 4ml 混合
6 . 30 %氢氧化钠溶液
7 . 0 . 0lmol / L 盐酸标准溶液
【操作】
一、消化
取消化管二支,标明测定管与空白管,按下表进行操作:
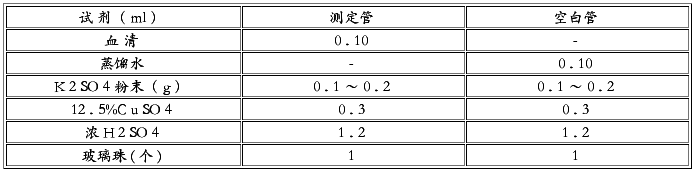
混匀,置于电炉上加热消化(图 3-1 ),开始有水蒸气逸出,继而溶液呈现棕色并冒出白烟 (SO 3 ) ,此时火力应减小,并在管口上盖一小漏斗,以免硫酸损失过多,再继续消化至溶液变为澄清的蓝绿色,即消化完毕 ( 此过程约需 25 分钟左右 ) ,冷却后加水 3 . 8ml ,使总量成为 5ml( 内有 1 . 2ml 硫酸 ) ,混匀,准备蒸馏。

图 3-1 消化装置示意图
二、蒸馏
1 .蒸馏器的结构和用法
蒸馏器有多种,但大同小异。用前需熟悉其使用方法。本实验所用蒸馏器如图 3-2 所示:

图 3-2 微量凯氏定氮器结构示意图
P 1 为出水开关, P 2 为入水开关, A 为蒸气发生室, B 为蒸馏室,与出气管 M 相通。 B 室内有 Y 形管,一端与 A 室相通,另一端经 P 3 与漏斗 D 相连,经此可将样品和试剂加入 B 室, E 为进水管,接水龙头, F 为指形冷凝管, H 为盛有定量硼酸溶液的锥形瓶,以吸收氨。水经 E 、 F 、 G 、 K 而流出,蒸馏时 B 室加入消化好的样品及氢氧化钠,二者反应产生氨, A 室因加热而产生的水蒸气经 Y 管进入 B 室,并将氨一起带出,经冷凝由 M 管进入锥形瓶中被酸吸收。
将洗干净的微量凯氏定氮器安装妥当,把 E 管接水龙头,并关闭 P 1 、 P 2 、 P 3 各塞,打开水源,水则由 E→F→G→K 缓缓流出 ( 水不宜开的过大,以免水从 G 管溢出 ) 。放开 P 2 ,水流入 A 室,并让少量水流入 B 室,然后塞住管口 G ,放开 P 1 ,此时 B 室内水应被吸出,否则应检查各接头处是否漏气。
2 .蒸馏
( 1 ) 打开水笼头和 P 2 ,使水经 E→F→G→P 2 进入 A 室,水约至瓶下球形部分的 2 / 3 处,即关闭 P 2 。
( 2 ) 吸取 2 %硼酸溶液 l0ml ,放人 l00ml 锥形瓶中,加混合指示剂 3 滴 ( 呈灰紫色 ) ,把锥形瓶置于 M 管下,并使管口完全进入硼酸溶液中。
( 3 ) 打开 P 3 ,吸取消化好的样品溶液 2ml ,由漏斗 D 加入蒸馏室 B 中,用 lml 蒸馏水冲洗漏斗,再加入 30 %氢氧化钠溶液 5ml ,立即将 P 3 夹紧 ( 可在漏斗中加少量水封闭,以防漏气。
( 4 ) 用酒精灯加热 A 室,火焰应稳定,以免锥形瓶中的溶液倒吸,待硼酸溶液变为蓝绿色后再继续蒸馏 5min 。
( 5 ) 将锥形瓶下移,使 M 管离开硼酸液面,再继续蒸馏 1 分钟,最后用蒸馏水 1ml 冲洗 M 管外壁,取下锥形瓶进行滴定。
( 6 ) 蒸馏完后应立即清洗蒸馏器,其方法是先打开 P 2 ,将 A 室的水充至球形上方,然后塞住 G 口,放开 P l , B 室内溶液即被吸出,然后再经 D 加蒸馏水入 B 室,如上所述吸出 B 室的水。如此反复洗涤 2 ~ 3 次。
( 7 ) 空白管溶液也同样进行蒸馏。
三.滴定
用 0 . 01mol/L 的盐酸滴定锥形瓶中收集液,使其由蓝色变为灰紫色 ( 蒸馏前硼酸的颜色 ) ,即为终点,记录滴定所消耗盐酸的数量。
【计算】
1 . 
式中, A 表示滴定样品用 0 . 01mol / L 盐酸的 ml 数; B 表示滴定空白用 0 . 01mol / L 盐酸的 ml 数; 0.14 表示 1ml 0 . 01mol / L 盐酸 相当于 氮的毫克数。
2 . 血清蛋白质含量( g/L ) = 
式中, NPN 表示 非蛋白氮 , 即制备样品无蛋白滤液中的氮。
【注意事项】
一、样品消化注意事项
1 .加入样品不要沾附在凯氏烧瓶瓶颈。
2 .消化开始时不要用强火,要控制好热源,并注意不时转动凯氏烧瓶,以便利用冷凝酸液将附在瓶壁上的固体残渣洗下并促进其消化完全。
3 .样品中若含脂肪或糖较多,在消化前应加入少量辛醇或液体石蜡或硅油作消泡剂,以防消化过程中产生大量泡沫。
4 .消化完全后要冷至室温才能稀释或定容。所用试剂溶液应用无氨蒸馏水配制。
二、蒸馏注意事项
1 .进行蒸馏前必须熟悉仪器特点, P 1 打开 A 室水流出; P 2 打开 G 管水流入; P 3 打开漏斗 D 液体流入 B 室。蒸馏开始后, P 1 、 P 2 、 P 3 均需关闭,定氮处于密闭状态,切不可随意开启。
2 .下列因素可导致 B 室液体压入 A 室,同时锥形瓶中的硼酸也可能倒吸入 B 室,导致定氮的失败。
( 1 ) 蒸馏时 P 3 打开, B 室压力增高。
( 2 ) 蒸馏时酒精灯移开,或火焰时断时续,时大时小, A 室遇冷,压力降低。
( 3 ) 蒸馏时 P 2 打开,水至 G 管流入 A 室, A 室遇冷压力降低。
3 .进行蒸馏前必须用水蒸气充分洗涤蒸馏器,以消除可能残存的氨。方法是于 M 管下放一盛有硼酸加指示剂的锥形瓶,若经蒸馏,锥形瓶内颜色不变,即证明蒸馏器内部已经洗涤干净,无氨残留。
4 .实验室环境忌有碱性雾气,否则影响实验结果。
5 .溴甲酚绿 - 甲基红指示剂的变色点为 pH5 . 1 ,大于 5 . 1 呈绿色,硼酸加指示剂应为灰紫色,若呈红色,说明硼酸酸性过强,可用 0 . 1mol / L 氢氧化钠调整。另外所用仪器不净也会出现红色。
6 .本法极为灵敏,因此应避免外界氨的干扰,所用试剂及蒸馏水必须无氨。
7 .一般在操作时,应先蒸馏空白管,然后再蒸馏样品管。
8 .每次蒸馏完毕,应立即清洗蒸馏器,否则冷却后,清洗困难。
【思考题】
1 . 消化是否完全与测定结果有何关系?
2 . 实验室的碱性雾气如何影响实验结果?
