水杨酸甲酯的制备
魏 爽
安志鹏
摘要:为了探究催化剂的用量对制备水杨酸甲酯的量是否有影响?有什么影响?我们进行了水杨酸甲酯的制备实验。实验涉及到由羧酸和醇制备酯的反应原理和实验操作以及减压蒸馏的原理和操作。在进行实验探究的同时,我们也能进一步熟悉某些有机反应的基本实验操作。本次实验以浓硫酸的用量为唯一变量,共进行了四次实验。用2.8g(0.02mol)水杨酸和12.2ml(0.30mol)甲醇,再分别用2.4ml、2.8ml、3.2ml、3.6ml浓硫酸作催化剂来进行实验。经过一系列的反应和后处理,最终实验制得水杨酸甲酯的量依次为:1.15g、1.65g、2.08g、1.87g。实验结果表明:催化剂的量对制备水杨酸甲酯的量存在影响,并且在水杨酸和甲醇的量为上述数据时,用3.2ml的浓硫酸作催化剂制得的水杨酸甲酯的量是最高的。
关键词:水杨酸甲酯;减压蒸馏;水杨酸;催化剂
1. 前言
1.1水杨酸甲酯:俗名冬青油,又名柳酸甲酯,是无色且有香味的液体,沸点220~222℃,易溶于异辛烷、乙醚等有机溶剂,微溶于水。放置在空气中易变色,在酸、碱条件下易水解。现被广泛的应用在精细品化工中做溶剂、防腐剂、固定液,也用作饮料、食品.
1.2性质
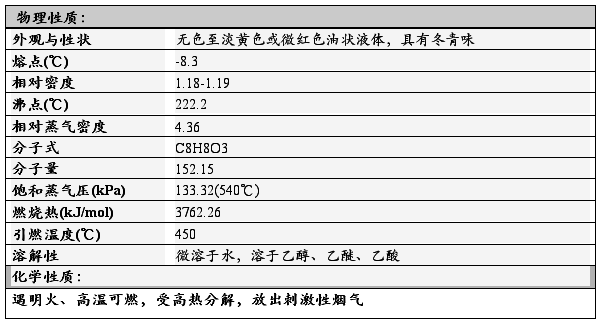
2. 正文
2.1 实验部分
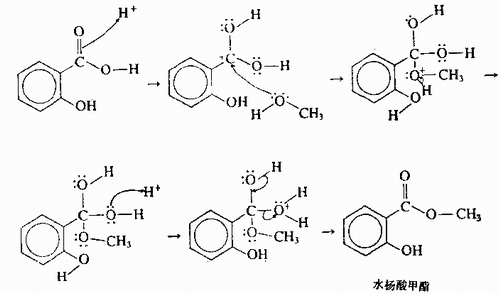
2.1.1反应机理
2.1.2仪器和药品
仪器
球形冷凝管 直形冷凝管 减压蒸馏装置 量筒(10ml,50ml) 锥形瓶 分液漏斗 三口烧瓶 圆底烧瓶 温度计 烧杯 带分水功能的回流装置 克氏蒸馏头
药品
水杨酸(分析纯) 甲醇 浓硫酸 5%碳酸氢钠溶液 饱和食盐水
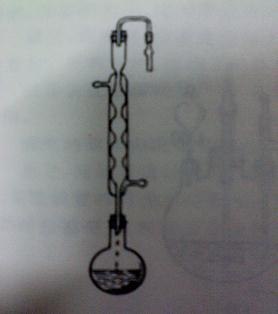
2.1.3实验装置图
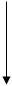

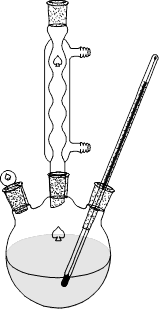
 后接真空泵
后接真空泵
2.1.4后处理装置图

2.1.5反应方程式
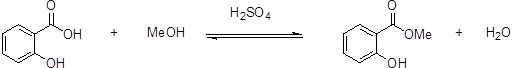
2.1.6实验步骤
(1)三口烧瓶中放入2.8g水杨酸和12.2ml甲醇,再缓慢倒入2.4ml的浓硫酸(余下的三个实验分别加入2.8ml、3.2ml、3.6ml浓硫酸),接上温度计,球形冷凝管,加热回流一个小时四十分钟。
(2)反应完毕,将烧瓶冷却,把液体倒入分液漏斗里,加入饱和食盐水洗净,再加入水,充分震荡,进行分液。
(3)用圆底烧瓶和克氏蒸馏头连接好减压蒸馏装置,接上水泵,进行减压分馏,收集纯净的水杨酸甲酯成分。称重,计算产率。
2.2 数据处理、结果
表1
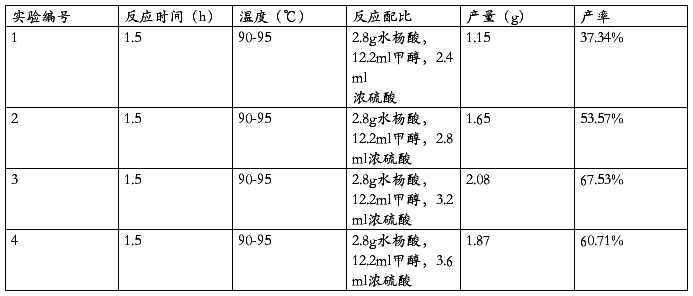
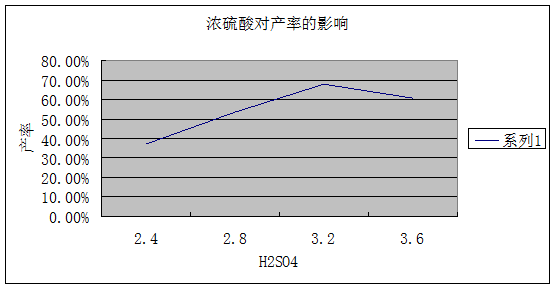
图1
2.3 注意事项
(1)反应仪器一定要干燥,否则会降低冬青油的产率。
(2)实验中一定要将浓硫酸加入其它液体中,不能加反。
(3)反应温度一定要控制在90℃左右,不能太高,否则生产的酯容易分解,降低产率。
(4)减压蒸馏时全部仪器接头都应该涂上甘油。
2.4 结果与讨论
2.4.1结果
由表格可以看出,浓硫酸的用量对反应产率影响很大,随着硫酸用量的增加,产量先上升后下降,其中3.2ml的硫酸实验中,产率最高。由此分析,可能的原因就是:浓硫酸较少时,脱水不完全,产率就低了。而当浓硫酸过量时,速率固然提高了,但是副反应也会增加,例如氧化反应等。除了浓硫酸的用量以外,在做实验的过程中,还可能存在其他影响产率的因素,比如硫酸的加入方法不正确,或加热温度过高这些都会使有机物分解甚至炭化,进而影响产率。
2.4.2 讨论
通过这几次的实验,我们认为不只浓硫酸的用量对实验的产率有重大的影响,温度和反应时间的影响也不容忽视。虽然实验中我们一直在努力进来把温度控制在92℃,但是毕竟不会做得那么完美,这四次的实验在温度方面还是存在一些小的不同。如果实验的仪器和条件可以更好一些的话,我想这些问题还是能尽可能的减小。而且,我们认为在实验操作上还可以改进,比如说在减压蒸馏时,由于仪器的原因,压力的读数不是很准确,可以通过改进,接一个水银压力计,使压力读数更准确,这样实验误差会更小。
2.5 思考与总结
通过这几次的实验,我们认识到实验最大的误差还是操作者。有机实验最重要的是做好实验预习,并且一定要专注于实验本身,不能做与实验无关的事情,并且做实验的过程中要专心致志,因为每一个过程,每一个现象都会对实验的成败起着决定性的作用。当我们能克服急躁心理时,做实验就会变成一件非常有意义的事情,当看到有机产品在我们的努力下慢慢的流出来时,那是一种成就感和满足感。
参考文献
[1]姜艳,韩国防.有机化学实验(第二版).化学工业出版社,2010.
[2]张德华,水杨酸甲酯的合成改进.中国科学院上海冶金研究所.2000.
[3]孟长功,亲剪.基础化学实验(第二版),高等教育出版社,2009.
第二篇:水杨酸甲酯的制备
水杨酸甲酯的制备
11化学本科(1)班 姓名:韦世菊 张小方 冯照艳 康国娇 赵继奖 王教帅
一、实验目的
1、学习在酸催化下用有机酸与醇反应制备酯的原理和方法;
2、掌握有机回流、蒸馏的原理和方法。
3、掌握有机分液的原理和操作。
二、实验原理
水杨酸甲酯可由水杨酸和甲醇在浓硫酸催化下制得。
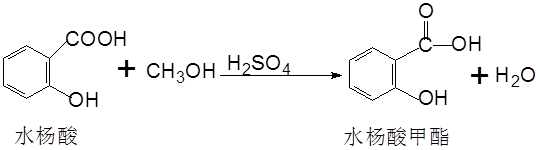
三、仪器与试剂
1、仪器:
圆底烧瓶、蒸馏头、蒸馏柱、分液漏斗、直形冷凝管、烧杯、温度计、接引管、三角烧瓶、量筒、电热套
2、试剂:
水杨酸;甲醇;10%碳酸钠10mL;(6mL,0.1mol);浓H2SO4,无水硫酸镁。
四、实验步骤
1、实验装置如图所示
反应装置图
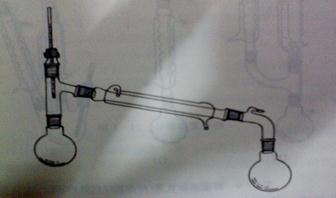
蒸馏装置
除杂装置
2、在干燥的100mL圆底烧瓶中加入3.5g(0.025moL)的水杨酸和15mL(0.37moL)甲醇,然后边摇动边缓缓加入1mL浓H2SO4摇匀,投入几粒沸石,如图接好装置,向冷凝管中通水水浴加热,在85~95摄氏度下加热回流1.5h,反应完将回流装置改为蒸馏装置,水浴加热,蒸去多余的甲醇。
待瓶中剩余的反液冷却后倒入分液漏斗,加入10mL水振荡后静置分层,分去水层。有机层依次用10mL水、10mL10%碳酸钠溶液洗涤,然后用水洗涤数次,直至呈中性。将分出的有机层(粗产品)倒入一干燥的小锥形瓶中,用无水硫酸镁干燥,直至液体澄清。干燥后的液体过滤至干燥的100mL蒸馏瓶中,加入沸石,安装好装置,电热套加热,收集221摄氏度至224摄氏度的馏分。称量产品质量,计算产率。
五、实验注意事项与关键
1、反应过程温度不可过高,否则生成的酯容易分解,影响产率;
2、反应所用仪器一定要干燥,容器中若有水会加长反应时间,影响水杨酸甲酯的产率。
3、蒸馏装置中,温度计水银球上缘恰与蒸馏头支管口下缘水平。
4、加热时,要在圆底烧瓶中加入3~4粒沸石。
5、如蒸馏途中停止,而后来又需要继续蒸馏,也必须在加热补添新的止暴剂,以免出现暴沸。
6、用碳酸氢钠溶液洗涤时,会有二氧化碳气体逸出,应不时地倾斜漏斗打开活塞放出气体。
7、避免明火加热,因为甲醇为低沸点易燃物品。
六、问题:
a) 酯化反应有哪些特点,本实验中如何提高产品产率,
b) 粗产品中含有哪些杂质?如何将它们除去?
c) 甲醇为什么要过量?
