洗涤剂中大肠菌群检测方法探讨与分析
摘要:大肠菌群是洗涤剂产品关键的卫生指标,表明产品被粪便污染的程度。本文对洗涤剂样品中大肠菌群按三种不同的检测方法进行检测,分析讨论不同检测方法对结果的影响。
关键词:大肠菌群 洗涤剂 检测方法
1、前言
大肠菌群是一类需氧及间性厌氧菌,在37℃能分解乳糖产酸产气的革兰氏阴性无芽胞杆菌。食品或洗涤剂中大肠菌群数的高低,表明物品被粪便污染的程度,也反映对人体健康危害性的大小。粪便是人类肠道的排泄物,粪便中除含有正常细菌外,也可能含有肠道致病菌(如沙门氏菌、志贺氏菌等)。因此食品或者洗涤剂如被粪便污染,则有被肠道致病菌污染的可能性,即潜伏着引起人类食物中毒和流行病的威胁。当前,洗涤剂中大肠菌群的最新检验标准是《食品安全国家标准 食品微生物学检验 大肠菌群计数》GB/T4789.3-2010,但洗涤剂卫生标准为《食品工具、设备用洗涤剂卫生标准》GB14930.1-1994,前者单位是“MPN/g(mL)” 或“CFU/g(mL)”,后者单位是“个/100g”,如果洗涤剂按GB/T4789.3-2010标准检测将无法对结果进行判定。同时根据卫生部《关于规范食品中大肠菌群指标的检测工作的公告》(20##年 第16号)规定,现行食品标准中规定的大肠菌群指标以“MPN/100克或MPN/100毫升”为单位的,适用《食品卫生微生物学检验 大肠菌群测定》GB/T4789.3-2003进行检测。另外考虑到洗涤剂本身是一种化学产品,实验过程中可能产生化学反应而影响发酵管中产气的结果判断,我们对一组大肠菌群超标的抽检样品分别用三种不同检测方法进行验证并分析讨论,其中后两种方法是平板计数法避免了产酸产气对结果的影响。三种检测方法分别是:《大肠菌群MPN计数法》GB/T4789.3-20##、《大肠菌群PetrifilmTM测试片法》GB/T4789.3-2008和《大肠菌群平板计数法》GB/T4789.3-2010。
2、 实验部分
2.1实验设备及材料
恒温培养箱 恒温水浴锅 天平 振荡器
菌落计数器 显微镜 无菌吸管(1 mL) 无菌锥形瓶
无菌培养皿 灭菌试管 高压灭菌锅
乳糖胆盐发酵管 伊红美蓝琼脂平板 乳糖发酵管
结晶紫中性红胆盐琼脂(Violet Red Bile Agar,VRBA)
煌绿乳糖胆盐(Brilliant Green Lactose Bile,BGLB)肉汤
革兰氏染色液 无菌生理盐水0.85% 无菌1 mol/L NaOH
无菌1 mol/L HCl 大肠菌群PetrifilmTM测试片
2.2检测样品
抽检某公司洗涤剂样品
2.3检测方法
样品的稀释:称取25 g 样品,放入盛有225 mL生理盐水的无菌锥形瓶(瓶内预置适当数量的无菌玻璃珠)中,用振荡器充分混匀,制成1:10 的样品匀液。用1 mL无菌吸管吸取1:10样品匀液1 mL,沿管壁缓缓注入9 mL生理盐水的无菌试管中(注意吸管尖端不要触及稀释液面),使其混合均匀,制成1:100的样品匀液。按上述操作,依次制成1:1000,1:10000的样品匀液
2.3.1大肠菌群MPN计数法:检测步骤按GB/T4789.3-2003标准中大肠菌群MPN计数法进行。
2.3.2大肠菌群PetrifilmTM测试片法:检测步骤按GB/T4789.3-2008标准中大肠菌群PetrifilmTM测试片法进行。
2.3.3大肠菌群平板计数法:检测步骤按GB/T4789.3-2010标准中大肠菌群平板计数法进行。
3、 结果与讨论
3.1检测结果
3.1.1大肠菌群(MPN计数法)
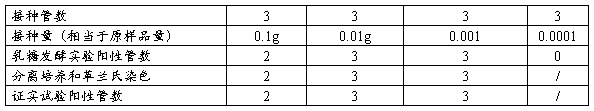
根据证实实验阳性管数,查MPN表,大肠菌群结果:5.3×103个/100g
3.1.2大肠菌群(PetrifilmTM测试片法)

大肠菌群检测结果:2.8×105CFU/g
3.1.3大肠菌群(平板计数法)

大肠菌群检测结果:19×(8/10)×104= 1.5×105CFU/g
3.2讨论与分析
3.2.1大肠菌群三种检测方法的结果分别为5.3×103个/100g、2.8×105CFU/g、1.5×105CFU/g,三种检测方法的结果都表明该洗涤剂产品大肠菌群严重超标,避免了洗涤剂中可能存在的化学反应造成发酵管产气而对结果判定的影响.其中三种检测方法的结果存在一定相关性,“MPN计数法”与“PetrifilmTM测试片法”和“平板计数法”单位不一致无法直接比较,“PetrifilmTM测试片法”和“平板计数法”两种方法检测的结果在一个数量级上。
3.2.2分析此样品中大肠菌群超标原因,可能是洗涤剂生产用水受到粪便污染,生产工艺环节没有得到有效控制,产品受到严重污染。因此洗涤剂生产者要严格检测生产用水,保证生产用水不能受到粪便污染,对生产用水以及生产环境采取有效杀菌方法,应从进入配料罐的管道口处定期取样测定,以考察各原料储罐及输送管道的情况。若有发现微生物超标,应及时检查原因并进行相关的分析改进。同时产品要加品质好的防腐剂,防腐剂具体的用量要结合需要的保质期、防腐剂的含量、水质的干净程度、生产工具与包装物的清洁程度、四季气候的变化等各种因素来综合确定。
3.2.3洗涤剂卫生标准为《食品工具、设备用洗涤剂卫生标准》GB14930.1-1994 ,而大肠菌群最新的检测标准是《食品安全国家标准 食品微生物学检验 大肠菌群计数》GB/T4789.3-2010,由于结果单位表示的不同以及根据卫生部《关于规范食品中大肠菌群指标的检测工作的公告》(20##年 第16号)规定,洗涤剂中大肠菌群检测只能用GB/T4789.3-2003 ,GB/T4789.3-2010与GB/T4789.3-2003相比,最主要的差别为初发酵试剂不同。GB/T4789.3-2010为月桂基硫酸盐胰蛋白胨,GB/T4789.3-2003为乳糖胆盐。月桂基与乳糖胆盐相比,稳定性好、可抑制革兰氏阳性菌增长、对损伤的大肠菌群有修复作用。GB/T4789.3-2010提高了灵敏度和检测率。而GB14930.1-1994如今还是现行的,与最新的大肠菌群检测标准GB/T4789.3-2010不配套。现在急需要相关部门修订洗涤剂卫生标准GB14930.1-1994,研究按照GB/T4789.3-2010的方法检测大肠菌群的技术要求,单位统一到
“MPN/g(mL)” 和“CFU/g(mL)”,更好的规范洗涤剂产品的卫生标准和检测方法。
第二篇:大肠菌群检测方法
大肠菌检测方法
1. 进入无菌室前应打开紫外线灯消毒时间为0.5-1小时。
2. 关灯后0.5小时后方可进入。
3. 进入更衣间更换衣服,佩带口罩、帽子、鞋套
实验步骤
1. 进入无菌室后,先把酒精灯点燃,然后在用酒精棉进行手部消毒。(酒精棉是用75%的酒精加入脱脂棉中制成)
2. 准备双料管3根,单料管6根,培养皿7个。
3. 直接从原液中吸取10ml放入双料管,(3根每根各10ml)
4. 再吸取原液1ml放入单料管中(3根每根各1ml)
5. 再吸取原液1ml放入培养皿中(2个培养皿各1ml)
6. 再吸取原液1ml放入盐水管中制成-1梯度的样液
7. 更换一根吸管,从-1梯度的样液吸取1ml样液放入单料管中(3根每根各1ml)
8. 再吸取-1梯度样液1ml放入培养皿中(2个培养皿各1ml)
9. 再把每个培养皿中倒入营养琼脂平铺底部摇匀(注:另作3个培养皿:空气空白,把培养皿打开10分钟倒入营养琼脂平铺底部摇匀。琼脂空白,把培养皿中倒入营养琼脂平铺底部摇匀。盐水空白,吸1ml生理盐水放入培养皿中倒入营养琼脂平铺底部摇匀。)
10. 把全部做好的放入培养箱中,温度36±1℃,大肠24小时±1小时,菌落48小时±2小时(待培养皿中的琼脂凝固后翻转过来放入培养箱中)
11. 梯度:-1梯度为1ml原液加入9ml生理盐水配成
-2梯度为1ml-1梯度样液加入9ml生理盐水配成
-3梯度-4梯度配制方法和-1、-2的配制方法一样
12.如果大肠初发酵产生气泡,用接种笔沾一个产气的液在伊红美兰平板上画之字形然后放入培养箱中36℃,24±2小时。(接种笔在每次使用前必须在酒精灯上消毒。所画之行不能划破伊红美兰琼脂表面)
13.取出后再用接种笔在伊红美兰平板之字形上挑菌,放入乳糖复发酵管中,然后再培养36±1℃,24±2小时。
14.再在伊红美兰平板之字形上挑菌,放到载玻片上作镜检。(方法见标准)
15.只有镜检成紫红色和乳糖复发酵管产气同时成立的情况下,才能断定这根管是不合格。
16.清洗消毒这根管前必须进行消毒霉菌,121℃,0.5小时同时不能放气。
祝你成功的十条忠告
1、买个闹钟,以便按时叫醒你。贪睡和不守时,将成为你工作上的绊脚石,任何时候都一样。不仅要学会准时,更要学会提前。就如你去某地却不是准时到达。“闹钟”只是一种简单的标志和提示,真正灵活、实用的时间,掌握在每个人的心中。
