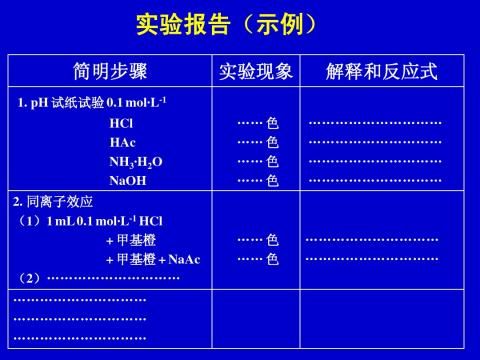
无机实验报告
实验九 氧化还原与电化学
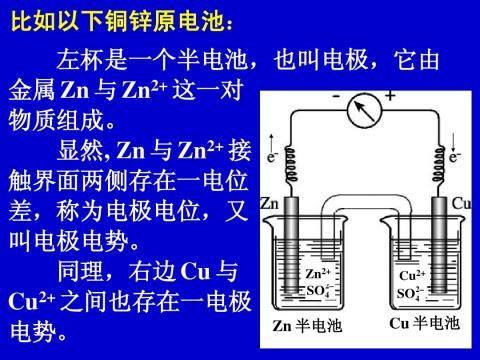
一、电极电势与氧化还原反应方向

结论: (MnO4/ Mn2+)
(MnO4/ Mn2+)  (Fe3/Fe2+)
(Fe3/Fe2+)  (I2/I-)
(I2/I-)  (Sn4+/ Sn2+)
(Sn4+/ Sn2+)
查表:
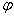 °(MnO4/Mn2+)= ,
°(MnO4/Mn2+)= , °(Fe3+/Fe2+)= ,
°(Fe3+/Fe2+)= , °(I2/I-) ,
°(I2/I-) ,
 °(Sn4+/Sn2+)= 。与上述实验所得 ,所以氧还方向为 。
°(Sn4+/Sn2+)= 。与上述实验所得 ,所以氧还方向为 。
二酸度对氧化还原反应的影响

结论:(1)C[H+]增大, (MnO2/Mn2+)及
(MnO2/Mn2+)及 (Cr2O72-/Cr3+)值 。
(Cr2O72-/Cr3+)值 。
(2)C[HCl]增大, (C12/C1-)值 ,所以,反应 。
(C12/C1-)值 ,所以,反应 。
三、影响氧化还原反应的其它因素
1、浓度的影响
FeC13+FeSO4+K1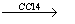 (CC14层 色)
(CC14层 色)
FeC13+K1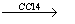 (CC14层 色)
(CC14层 色)
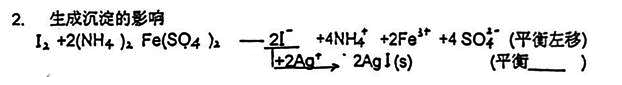
3、生成配合物的影响
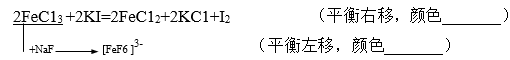
结论:
(1)反应1(稀释),3(生成配合物),使电对Fe3+/Fe2+中[Fe3+]降低,从而使反应难进行,即 (Fe3/Fe2+)下降了,Fe3+氧化性减弱。
(Fe3/Fe2+)下降了,Fe3+氧化性减弱。
(2)反应2(生成沉淀),使电对I2/I-中[I-]降低,  (I2/I-)值升高。
(I2/I-)值升高。
四、介值(碱)度对氧化还原反应的影响

五、酸度对氧-还反应速率的影响

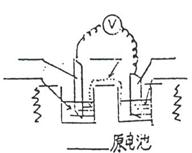
六、原电池
1、简易原电池的构成和电极电势的比较
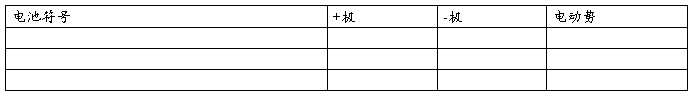
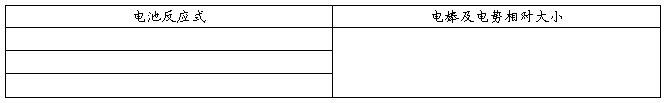
上述原电池中,各电极的反应式为:
原电池:负极反应 。
正极反应 。
原电池:负极反应 。
正极反应 。
原电池:负极反应 。
正极反应 。
2、浓度对电极电势的影响
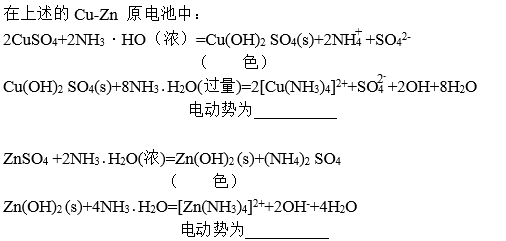
结论:电极电势随离子浓度改变而 ,在原电池中,正极离子浓度降低,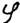 值 ,负极离子浓度降低,其
值 ,负极离子浓度降低,其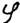 值 ,前者使电动势 ,后者使电动势 。
值 ,前者使电动势 ,后者使电动势 。
3、介质酸(碱)度对电极电势的影响
电池反应:

七、电解

专业 班,姓名 学号 评分
第二篇:实验十三 氧化还原反应与电化学