类别: 编号:
部门:固体口服制剂车间 页数:
V 混机总混均匀性工艺验证方案
起 草: 年 月 日
审核会签:
质 量 部
生产技术部
工程技术部
批 准: 年 月 日
实施计划:从 年 月 日到 年 月 日
编订人: 编订日期:
目 录
一.目的...........................................................................................................................
二.范围...........................................................................................................................
三.责任...........................................................................................................................
四.编制依据
五.方案...........................................................................................................................
1. 验证程序
2.生产工艺流程及说明
3.验证必备条件
4.验证方法:
5.操作步骤
6.成品检测
7.方案偏差分析
8. 批生产记录
9. 再验证
V型混合机混合均匀性的验证方案
1.目的
我公司固体口服制剂车间所用的V型混合机设备容量为每锅为360kg,因V混合机的容量过小,给生产和检验带来很大工作量,现制定方案在颗粒混合对将三批进行总混后,对其含量、水分、均匀度进行检测,以确认混合的均匀性是否达到要求,确保设定工艺在现有设备条件下能够生产出质量稳定、符合质量标准的产品。
2.范围
此次验证包括9个批次多维元素片的总混,每批360kg,采用主要设备请详见设备/系统描述,按照《规范》要求提供验证用的MO、MD 连续生产9个批次,并按取样计划进行取样、监测,按经验证的质量标准、分析方法进行测定。验证完毕,根据实际情况对MD 相关参数进行确认和必要的调整。
3.缩写和定义
MO :生产卡
MD :生产操作规程(批记录)
RSD :相对标准偏差
ChP :中华人民共和国药典
rpm :每分钟转速
4.验证小组职责分工(表4-1)
表4-1 职责分工

批准人: 批准日期: 年 月 日
5.产品处方
按处方列出每片、每千片所用主药(活性成分)、辅料、包衣材料的用量或百分比(%)。素片或包衣片应标明每片的理论重量。
6.工艺简介
主料及辅料按MD 要求进行粉碎或过筛后进行备料,使用混合制粒机湿法制粒,湿制粒在流化干燥机中干燥,干颗粒整粒后加入干掺崩解剂和润滑剂在专用混合桶中总混合,用高速旋转式压片机压片,在薄膜包衣锅中包衣,在 包装线上进行包装。
7.工艺流程图请参考片剂生产工艺流程图
7-1.生产工艺流程示意图及区域划分



注: 为300000洁净区。
8.工艺:考察计划和验证合格标准
(1)对原辅料进行备料前监控质量管理部门需对原辅料逐一进行检(化)验,合格
后方可放行,验证小组相关人员须复核化验报告单(表7),包括供应商、包装情况、
有效期
表7 化验报告单
(2)备料 主要对粉碎机粉碎效果的观察。
①试验条件的设计:速度、筛目大小及型号、刀的方向,每次至少取 个样品。
②评估项目:粒度及粒度分布、松密度。
③按MD规定条件粉碎,质量应符合要求。
(3)制粒
①试验条件的设计:搅拌条件及时间、干燥温度及时间、结合剂浓度及用量每次至少取 个样品。
②评估项目:水分、筛目分析、松密度。
③按MD规定参数制粒,质量应符合要求,如需调整,需做好记录。
(4)总混合
①试验条件的设计:多维元素片产品规定混合时间为10min,每三批为一组,此次验证共5组成5批。1、2、3批按规定时间和工艺参数进行总混,混合后每次根据设备情况设置5个点,取样检测。三批总混后分三次各取1/3在V混机按规定工艺参数进行总混,共混3次,混合后每次根据设备情况设置5个点,再取样检测。先算5个点均值,再算组间的偏差,偏差±3%为验证合格。检验以
②评估项目:含量、均匀度、水分。
③检查粒度分析、松密度,不同颜色组分的产品须检查色泽均匀度。
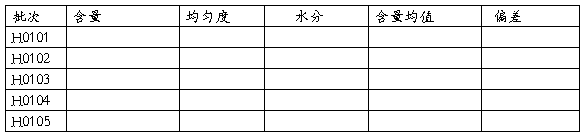
组间偏差
(5)压片
①按岗位SOP规定确定适当的转速、压力后,按规定取样。
②评估项目:外观、片重差异、硬度、溶出度、含量、检查厚度、脆碎度按MD参数压片适应包衣要求并符合中控质量标准。
(6)包衣
①试验条件的设计:锅速、进风/排风温度、喷射速率、喷雾粒度、直径、包衣液浓度、用量,每次按规定取样。
②评估项目:外观、片重、片重差异、溶出度(崩解度)。按MD参数包衣,应符合质量标准要求。
(8)包装
①实验条件的设计:运行速度、热封温度参数、热材压力(或热合轴间隙)设定每15min取样一次,直至300min。
②评估项目:外观、渗漏试验。
③按包装操作规程(Packaging Direction ,PKD)操作,质量应符合相关SOP要求。具体接收标准应根据产品质量标准、中控标准判断。样品中允许的相对标准偏差(即变异系数)根据品种和项目而定,如含量的相对标准偏差(即RSD值)一般为2%,但含量大小不同亦可酌情变动。目的是保证产品质量的安全可靠。
9.取样计划和记录
(1)取样计划 ①取样时间;②取样点;③取样量;④取样容器;⑤取样编号。
(2)设计取样记录表格举例如表,供参考。
第二篇:2-V1.0型型混合机验证方案
北京瑞先农科技发展有限公司GMP管理文件

1.概述
该机由无锡市荣伟制药机械厂生产,是国际上较为通用的干粉、干颗粒混合机,它具有结构简单、操作容易、维护清洗方便、速度快、混合效果极佳等特点。广泛应用于制药、化工、食品、电子、冶金、塑料、建材、耐火材料等行业。
1.1本机有以下几个特点:
—所用材质、设计、制造均符合GMP要求。
—设备的操作控制系统操作方便、显示准确。
—本设备与药物接触的部位的材料符合GMP要求,为不锈钢材质,并加工表面光洁、平整、易清洗。
—本设备运行稳定便于操作、维护保养。
—本设备设有控制系统,可保证设备的正常运行。
1.2主要技术参数

2.验证对象:
适用于混合机的验证。
3.验证小组成员:组 长: 王 鹏
成 员: 纪红梅 张士鑫 张树华 王海月
4.验证目的:
通过对混合机和真空泵设备的安装、运行、性能的确认,作出该设备能适应工艺的评估。
5.验证内容:
5.1安装确认
5.1.1文件资料确认 符合要求
5.1.2设备材质确认 符合要求
5.1.3检查并确认设备外观无缺陷和损坏
5.1.4检查并确认设备安装水平、稳固
5.1.5检查并确认主电源与控制的连接正确
5.1.6检查并确认控制柜与控制仪表的连接正确
5.1.7检查并确认可拆卸的工作部件易于拆卸、装配
5.1.8检查并确认混合机安装位置符合设计要求
5.1.10公用工程的安装确认
5.1.10.1配电 符合要求
※ 检查穿墙电缆套管与彩钢板间缝隙是否密封良好。
5.1.11仪器仪表的校正 符合要求
5.2运行确认:按照《混合机操作SOP》进行操作。
5.2.1验证目的
在通电的情况下,检查所有的管路和控制点是否与工艺流程相符,检查各容器、管件的密封情况和设备运行工况符合设计要求,无泄露现象。
5.2.2验证判定标准
5.2.2.1可实现系统的操作控制,控制系统能正常工作。
5.2.2.2设备运行平稳,无异常震动、噪音。噪音≤65dB
5.2.2.4各项技术参数符合设计要求。
5.2.2.5按照厂商提供的操作说明书每步操作均运行正常。
5.2.3验证程序
5.2.3.1清洗擦抹干混合机的脏物和灰尘,检查并确认已清洗干净。
5.2.3.2检查配电连接正确。
5.2.3.3检查主机的机架连接牢固并确认无松动。
5.2.3.4检查并确认混合机主机按规定方向运转平稳,无异常振动。
5.2.3.5检查并确认控制系统的功能符合设计要求。
5.2.3.6检查并确认管道连接处无泄露。
5.2.3.7检查并确认机器的周边空间能满足生产、维修的要求。
5.3性能确认
5.3.1验证目的
在安装确认和运行确认的前提下,通过物料混和工艺验证,以提供足够的数据和文件依据,混和工艺所制定的工艺条件能够保证生产的可靠性和重现性,即所认定的混合时间能够确保物料混合的均匀度,所混合物料能够保证质量的要求。
5.3.2验证判定标准
附件1 运行确认记录

检验人: 复核人 日期:20##年 月 日
附件2 性能确认记录表

检验人: 复核人 日期:20##年 月 日
附件3 重现性试验记录表

检验人: 复核人 日期:20##年 月 日
5.4异常情况处理程序:若出现个别检测项目不合格,应重新进行检测并分析原因。若属于自身原因,应上报验证委员会调整设备运行参数或对其进行处理。
5.5验证结果评价与结论:验证小组根据设备确认情况,作出相应评定及结论。
6、再验证周期:验证小组根据设备确认运行情况,拟订再验证周期报验证委员会审批。
7、验证进度安排:验证小组于20##年验证对三维运动混合机进行验证。
