实验九 电位滴定法测定酱油中氨基酸态氮的含量
一、实验原理
根据氨基酸的两性作用,加入甲醛以固定氨基的碱性,使羧基显示出酸性,将酸度计的玻璃电极及甘汞电极(或复合电极)插入被测液中构成电池,用碱液滴定,根据酸度计指示的pH值判断和控制滴定终点。
二、仪器与试剂
1、仪器 酸度计 磁力搅拌器 烧杯(250mL) 微量滴定管
2、试剂 pH=6.18标准缓冲溶液;20%中性甲醛溶液;0.05mol/L左右的NaOH标准溶液
三、实验操作方法
(1)样品处理
先根据实验四测出待测酱油的比重,然后吸取酱油5.00mL于100mL容量瓶中,加水定容。吸取定容液20.00mL于250mL烧杯中,加水60mL,放入磁力转子,开动磁力搅拌器使转速适当。用pH6.18的标准缓冲液校正好酸度计,然后将电极清洗干净,再插入到上述酱油液中,用NaOH标准溶液滴定至酸度计指示pH8.2,记下消耗的NaOH溶液体积。
(2)氨基酸的滴定
在上述滴定至pH8.2的溶液中加入10.00mL的中性甲醛溶液,再用NaOH标准溶液滴定至pH9.2,记下消耗的NaOH溶液体积。
(3)空白滴定
吸取80mL蒸馏水于250mL的烧杯中,用NaOH标准溶液滴定至pH8.2,然后加入10.00mL中性甲醛溶液,再用NaOH标准溶液滴定至pH9.2,记下加入甲醛后消耗的NaOH溶液体积。
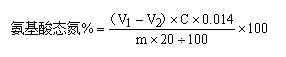
四、 实验计算
式中:
V1——酱油稀释液在加入甲醛后滴定至pH9.2所用NaOH标准溶液的体积mL;
V2——空白滴定在加入甲醛后滴定至pH9.2所用NaOH标准溶液的体积mL
C ——NaOH标准溶液的浓度mol/L
M——吸取的酱油的质量g
0.014——氮的毫摩尔质量g/m mol
第二篇:电位滴定法测定酱油中氨基酸态氮的含量 - 副本
实验九 电位滴定法测定酱油中氨基酸态氮的含量
一、实验原理
根据氨基酸的两性作用,加入甲醛以固定氨基的碱性,使羧基显示出酸性,将酸度计的玻璃电极及甘汞电极(或复合电极)插入被测液中构成电池,用碱液滴定,根据酸度计指示的pH值判断和控制滴定终点。
二、仪器与试剂
1、仪器:电位电动滴定仪 烧杯(250mL) 20ml移液管
2、试剂: pH=6.18标准缓冲溶液,pH=4.00标准缓冲溶液 ,20%中性甲醛溶液;0.1mol/L左右的NaOH标准溶液
三、实验操作方法
(1)清洗和润洗管路
开机,按“F3”清洗键,用蒸馏水清洗3次滴定管路,随后用滴定剂清洗3次滴定管路,使溶液充满整个滴定管道。
(2)PH标定
选择合适的缓冲溶液进行两点标定。
(3)滴定模式选择和参数设置
选择预控滴定模式,设置第一滴定终点为PH8.2,第二滴定终点为PH9.2。
(4)酱油中总酸测定
吸取酱油稀释液10.00ml(酱油稀释5倍) 于250mL烧杯中,加水30mL,放入磁力转子,开动磁力搅拌器使转速适当。选择预控滴定模式,滴定至PH8.2,记录消耗的NaOH体积V1,计算酱油中总酸含量。
(5)氨基酸的滴定
在上述滴定至pH8.2的溶液中加入10.00mL的中性甲醛溶液,再用NaOH标准溶液滴定至pH9.2,记下消耗的NaOH溶液体积V2,计算氨基酸态氮含量。
(6)空白滴定
吸取80mL蒸馏水于250mL的烧杯中,选择空白滴定模式,用NaOH标准溶液滴定至pH8.2,然后加入10.00mL中性甲醛溶液,再用NaOH标准溶液滴定至pH9.2,记下加入甲醛后消耗的NaOH溶液体积V空白。
1
结果表示
酱油中总酸含量以mol/L表示
酱油中氨基酸总量以氨基酸态氮含量表示(g/100g)
对比: 酱油中氨基酸态氮含量的测定-双指示剂甲醛法 实验步骤
1、 移取1份10ml酱油稀释液分别加入250ml锥形瓶中,加入30ml
蒸馏水,其中1份加入3滴中性红指示剂,用NaOH标液滴定至溶液由红色变为琥珀色为终点,记录体积为V1,用于计算酱油中总酸含量。
2、 移取1份10ml酱油稀释液分别加入250ml锥形瓶中,加入30ml
蒸馏水,加入3滴百里酚酞指示剂及中性甲醛溶液10ml,摇匀,静置1min,用NaOH标液滴定至淡蓝色为终点,记录体积为V2,用于计算酱油中氨基酸态氮含量 。
3、 移取10ml蒸馏水加入250ml锥形瓶中,加入30ml蒸馏水,加入
3滴百里酚酞指示剂及中性甲醛溶液10ml,摇匀,静置1min,用NaOH标液滴定至淡蓝色为终点,记录体积为V空白.
2
