本科生实验报告
实验课程 新能源材料设计与制备综合实验
学院名称 材料与化学化工学院
专业名称 新能源材料与器件
学生姓名 蒋 澄
学生学号 201202060121
指导教师 张文涛、张力、罗大伟
实验地点 测试楼519
实验成绩
 二〇##年六月 二〇##年七
二〇##年六月 二〇##年七
填写说明
1、 适用于本科生所有的实验报告(印制实验报告册除外);
2、 专业填写为专业全称,有专业方向的用小括号标明;
3、格式要求:
① 用A4纸双面打印(封面双面打印)或在A4大小纸上用蓝黑色水笔书写。
② 打印排版:正文用宋体小四号,1.5倍行距,页边距采取默认形式(上下2.54cm,左右2.54cm,页眉1.5cm,页脚1.75cm)。字符间距为默认值(缩放100%,间距:标准);页码用小五号字底端居中。
③ 具体要求:
题目(二号黑体居中);
摘要(“摘要”二字用小二号黑体居中,隔行书写摘要的文字部分,小4号宋体);
关键词(隔行顶格书写“关键词”三字,提炼3-5个关键词,用分号隔开,小4号黑体);
正文部分采用三级标题;
第1章 ××(小二号黑体居中,段前0.5行)
1.1 ×××××小三号黑体×××××(段前、段后0.5行)
1.1.1小四号黑体(段前、段后0.5行)
参考文献(黑体小二号居中,段前0.5行),参考文献用五号宋体,参照《参考文献著录规则(GB/T 7714-2005)》。
实验一:锂离子电池正极材料磷酸铁锂的制备
一、 实验目的
了解锂离子电池的工作原理,掌握锂离子电池正极材料在电池中所起的作用,掌握正极材料的一般制备方法。
二、 实验原理
锂离子电池充电过程中,正极活性物质中的部分Li+脱离其晶格进入到电解液中,同时正极提供电子到外电路,然后,Li+通过隔膜嵌入到负极活性物质的层状结构中,同时负极从外电路得到电子生成LixC,这一过程锂离子电池的端电压上升。当电池放电时,LixC中的Li失去电子生成Li+,Li+脱出进入到电解液,通过隔膜嵌入到正极,同时电子通过外电路从负极流向正极,这一过程锂离子电池的端电压下降。正极是锂离子电池的核心部件,正极材料对锂离子电池的性能至关重要。
常规锂离子电池正极材料有层状的过渡金属氧化物LiMO2(M=Co,Ni,Mn等)、尖晶石型的LiM2O2(M=Co,Ni,Mn等)以及橄榄石型的磷酸铁锂(LiFePO4)。钴酸锂(LiCoO2)安全性能差、钴资源的严重缺乏;锰酸锂(LiMnO2)比容量低和高温性能差。
固相合成法是电极材料制备中最为常用的一种方法,也是合成LiFePO4的主要方法之一。固相合成以锂源(如碳酸锂、氢氧化锂、醋酸锂及磷酸锂等)、铁源(如草酸亚铁、醋酸铁、磷酸亚铁等)和磷源(如磷酸氢二铵、磷酸二氢铵、磷酸等)为原料,在保护气氛(氮气、氩气或它们与氢气的混合气体)中经300~400℃加热3~6 h进行预处理,然后在500~800℃煅烧4~24 h可得LiFePO4粉体材料。
液相法合成LiFePO4的主要途径有水热法、溶胶-凝胶法、共沉淀法、氧化-还原法和乳化干燥法等。水热法是以可溶性亚铁盐、锂盐和磷酸盐为原料,在水热条件下直接合成LiFePO4的方法。水热法是在高压釜的高温、高压反应环境中,采用水为反应介质,使得通常难溶或不溶的物质溶解,反应还可以进行重结晶。
。
三、 试剂和材料
仪器:马弗炉、陶瓷坩埚、电磁搅拌器、研钵、电子天平、恒温干燥箱、离心机、真空水泵、布氏漏斗等。
试剂及材料:磷酸二氢铵、硫酸亚铁、氯化亚铁、硝酸锂、葡萄糖、活性碳粉。
四、 实验步骤
4.1 固相反应法合成磷酸铁锂
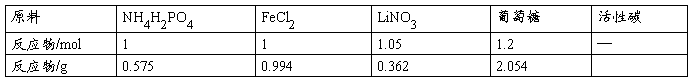
合成反应式:NH4H2PO4+FeCl2+LiNO3=LiFePO4+NH3+HCl+H2O+NO2
1. 药品称量:按照磷酸二氢铵:氯化亚铁:硝酸锂=1:1:x(x=1~1.1)的比例,分别称取0.005mol磷酸二氢铵、氯化亚铁及相应的硝酸锂,分别溶解于10ml蒸馏水中。另外称取适量的葡萄糖,溶解在氯化亚铁溶液中,再将三种溶液在电磁搅拌下混合均匀。
2. 烘干:将混合后的液体在110℃烘箱中烘干,取出在研钵中研磨均匀,放入25ml陶瓷坩埚中。
3. 埋碳:50ml陶瓷坩埚中加入活性碳颗粒,再把25ml陶瓷坩埚放入活性碳中包埋,盖上坩埚盖子。
4. 煅烧:以5℃ /min的升温速率升温至一定温度(700℃~800℃),保温一定时间(4h~10h),随炉冷却后取出样品。观察产物形貌、颜色,称量计算产率。
固相反应法合成LiFePO4的可能影响因素:
(1)硝酸锂摩尔比;
(2)葡萄糖加入量;
(3)煅烧温度;
(4)保温时间。
4.2 水热法合成磷酸铁锂
合成反应式:CO(NH2)2+NH4H2PO4+FeSO4+LiNO3=LiFePO4+NH4NO3+(NH4)2SO4
1. 药品称量:按照尿素:磷酸二氢铵:硫酸亚铁:硝酸锂=1:1:1的比例,分别称取0.005mol磷酸二氢铵、硫酸亚铁、硝酸锂,分别溶解于10ml蒸馏水中。另外称取适量的尿素,溶解在磷酸二氢铵溶液中,再将三种溶液在电磁搅拌下混合均匀。
2. 根据水热反应釜的容积,按照60%~80%的填充比例(即液体占容积的比例)加入蒸馏水,锁好反应釜。
3. 设置水热反应温度为120℃~180℃,反应温度为4h~12h。
水热法合成LiFePO4的可能影响因素:
(1)尿素的摩尔比;
(2)水热反应的填充度;
(3)反应温度;
(4)保温时间。

4.3 产物表征
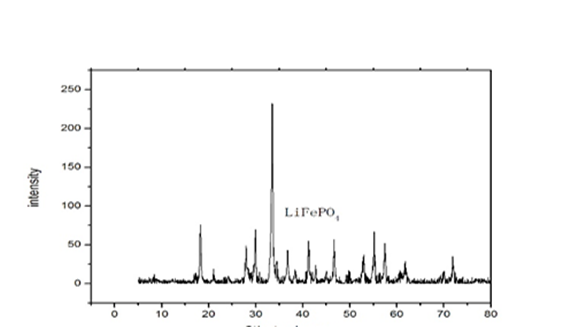
4.3.1 XRD物相分析
烘干粉末做XRD衍射分析,确认产物的物相是否磷酸铁锂,分析原因。
实验二、染料敏化二氧化钛太阳能电池的制备
一.实验目的
1.了解太阳能电池的特点及用途。
2.通过查阅文献,了解太阳能电池的常用制备方法及优缺点。
3.掌握试验方法,自行制备一个或多个二氧化钛太阳能电池。
4.探索影响产物性质的因素
5.可探索不同试验方法得到产物的优缺点
二.染料敏化太阳能电池的原理
(1)染料分子受太阳光照射后由基态跃迁至激发态;
(2)处于激发态的染料分子将电子注入到半导体的导带中;
(3)电子扩散至导带基底,后流入外电路中
(4)处于氧化态的染料被还原态的电解质还原再生
(5)氧化态的电解质在对电极接受电子后被还原,从而完成一个循环。
三.仪器与试剂
试剂:FTO导电玻璃,丙酮,无水乙醇,吐温-100,乙酰丙酮,酞酸丁酯,冰醋酸,二氧化钛,叶绿素,异丙醇,乙二醇,已腈六水合氯铂酸,磷,碘化钾等,均为分析纯。
仪器:超声波清洗器,电热鼓风干燥箱,电子天平,数字万用表,数字式照度计,控温磁力搅拌器,箱式气氛炉,电炉温度控制器。
四.实验步骤
1.导电玻璃清洗
首先用去离子水将导电玻璃表面的灰尘等颗粒冲洗干净,在分别用去离子水、丙酮、乙醇依次超声清洗15min,除去导电玻璃表面的各种有机和无机杂质,洗涤完成后,再用去离子水冲洗2~3次,晾干后保存使用。
2.TiO2薄膜电极的制备
溶胶-凝胶法 量取10ml钛酸丁酯、25ml无水乙醇、3ml冰醋酸,利用磁力搅拌器搅拌0.5h,此溶液称为A;再量取20ml无水乙醇、1ml去离子水,搅拌使之混合均匀,此溶液称为B。随后边对A溶液进行磁力搅拌,边用滴管向A溶液中逐滴加入B溶液,滴加完毕后,再继续搅拌0.5h,得到微黄透明的溶胶液。
3.组装电池
小心地把着色后的电极从溶液中取出,并用水清洗。烘干之前再用乙醇或异丙醇清洗一下,以确保将着色后的多孔TiO2膜中的水份除去。把烘干后的电极的着色膜面朝上放在桌上,再把涂有催化剂的反电极放在上面,把两片玻璃稍微错开,以便于利用未涂有TiO2的电极部分和反电极作为电池的测试用。
4.注入电解质
用两个夹子把电池夹住,再滴入两滴含碘和碘离子的电解质溶液,由于毛细管原理,电解质很快在两个电极间均匀扩散。
五.实验数据


第三章 溶胶-凝胶法制备YAG:Ce3+黄色荧光粉
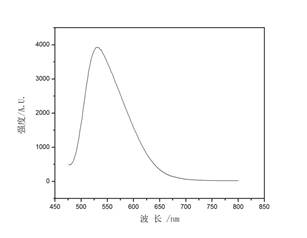
Y3Al5O12(YAG)即钇铝石榴石,是一种非常重要的基质,具有优良的物理、化学和机械特性,且容易实现稀土离子掺杂。稀土掺杂YAG中,掺杂Eu3+、Ce3+、Tb3+的是很好的荧光材料。YAG:Ce3+在460nm附近有较强的宽带吸收,其发射波长在530nm附近,能与蓝色LED芯片组合形成白光。采用InGaN蓝光LED芯片涂覆发黄光的YAG:Ce3+荧光粉已成为目前白光LED制作的主导方案。
3.1 实验目的
(1)掌握溶胶-凝胶法制备粉体材料的过程;
(2)熟悉YAG:Ce3+黄色荧光粉的光学性能;
(3)了解YAG:Ce3+黄色荧光粉在白光LED的应用。
3.2 实验药品
硝酸铝(AlNO3);氧化钇(Y2O3);氧化铈(CeO2);硝酸(HNO3);柠檬酸(C6H8O7);氨水(NH3·H2O)。
3.3 实验过程
(1)将Y2O3及CeO2粉末溶于稀硝酸中,配成一定浓度的溶液,按Y3-xAl5O12Ce3+化学计量比向该溶液中加入一定量Al(NO3)3溶液,混合均匀。称量药品如下Y2O3:1.6097g,Ce(NO3)3:0.3257g,Al(NO3)3:9.8737g,Y(NO3)3:5.4468g。
(2)取一定量的柠檬酸作为络合剂加入到上述混合溶液中,用氨水调节溶液Ph7~8。
(3)溶液于80℃下缓慢蒸发,直至得到粘滞性溶液,再于120℃下干燥2h,得到干凝胶。
(4)将干凝胶研磨后于1000℃下煅烧3h,随炉冷却。
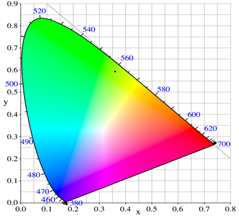
3.4 结果测试与分析

第二篇:本科学生综合性实验报告

本科生综合性实验报告
学号 084130091 姓名张微
学院 旅游与地理科学学院
专业、班级 08 地理科学 B 班
实验课程名称 地理信息系统
教师及职称 付磊(助教)
开课学期 2010 至 2011 学年 上 学期
填报时间 2010 年 12 月 17 日
云南师范大学教务处编印
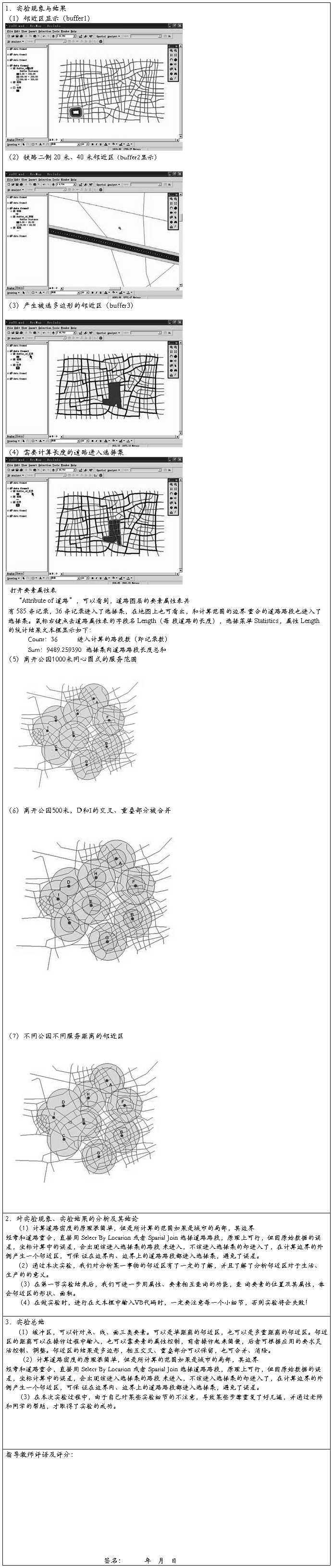
一、实验设计方案

二、实验报告