实验四 比较过氧化氢在不同条件下的分解
!实验安全:
1.使用酒精灯加热一定注意按照要求,防止烫伤、烧伤和引发火灾!
2.实验材料一律不能入口,以防发生意外!
3.H2O2溶液有一定的腐蚀作用。用量筒量取H2O2溶液时请小心,切勿将H2O2溅在皮肤上或者衣服上,一旦发生要马上用大量清水冲洗!
4.实验中,试管口不要对着自己或同学,以免反应太剧烈,气泡冲出试管到脸上产生危险!
一、实验目的
通过比较过氧化氢在不同条件下分解的快慢,了解过氧化氢酶的作用和意义。
二、知识背景
1. 化学反应活化能在一个化学反应体系中,任何一个分子要发生化学反应,都必须先被活化,即增加能量。分子从常态跃迁到容易发生化学反应的活跃状态所需要的能量,称为化学反应的活化能。酶是一种有机催化剂,与无机催化剂相比较,其主要作用是高效性,即在常温常压下能显著地降低化学反应所需要的活化能,从而促进化学反应高效地进行。
2.过氧化氢是一种代谢过程中产生的废物,它能够对机体造成损害。为了避免这种损害,过氧化氢必须被快速地转化为其他无害或毒性较小的物质,而过氧化氢酶就是常常被细胞用来催化过氧化氢分解的工具。几乎所有的生物机体都存在过氧化氢酶,肝脏是重要的解毒器官,过氧化氢酶尤其丰富,另外在土豆、青椒、鸡血等材料中也较多。过氧化氢酶是一种生物催化剂,Fe3+是一种无机催化剂,它们都可以将过氧化氢分解成水和氧气。反应如下:

每滴质量分数为3.5%的FeCl3溶液中的Fe3+数,大约是每滴质量分数为20%的肝脏研磨液中过氧化氢酶分子数的25万倍。
三、材料器材
1.实验材料:新鲜的质量分数为20%的肝脏研磨液、土豆提取液和青椒提取液;
2.试剂:质量分数为3.5%的FeCl3溶液;③新配制的体积分数为3%的过氧化氢溶液;
3.器材:量筒,试管,滴管,试管架,卫生香,火柴,酒精灯(或恒温水浴锅),试管夹,大烧杯,三脚架,石棉网,温度计。
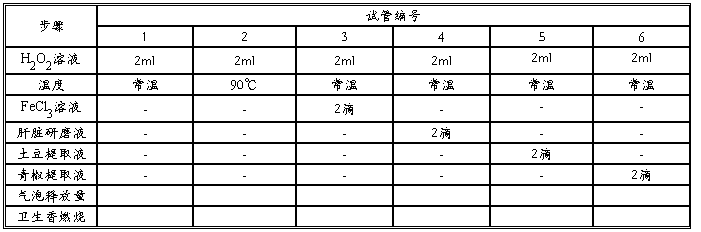
四、方法与步骤(按下表添加试剂并观察现象)
操作要点:
1.取6支洁净的试管,分别编上序号1、2、3、4、5、6,向各试管内分别加入2 mL过氧化氢溶液,按序号依次放置在试管架上。
2.将2号试管放在90 ℃左右的水浴中加热,观察气泡冒出的情况,并与1号试管作比较。
3.向3号试管内滴入2滴FeCl3溶液,向4号试管内滴入2滴肝脏研磨液,5号试管内滴入2滴土豆提取液,6号试管内滴入2滴青椒提取液,仔细观察哪支试管产生的气泡多。
4.2~3 min后,将点燃的卫生香分别放入3、4、5、6试管内液面的上方,观察哪支试管中的卫生香燃烧猛烈。
五、实验结论及分析
1.实验结果与预测结果的比较
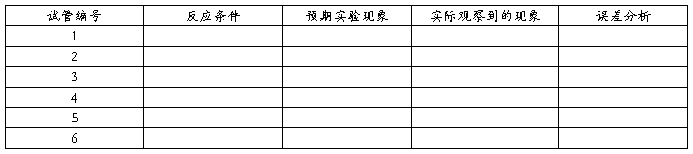
2.实验中遇到的问题
(1)为什么要选用新鲜的肝脏?
(2)3号和4号试管未经加热,也有大量气泡产生,这说明什么?
(3)在细胞内,可以通过加热来提高反应速率吗?
六、实验指导及注意事项
1.一定要保证肝脏的新鲜程度。新鲜肝脏中含有较多的过氧化氢酶,如果肝脏不新鲜,在微生物的作用下,过氧化氢酶可能被分解。另外,肝脏一定要充分研磨,以保证肝细胞破裂,否则可能影响实验效果。
2.试管壁一定要清洗干净,否则在温度不高的情况下,会在试管壁上形成小气泡,从而干扰实验结果的观察。
3.生物学教师所教的班级一般较多,做实验时往往是连续使用实验室,一个班的学生做完实验,另一个班的学生紧接着做同一个实验。如果试管没有清洗干净,可能出现的情况有:①如果使用的是上一个班同学做的3号试管或4号试管,则不需要加热,在常温下就会有大量的气泡产生,从而难以观察到真实的结果;②如果使用的是1号试管或2号试管,在水浴加热的过程中会在试管壁上产生大量的附着在试管壁上的小气泡。因此,每个班的学生做完之后,教师一定要求学生将试管清洗干净。
4.在测定水浴的温度时,温度计的水银球不要接触正在加热升温的烧杯的底部,否则测
出的水温会高出所需要的正确温度。
5.在做“操作要点”的第3步和第4步时,注意不要用拇指堵住试管口并用力振荡,否则4号试管内会产生大量的气泡,而且气泡的体积很大,会在试管中堆积起来,一直堆到试管口,这时,如果将点燃的卫生香放入4号试管中,会将卫生香浸灭。
第3步的操作可以这样进行:滴入催化剂后,将两支试管放在试管架上,仔细观察哪支试管产生的气泡多。这样做的优点是,第3步的现象十分明显,可以看出4号试管明显比3号试管放出的气泡多。同时,4号试管不会堆积大量的气泡,这时,再进行第4步的操作,效果会十分明显。
6.不要混用滴管。混用滴管的直接后果是实验的现象不一定真实可靠。
7.向试管中插入带火星的卫生香时动作要快,尽量往下,直到接近液面,但不要插到气泡中,以免使卫生香因潮湿而熄灭。
8.本实验中,H2O2溶液浓度、使用剂量、肝脏研磨液的新鲜程度等为无关变量,须控制一致。
七、同步练习
1.使用酶作为催化剂,与一般的无机催化剂相比,反应速度提高107~13倍。这说明酶具有
A.专一性 B.多样性 C.高效性 D.多变性
2.在做比较过氧化氢在不同条件下的分解实验时,向试管中插入燃烧但无火焰的卫生香时,不要插到气泡中,原因是 ( )
A.气泡中的氧含量低 B.气泡中的气体灭火
C.卫生香会因潮湿而灭火 D.燃烧过旺,不安全
3.在过氧化氢酶和Fe3+的催化效率比较的实验中,把肝脏制成研磨液的目的是 ( )
A.有利于过氧化氢酶的释放 B.保护过氧化氢酶
C.提高过氧化氢酶的活性 D.防止过氧化氢酶的分解
4.比较过氧化氢在不同条件下的分解实验中,滴入过氧化氢酶的试管内 ( )
A.产生的气泡多,燃烧得不猛烈 B. 产生的气泡多,燃烧得猛烈
 C.产生的气泡少,燃烧得不猛烈 D. 产生的气泡少,燃烧得猛烈
C.产生的气泡少,燃烧得不猛烈 D. 产生的气泡少,燃烧得猛烈
5.在右图所示的实验中属于自变量的是 ( )
A.催化剂不同
B.过氧化氢分解速率的大小
C.试管的大小
D.试管中过氧化氢溶液的量
6.常温常压下,要使过氧化氢溶液迅速放出大量的氧气,最好投入的物质是 ( )
A.新鲜肝脏 B.煮熟的肝脏 C.冰冻肝脏 D.生锈铁钉
7.把点燃但无火焰的卫生香插入盛有过氧化氢溶液和肝脏研磨液的试管中,卫生香猛烈燃烧的原因是试管中产生了 ( )
A.氧气 B.氢气 C.酒精 D.甲烷
8.下列有关对照实验设置的叙述中,错误的是 ( )
A.要设置对照组和实验组 B.要遵循单因子变量原则
C.无关变量要始终相同且适宜 D.自变量要始终保持相同
9.在煮过的和没煮过的马铃薯片上分别滴几滴过氧化氢。在马铃薯片X上出现泡沫,在马铃薯片Y上没有泡沫,以下哪一项是正确的解释 ( )
A.马铃薯片X是煮过的,因为过氧化氢只影响碳水化合物分解成单糖
B.马铃薯片X是煮过的,因为没煮过的马铃薯片酶能使过氧化氢不起作用
C.马铃薯片X是没煮过的,因为过氧化氢分解马铃薯片中的酶
D.马铃薯片X是没煮过的,马铃薯中含有促使过氧化氢分解的酶
10.在比较过氧化氢酶和Fe3+的催化效率实验中,要选用动物的新鲜肝脏,还要将肝脏制成研磨液,滴入肝脏研磨液和氯化铁溶液时,吸管要分开,这样实验效果才明显。回答下列问题。
(1)实验时选用新鲜肝脏,是因为 。
(2)将肝脏制成研磨液,是因为 。
(3)滴入肝脏研磨液和氯化铁溶液时,可否共用一个吸管? 。原因是 。
11.为了研究酶的有关特性,取两支洁净的试管并编号为A、B,各注入2ml体积分数3%的H202溶液;再向A管滴入2滴体积分数为3.5%的FeCl3溶液,向B管滴入2滴质量分数20%的肝脏研磨液;堵住管口,轻轻振荡;用点燃但无火焰的卫生香检验;观察并记录结果。
(1)本实验的主要目的是探索 。
(2)如果实验所用肝脏是新鲜的,但是两支试管的现象均不明显,从实验材料分析,原因可能是 。
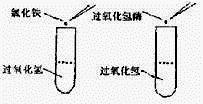
(3)过氧化物酶也能催化H2O2的分解,产生的[O]能使溶于水的无色焦性没食子酸氧化生成橙红色沉淀。为了鉴定马铃薯块茎是否含有过氧化物酶,设计如下实验。

参照上图所给信息,回答下列问题。
①3号试管内加入的物质有马铃薯块茎提取液、 、 。
②如果1号、2号、4号试管均未产生颜色反应,原因依次是 、
、 。
《比较过氧化氢在不同条件下的分解》答案及提示
同步练习:1.C 2.C 3.A 4. B 5.A 6. A 7.A 8.D 9.D
10.(1)肝脏如果不新鲜,肝脏细胞内的过氧化氢酶等有机物就会在腐生细菌的作用下分解,过氧化氢就不能分解成水和氧。
(2)可以使肝细胞内更多过氧化氢酶参与反应,从而加速过氧化氢的分解。
(3)不能。如果滴入的氯化铁溶液中混有少量的肝脏研磨液,会影响实验结果的准确性。
11.(1)酶的高效性(过氧化氢酶和Fe3+催化效率的高低)
(2)H2O2溶液放置时间过长而分解
(3)①2滴H2O2溶液 2ml焦性没食子酸溶液 ②没有过氧化物酶 没有过氧化氢 过氧化物酶因煮熟而失活
第二篇:实验报告探究不同条件下过氧化氢的分解
实验:比较过氧化氢在不同条件下的分解
目的要求:通过比较过氧化氢在不同条件下分解的快慢,了解过氧化氢酶的作用和意义。
实验材料:新鲜的质量分数为20%的肝脏(如猪肝、鸡肝)研磨液。
新配制的体积分数为3%的过氧化氢溶液,质量分数为3.5%的FeCl3溶液。
量筒、试管、滴管、试管架、卫生香、火柴、酒精灯、试管夹、大烧杯、三脚架、石棉网、温度计
实验原理:新鲜肝脏中有较多的过氧化氢酶。经计算,质量分数为3.5%的FeCl3溶液和质量分数为20%的肝脏研磨液相比,每滴FeCl3溶液的Fe3+数,大约是每滴研磨液中过氧化氢酶分子数的25万倍。比较过氧化氢在常温、加热、滴加FeCl3溶液和肝脏研磨液的条件下,比较过氧化氢的分解产生的气泡数或者观察带火星的木条复燃的情况,来分析不同条件下的过氧化氢的分解情况。
变量控制:自变量 因变量
方法步骤:
1、取4支洁净的试管,分别编上序号ABCD,向各试管中分别加入2ml过氧化氢溶液,按序号依次放置在试管架上。
2、设计实验组和对照组如下表,填写表中的空白位置,3、填写你观察到的实验结果
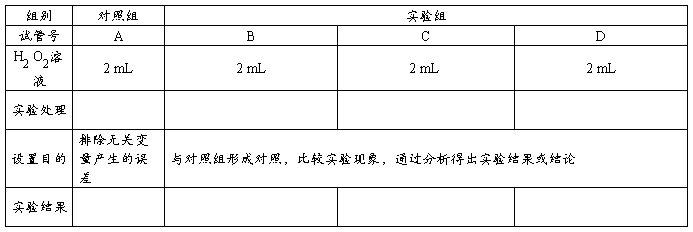
4、实验现象分析
(1) B、C、D号试管与A号试管对比说明 。
(2)C号试管和D号试管对比说明 。
(3)CD号试管和B号试管对比说明 。
说明:对照实验中的自变量应具有单一性,即遵循单一变量原则,只有这样才能保证实验结果的正确性,增强实验结论的说服力。
注意:①实验时要选用新鲜的肝脏作材料,否则肝细胞中的过氧化氢酶等有机物会部分分解,从而影响实验的准确性。
②肝脏要制成研磨液。研磨后的肝脏能与试管中的过氧化氢充分接触,加速过氧化氢的分解。
实验设置原则:单一变量原则、 、 。
巩固练习:
已知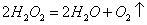 ,可以通过观察反应过程中O2的生成速度(即气泡从溶液中释放的速度)来判断H2O2分解反应的速度。请用所给的实验材料和用具设计实验,使其能同时验证过氧化氢酶具有催化作用和高效性。要求写出实验步骤、预测实验结果、得出结论,并回答问题。
,可以通过观察反应过程中O2的生成速度(即气泡从溶液中释放的速度)来判断H2O2分解反应的速度。请用所给的实验材料和用具设计实验,使其能同时验证过氧化氢酶具有催化作用和高效性。要求写出实验步骤、预测实验结果、得出结论,并回答问题。
实验材料与用具:适宜浓度的H2O2溶液,蒸馏水,3.5%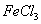 溶液,0.01%的过氧化氢酶溶液,恒温水浴锅,试管。
溶液,0.01%的过氧化氢酶溶液,恒温水浴锅,试管。
(1)实验步骤:
① ;
② ;
③ 。
(2)实验结果预测及结论:
整个实验中不同处理的试管中O2的释放速度从快到慢依次是: 。由此可得出的结论是 。
(3)如果仅将实验中的恒温水浴改为80℃,重做上述实验,O2释放的速度最快的是 ,原因是 。
1.使用酶作为催化剂,与一般的无机催化剂相比,反应速度提高107~13倍。这说明了酶具有
A.专一性 B.多样性 C.高效性 D.多变性
2.在做比较过氧化氢在不同条件下的分解实验时,向试管中插入燃烧但无火焰的卫生香时,不要插到气泡中,原因是
A.气泡中的氧含量低 B.气泡中的气体灭火
C.卫生香会因潮湿而灭火 D.燃烧过旺,不安全
3.在过氧化氢酶和Fe3+的催化效率比较的实验中,把肝脏制成研磨液的目的是
A.有利于过氧化氢酶的释放 B.保护过氧化氢酶
C.提高过氧化氢酶的活性 D.防止过氧化氢酶的分解
4.比较过氧化氢在不同条件下的分解实验中,滴入过氧化氢酶的试管内
A.产生的气泡多,燃烧得不猛烈 B. 产生的气泡多,燃烧得猛烈
C.产生的气泡少,燃烧得不猛烈 D. 产生的气泡少,燃烧得猛烈
D.试管中过氧化氢溶液的量
6.常温常压下,要使过氧化氢溶液迅速放出大量的氧气,最好投入的物质是 ( )
A.新鲜猪肝 B.煮熟煮猪肝 C.冰冻猪肝 D.生锈铁钉
7.把点燃但无火焰的卫生香插入盛有过氧化氢溶液和肝脏研磨液的试管中,卫生香猛烈燃烧的原因是试管中产生了 ( )
A.氧气 B.氢气 C.酒精 D.甲烷
8.下列有关对照实验设置的叙述中,错误的是 ( )
A.要设置对照组和实验组 B.要遵循单因子变量原则
C.无关变量要始终相同且适宜 D.自变量要始终保持相同
