蔗糖水解速率常数的测定
1.数据处理
(1) 结果要求:① 蔗糖比旋度
结果要求:① 蔗糖比旋度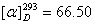 ,用100mm旋光管测定,数据可控制在66.0±1.0
,用100mm旋光管测定,数据可控制在66.0±1.0
②用公式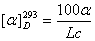 计算实验数据,并与手册中查得的蔗糖旋光度
计算实验数据,并与手册中查得的蔗糖旋光度
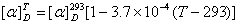 (适用范围287~303K)进行比较。
(适用范围287~303K)进行比较。
③将时间t、旋光度(at-a¥)、lg(at-a¥)列表。
④ lg(at-a¥)~ t作图,由直线斜率求出两温度下的k(T1)和k(T2) ,各自的反应半衰期,由图外推求t=0时的两个a0。
⑤ 由k(T1)和k(T2)利用Arrhenius公式求其平均活化能。
(2)HCl浓度对蔗糖水解速度常数的影响(蔗糖溶液浓度均为10%)

2. 点评
(1) 实验关键
①能正确而较快地测读旋光仪的读数,初操作仪器者通过测蔗糖比旋光度而得到练习。
②温度对实验数据的影响大,要注意整个实验时间内的恒温,如无样品管恒温夹套,则旋光管离开恒温水浴时间应短。根据实验数据,当[H+]=1M(HCl),蔗糖10%
k303.7K=3.35´10-2min-1 k313.2K=7.92´10-2min-1
由以上数据求得在303.7~313.2K温度范围内平均活化能Ea»71kJ×mol-1。
可见,本实验的实验温度范围最好控制在288~303K内进行,温度过高反应速度太快读数将发生困难。
③ HCl浓度也要配制正确,[H+]对反应速度常数有影响,若酸浓度不准,尽管数据线性关系再好,k值偏离文献数据。
④ HCl 与蔗糖都要预恒温至实验温度,否则将影响初始几点的实验真实温度。
(2) 蔗糖的水解在酸性介质中进行,H+为催化剂,在[H+]浓度较低时,水解速度常数
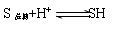 kµ[H+]但在[H+]增加时,k与[H+]不成比例,且用HCl和用HNO3或HClO4对反应速度常数的影响也不一样(特别是酸浓度高时)。进一步实验指出若[H+]较大,反应速度常数k正比于h0,而h0可予如下定义:
kµ[H+]但在[H+]增加时,k与[H+]不成比例,且用HCl和用HNO3或HClO4对反应速度常数的影响也不一样(特别是酸浓度高时)。进一步实验指出若[H+]较大,反应速度常数k正比于h0,而h0可予如下定义:
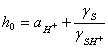
其中aH+是氢离子活度,gS和gSH+为H+、SH+的活度系数,利用[H+]对k的影响,可以研究蔗糖水解的机理,长期以来有二种假设:

按照反应①属一级反应,从理论上可以推出反应速度常数k应与h0成正比。
按照反应②属假单分子(二级)反应,从理论上可以推出反应速度常数k应与[H+]成正比。从而实践证明第一种机理是正确的,因而蔗糖水解判为一级反应。反应是一复杂反应。显然其计量方程式并不表示此反应的机理,反应也非双分子反应。
(3)本实验的误差可作如下估计:
根据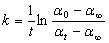
显然,在不同时刻t所得at代入上式中计算k的误差是不同的。采用微分方程
推导速率常数的相对误差的结果是
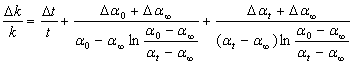
①应增加旋光管长度
假设在200mm旋光管中有下列一点的数据t=25min,a0=13.2,at=5.20,a¥= -4.10
dt=0.5min,da0=dat=da¥= 0.05 代入上式求得
若此点改在100mm旋光管中测,得到t=25min,a0=6.6,at=2.60,a¥= -2.05;dt=0.5min,da0=dat=da¥= 0.05 代入上式求得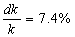
可见用较长旋光管可以减少读数误差而提高精度。
②选时间长短、取点要合理
当t较小时,主要误差来源于时间误差,如t=10min,引入误差为5%。而t较大时,(at-a¥)较小,是主要误差来源,因此实验取点要合理,既不能取时间太短,又不能取时间太长的点,本实验误差应小于10%(一般动力学实验误差限)。
3.讨论
(1)旋光度的零点校正有何意义?
解 蔗糖是否纯,通过测比旋光度来鉴定。另外,零点校正有利于近终点的判断。即旋光性由右旋变到左旋。
(2)为什么配蔗糖溶液可用粗天平秤量?
解 其一,对于这个假单分子(二级)反应,由于大量水存在,虽有部分水分子参加反应,但在反应过程中水的浓度变化极小,所以只要蔗糖浓度浓度不太浓,水的浓度变化问题对反应速度的影响不大。其二,浓度不同的蔗糖,在200mm管中测得a=26.60,则
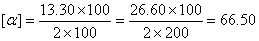 蔗糖反应中旋光系数正比于旋光系数,其三,尽管蔗糖的转化速度与蔗糖浓度、酸浓度、温度及催化剂种类有关,但速率常数k与其中的蔗糖浓度无关,是可以从公式看出的。
蔗糖反应中旋光系数正比于旋光系数,其三,尽管蔗糖的转化速度与蔗糖浓度、酸浓度、温度及催化剂种类有关,但速率常数k与其中的蔗糖浓度无关,是可以从公式看出的。
(3) 如果没有a¥数据(或者反应未趋完全),是否也能求得反应速率常数?
解 ①对于一级反应在没有a¥数值,或者在反应不完全,不能求得a¥值时,也可由下法求出反应的速率常数k值来。先列出时间为t时的浓度c1,(或a t)和时间为t+Dt时的浓度c2,(或a2),Dt可为任意的时间间隔,不过最好是实验时反应进行时间的一半,作lg(c1-c2)对t的图其斜率即为-k/2.303。公式推导如下:
c=c0e-kt
由此可得
c1=c0e-kt,c2=c0e-k(t+Dt),c1-c2= c0e-kt(1-e-kDt)
取对数
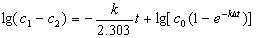 (2.10.1)
(2.10.1)
然后作lg(c1-c2)~t图,由斜率求得k。
由于旋光度a与浓度c成正比,所以可直接用旋光度a代c。设
a=Kc+P,c1-c2=(a1-a2)/K
代入(2.9.1)得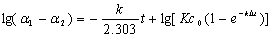
②ln(a¥-at)= ln(a¥-a0)-k×t
不知a0,也一样求k值。而蔗糖水溶液与HCl的混合恰恰是放热反应恒温条件被破坏,使得最初的一些点的测试出现偏差。
(4)试推导公式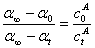
解 对于任何化学反应体系,在温度、压力一定时,若某物理性质“l”具有加和性,且与浓有线性关系,则必有关系式
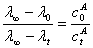 (2.10.2)
(2.10.2)
(2.10.2)式对于一级反应、二级(如乙酸乙脂皂化)反应及n级反应来说通用。推导如次:
对任意一个化学反应,其计量方程式为aA+bB=gG+hH,并设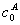 、
、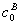 、
、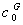 和
和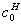 分别为A、B、G和H在反应进行到记时初始时刻(记为t=0)时的浓度,kA、kB、kG和kH为比例常数。列出线性关系式
分别为A、B、G和H在反应进行到记时初始时刻(记为t=0)时的浓度,kA、kB、kG和kH为比例常数。列出线性关系式
l=l介质+(lA+lB+lG+lH)
l0=l介质+(KA×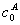 +KB×
+KB×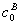 +KG×
+KG×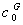 +KH×
+KH×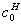 )
)
l¥=l介质+[KB(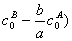 ]+[KG(
]+[KG(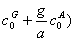 ]+[KH(
]+[KH(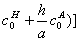
lt=l介质+{ KA×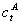 +KB[
+KB[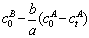 ]}+[KG(
]}+[KG(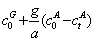 ]+KH[
]+KH[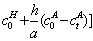 }
}
所以 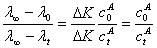
(5)判断:蔗糖水解实验是将盐酸溶液倒入蔗糖溶液。
解 对
(6)拟出测有色(红棕色水溶液)香精香根油旋光度的简易方法。
解:(1)用活性炭脱色 (2)用有机溶剂稀释 (3)选样品管长度的原则是使能透过光路看清三分视野的变化 (4)计算则根据稀释倍率及比旋度公式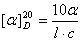
4.思考题
1.实验中,为什么用蒸馏水来校正旋光仪的零点?在蔗糖转化反应
过程中,所测的旋光度αt是否需要零点校正?为什么?
答:蔗糖溶液以蒸馏水作溶剂,故用纯蒸馏水作零点校正。蔗糖
转化反应过程中,无须再作零点校正,因都以蒸馏水作校正,只需校
正一次。
2.配置溶液时不够准确,对测量结果是否有影响?
答:有,当HCl溶液浓度过大时,蔗糖水解速率测量结果会偏大。
3.在混合蔗糖溶液和盐酸溶液时,我们将盐酸加到蔗糖溶液中,
可否将蔗糖溶液加到盐酸溶液中去?为什么?
答:如将蔗糖溶液加到HCl溶液中,由于,HCl溶液浓度过大,
会加快蔗糖水解,影响测量结果。
5、本实验要想减少误差,应注意什么?
答:(1)正确操作仪器。(2)准确配制HCl溶液浓度。
第二篇:蔗糖水解反应速率常数测定的实验改进
!44!
实验科学与技术20xx年10月
蔗糖水解反应速率常数测定的实验改进
邹桂华,刘春凤,沈广志,高?静
a
b
a
a
(牡丹江医学院?a?药学系;b?红旗医院,黑龙江牡丹江?157011)
摘要:蔗糖水解反应速率常数测定是典型的一级反应动力学实验,是物理化学实验的基本内容之一,针对实验中出现的问题,对实验方法,实验仪器,数据处理的方法进行了改进,实验结果满意,将实验变为综合性设计性实验,从设计实验方案到溶液的配制,到旋光仪的使用,到数据的处理,再到计算机的使用,激发了学生的学习热情,提高了学生的综合素质。关?键?词:蔗糖水解;旋光度;数据处理中图分类号:TS244?11??文献标识码:
B??文章编号:1672-4550(2009)05-0044-02
ImprovementofSpeedConstantDeterminationinSucrose
HydrolysisReaction
ZOUGui?hua,LIUChun?feng,SHENGuang?zhi,GAOJing
(a?PharmacyDepartment;
a
b
a
a
b?HongqiHospita,lMudanjingMedicalUniversity,Mudanjiang?157011,China)
Abstract:Speedconstantdeterminationinsucrosehydrolysisreactionisthetypicalfirst?levelreactionkineticsexperiment,oneofbas?iccontentsinphysicalchemistryexperiment.Inviewoftheproblemexistinginexperiment,thispaperimprovesthemethod,instru?
ment,anddataprocessing,whichproducesasatisfactoryexperimentalresult.Theexperimentischangedintocomprehensiveandde?signexperiment,fromthedesignedexperimenttothesolutionconfiguration,tousingopticalinstruments,todataprocessing,andcomputer?suse.Thusstimulatesstudent?sstudyenthusiasm,improvesstudent?soverallquality?Keywords:sucrosehydrolysisreaction;opticalrotation;dataprocessing
1?引?言
蔗糖水解反应速率常数测定是牡丹江医学院制药、药学、检验专业开设的实验项目。是一个典型的一级反应动力学实验。我们按照文献[1]的实验设计进行操作,测定20?下的旋光度,通过用坐标纸作图求得反应的速率常数k。通过几年的教学实践发现一些问题,因此我们根据现有的条件对实验进行了改进,取得了满意的结果。
于60?的水浴上温热30min,冷却至室温测定旋光度,但因为加热,酸和水的挥发导致物质浓度发生变化,影响反应的进行,可能有副产物生成,而且蔗糖是否完全转化也很难确定,导致反应终了时? 测定不准确。
4)手工使用坐标纸作图误差较大。5)学生被动的完成实验,学习热情不高。
3?改进的实验内容与操作方法
根据学校的实际情况,我校采用的是大循环式的实验教学方法,教师上课时同时指导2个不同实验的教学模式。将作蔗糖水解反应速率常数测定实验的学生分成4个小组,采用4台旋光仪,蔗糖浓度按照实验书的要求为20。影响实验结果的因素主要有2点:温度和催化剂的浓度。为了充分调动学生的积极性,让学生在阅读实验讲义后,自主选择实验温度和催化剂的浓度,设计实验方案,配制溶液进行实验。教师进行辅助指导,按实验教材步骤进行操作。
为了使反应在恒温条件下进行,我们制作了带。
2?实验出现的问题
1)实验课开设在6月份,天气好时,室温超过20?,很难将温度控制在20?。
2)反应测定需要恒温温度,而我校的旋光仪(WXG-4型圆盘旋光仪)没有恒温装置,无法进行恒温操作。
3)测定? 时,是将蔗糖和盐酸的混合液置
收稿日期:2009-01-20
作者简介:邹桂华(1981-)女,助教,在读硕士研究生,
第7卷?第5期ExperimentScience&Technology
!45!
由于测定? 时,误差较大,因此我们改变数据处理方法,不测定?
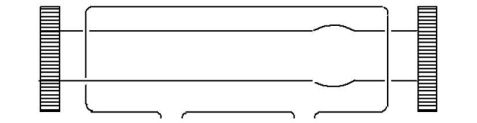
。下面介绍数据处理原理。
先将t和?t的数据手工输入,然后让C2的数据等于B8,C3的等于B9,以此类推。让D2=B2-C2,用鼠标拖动之后就可以得到数列D的数据,运用函数让E2=ln(D2),用鼠标拖动之后就可以得到数列E的数据。在?插入%中选择?图表%,选择XY散点图,在下一步的?系列%中添加X和Y,
图1?旋光仪的恒温套管
X选择A2到A9,Y选择E2到E9。点击下一步即完成散点图的绘制。在?图标%中选择?添加趋势线%,在类型中选择线性,在选项中选择显示公式和显示R平方值。R相关系数的平方,值越接近于1表示线性越好。这样就可得到回归公式,得到直线的斜率就是我们要求的k值,如图3
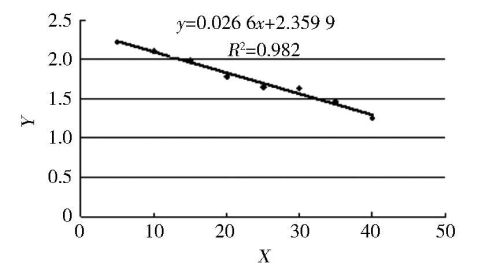
所示。
2
反应的动力学方程为:
ln(?t-? )=-kt+ln(?0-? )?t-? =Ae
式中,?t是定值。
由式(2)-式(3)得?t-?t+?t=Ae式中,e
-k?t
-kt
-kt
(1)(2)(3)
?A=?0-?
-k(t+?t)
?t+?t-? =Ae
-Ae
-k(t+?t)
-k?t
=
-kt
Ae是常数。
-kt
(1-e)=A#e(4)(5)
ln(?t-?nA#-ktt+?t)=l
以ln(?t-?t+?t)对t作图,可得一直线,通过斜率求得k,不必测出?n, 。我们让?t=30mi这样在记录数据时则需记录5min、10min、15min、20min、25min、30min、35min、40min、45min、50min、55min、60min、65min、70min时的数据。
由于作图时比例尺选择不当,描点时产生误差。作图时也不再用坐标纸手工作图。而采用Mi?crosoftExcel处理实验数据MicrosoftExcel是一个功能强大、使用方便的表格数据综合分析处理系统,数据处理简单,方便直观,而且有丰富的函数,可以进行数据处理、分析统计、制图。将我们的数据用MicrosoftExcel处理,简便、快速、减少误差。
以实验过程中所得的数据为例,介绍MicrosoftExcel的使用方法,如图2
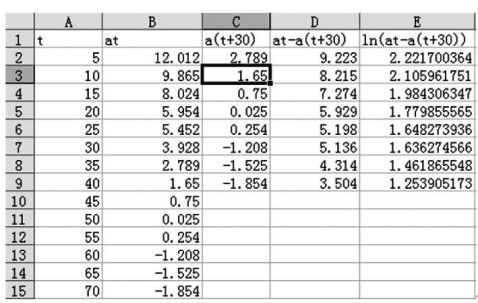
所示。
可以将工作表进行保护,将文件保存后下次使用:先将B列的数据选中,选择单元格格式中的保护,将锁定取消。然后将整个工作区选中,在?工具%中?保护%选择?保护工作表%。工作区当中的数据只有?t是可以改变的。在下次使用时只需输入?t的值即可,使数据处理更加简便。
图3?示例图
4?结束语
通过对实验的改进,让学生自己设计实验方案,学生是主体,而教师只起指导作用,充分激发了学生的学习热情,提高了学习的积极性,加深了学生对基础理论的理解。从设计实验方案到溶液的配制,到旋光仪的使用,到数据的处理,再到计算机的使用,提高了学生的综合素质。
参考文献
[1]?东北师范大学?物理化学实验[M]?2版?北京:高
等教育出版社,
1998?
[2]?周丛山,杨涛?蔗糖水解实验数据处理新方法?
[J]?实验科学与技术,2008,6(2):46-48?
[3]?周华锋,侯纯明,张丽清,等?蔗糖水解反应动力
学研究[,34(202?
图2?MicrosoftExcel的使用方法
