过氧化氢含量的测定
一、实验目的
1.掌握用KMnO4法直接滴定H2O2的基本原理和方法。
2.掌握用吸量管移取试液的操作。
二、实验原理
在强酸性条件下,KMnO4与H2O2进行如下反应:
2 KMnO4 +5 H2O2 + 3 H2SO4= 2MnSO4+ K2 SO4 + 5O2↑+ 8H2O
KMnO4自身作指示剂。
三、试剂
1.KMnO4标准滴定溶液c(1/5 KMnO4)=0.5mol/L。
2.H2SO4(20%)。
3.双氧水试样。
四、实验内容
用吸量管移取2.00mL(约2g)双氧水试样,放入250mL容量瓶中,称重M,用水稀释至刻度,摇匀。
用移液管吸取上述试液25.00mL,置于锥形瓶中,加10mL 20%H2SO4,用c(1/5 KMnO4)= 0.5mol/L KMnO4标准滴定溶液滴定至溶液呈浅粉色,保持30s不褪为终点。
五、计算公式
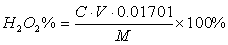
式中 C——c(1/5 KMnO4)的浓度,0.5mol/L
V——滴定所用的体积,ml
M——双氧水称取的质量,g
六、试剂
① H2SO4(20%):20ml浓硫酸定容至100ml。
② KMnO4标准滴定溶液c(1/5 KMnO4)=0.5mol/L。
16g KMnO4定容至1000ml,盖上表面皿,加热至沸并保持微沸状态1h,冷却后,贮于棕色试剂瓶中。在室温下静置2~3天后过滤备用(过滤可以省去,杂质不是很多的)。
KMnO4标定:用草酸钠
0.15~0.20g Na2C2O4基准物3份,分别置于250ml的锥形瓶中,加入60ml水使之溶解,加入15ml H2SO4,在水浴加热到75~85℃,趁热滴定。
开始滴定时反应速度慢,待生成Mn2+后,滴定速度可加快。
2MnO4-+5C2O42-+16H+→2 Mn 2++10CO2+ 8 H2O
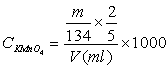 (大概应该是0.1左右,)
(大概应该是0.1左右,)
C(1/5 KMnO4)=0.5mol/L
C(KMnO4)=0.1mol/L
C(1/5 KMnO4)与C(KMnO4)是指 转移1mol电子的物质量。
七、实验注意问题
①只能用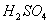 来控制酸度,不能用
来控制酸度,不能用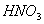 或HCl控制酸度。因
或HCl控制酸度。因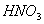 具有氧化性,
具有氧化性,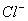 会与
会与 反应。
反应。
②不能通过加热来加速反应。因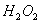 易分解。
易分解。
③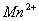 对滴定反应具有催化作用。滴定开始时反应缓慢,随着
对滴定反应具有催化作用。滴定开始时反应缓慢,随着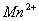 的生成而加速。
的生成而加速。
八、思考题
1.用高锰酸钾法测定H2O2时,能否用HNO3或HCl来控制酸度?
答:用高锰酸钾法测定H2O2时,不能用HCl或HNO3来控制酸度,因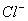 会与
会与 反应,HNO3具有氧化性。
反应,HNO3具有氧化性。
2.用高锰酸钾法测定H2O2时,为何不能通过加热来加速反应?
答:因H2O2在加热时易分解,所以用高锰酸钾法测定H2O2时,不能通过加热来加速反应。
第二篇:过氧化氢含量测定(KMnO4法)
河北工业大学 实验报告
课程:分析化学实验
班级: 姓名: 组别: 同组人: 日期:20##-3-2
实验:过氧化氢含量测定(KMnO4法)
一、实验目的:
1、掌握应用高锰酸钾法测定过氧化氢含量的原理和方法。
2、掌握高锰酸钾标准溶液的配制和标定方法。
二、实验原理:
1、工业品过氧化氢(俗名双氧水)的含量可用高锰酸钾法测定。在稀硫酸溶液中,室温条件下,H2O2被KMnO4定量氧化,其反应式为:
5H2O2+2MnO4-+6H+=2Mn2++5O2↑+8H2O
根据高锰酸钾溶液的浓度和滴定所耗用的体积,可以算得溶液中过氧化氢的含量。
市售的H2O2约为30%的水溶液,极不稳定,滴定前需先用水稀释到一定浓度,以减少取样误差。在要求较高的测定中,由于商品双氧水中常加入少量乙酰苯胺等有机物质作稳定剂,此类有机物也消耗4而造成误差,此时,可改用碘量法测定。
2、高锰酸钾是最常用的氧化剂之一。市售的高锰酸钾常含有少量杂质,如硫酸盐、氯化物及硝酸盐等,因此不能用精确称量的高锰酸钾来直接配置准确浓度的溶液。用KMnO4配制的溶液要在暗处放置数天,待KMnO4把还原性杂质充分氧化后,再除去生成的MnO2沉淀,标定其准确浓度。光线和Mn2+、MnO2等都能促进KMnO4分解,故配好的KMnO4应除尽杂质,并保存于暗处。
KMnO4标准溶液常用还原剂Na2C2O4作基准物来标定。Na2C2O4不含结晶水,容易配制。用Na2C2O4标定KMnO4溶液的反应如下:
2MnO4-+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O
滴定时可利用4-离子本身的颜色指示滴定终点。
三、实验试剂:
KMnO4(s) Na2C2O4(s) 1mol·L-1 H2SO4(aq) 1mol·L-1 MnSO4 H2O2样品
四、实验步骤:
1、KMnO4溶液的配置: 2、KMnO4溶液浓度的标定:
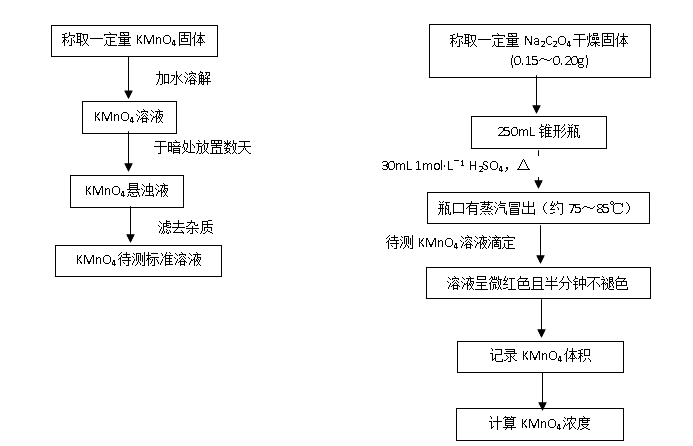
3、H2O2含量的测定:
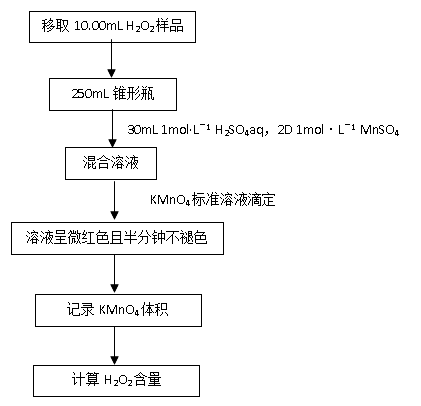
五、实验记录:
1、KMnO4溶液浓度的测定:

2、H2O2含量的测定:
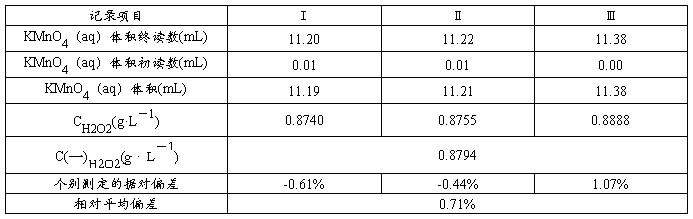
六、问题与思考:
1、配制KMnO4标准溶液时为什么要把KMnO4溶液煮沸一定时间(或放置数天)?
答:为了使KMnO4溶液中的还原性物质完全反应,使KMnO4溶液浓度稳定。
2、用Na2C2O4为基准物标定KMnO4溶液时,应注意哪些重要的反应条件?
答:滴定前要加入少量稀硫酸以确保酸度;为了使反应加快,需要加热至75~85℃,但在滴定至终点前,溶液温度不应低于60℃;滴定时应注意滴定速度,不能过快,滴完一滴后应等到溶液完全褪至无色再滴入下一滴。
3、用KMnO4法测定H2O2时,能否用HNO3或HCl来控制酸度?为什么?
答:不能。HNO3同样会氧化H2O2,而在酸性条件下,KMnO4会氧化Cl-,这两种酸消耗H2O2和KMnO4,干扰反应。
4、装过KMnO4溶液的滴定管或容器常有不易洗去的棕色物质,这是什么?应该怎样除去?
答:是MnO2,可用浓盐酸除去。
