实验二:乙醇的蒸馏及沸点的测定
一、实验目的
1.了解蒸馏提纯液体有机物的原理、用途。
2.掌握蒸馏提纯液体有机物的操作步骤。
3.了解沸点测定的方法。
4.了解折光率测定的方法和意义。
二、实验原理
将液体加热至沸,使液体变为气体,然后再将蒸气冷凝为液体,这两个过程的联合操作称为蒸馏。
蒸馏是分离和纯化液体有机混合物的重要方法之一。当液体混合物受热时,由于低沸点物质易挥发,首先被蒸出,而高沸点物质因不易挥发或挥发的少量气体易被冷凝而滞留在蒸馏瓶中,从而使混合物得以分离。蒸馏法提纯工业乙醇只能得到95%的乙醇,因为乙醇和水形成恒沸化合物(沸点78.1℃),若要制得无水乙醇,需用生石灰、金属钠或镁条法等化学方法。
三、主要试剂及产品的物理常数:(文献值)
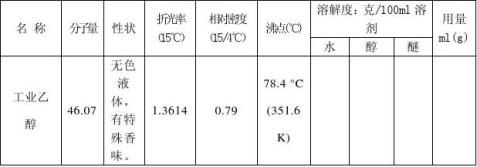
四、实验装置图
六、数据处理
实际产量=
回收率=
nDt =
nD20=
七、思考题:
1
1.什么叫沸点?液体的沸点和大气压有什么关系?
2.蒸馏时加入沸石的作用是什么?如果蒸馏前忘记加沸石,能否立即将沸石加至将近沸腾的液体中?当重新蒸馏时,用过的沸石能否继续使用?
3.如果液体具有恒定的沸点,那么能否认为它是单纯物质?
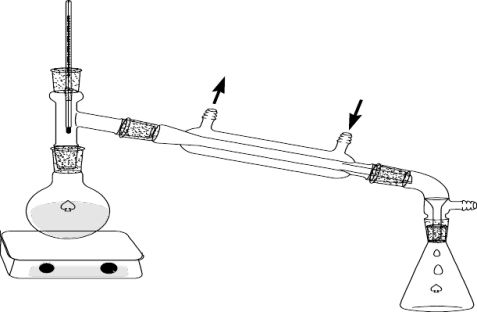
五、操作流程和实验记录
工业乙醇 + 沸石 +
蓝墨水
时间 实验记录:
100ml圆底烧瓶
工业乙醇=? 沸石=? 蓝墨水=?
第一滴馏出液流出时t1=?℃

工业乙醇
蒸馏结束时t2=?℃
沸程?(后馏分的起始温度)
称量

前馏分=总重-瓶重 后馏分=总重-瓶重
2
产品状态? nDt=?
第二篇:蒸馏及沸点的测定2
蒸馏及沸点的测定
一、 实验目的
1. 了解蒸馏和沸点测定的用途
2. 掌握沸点测定的方法。
3. 掌握蒸馏烧瓶、冷凝管等的使用方 法,学会蒸馏装置的使用。
二、 实验原理
当液体饱和蒸汽压与外界压强相等时,液体开始沸腾汽化。蒸馏是将液体加热到沸腾状态,使之汽化,再将蒸汽冷凝为液体的两个联合操作。它是分离和提纯液体化合物最常用的一种方法,也是测定液体沸点的一种方法。
沸点是液体的饱和蒸汽压与外界压强相等时的温度。每个纯的有机化合物在一定的压力下均有恒定的沸点。液体沸点的测定可以用来鉴别有机化合物,也可以用之定性的鉴定化合物的纯度。
三、 实验仪器和药品
仪器:圆底烧瓶、直形冷凝管、接受器、
锥形瓶、蒸馏头、温度计等。
药品:工业酒精。
四、 实验装置
(在装置上讲解)
五、 实验步骤
(结合装置讲解)
六、 实验注意事项
1. 是否放了沸石,若已经开始热而发现忘了放沸石,那么应等液体冷却后在加沸石。
2. 温度计水银球的位置是否正确。
3. 先通水后加热,水应从冷凝管的下方进上方出。
