实验二 蒸馏及沸点的测定
一. 实验目的:
1.了解测定沸点的意义。
2.掌握常量法(蒸馏法)测定沸点的原理和方法。
二. 实验原理:
当液体物质被加热时,该物质的蒸气压达到与外界施于液面的总压力(通常是大气压力)时液体沸腾,这时的温度称为沸点。常压蒸馏就是将液体加热到沸腾变成蒸气,又将蒸气冷凝得到液体的过程。
每种纯液态的有机物在一定的压力下均有固定的沸点。利用蒸馏可将二种或两种以上沸点相差较大(>30℃)的液体混合物分开。纯液体化合物的沸距一般为0.5~1℃,混合物的沸距则较长。可以利用蒸馏来测定液体化合物的沸点。
三、实验仪器和药品
请学生自已整理罗列
四、实验装置图
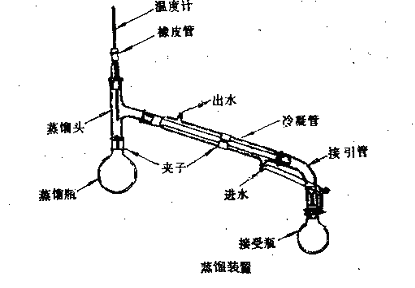
五.实验步骤
蒸馏实验装置主要包括蒸馏烧瓶,冷凝管,接受器三部分。仪器按从下往上,从左到右原则安置完毕,注意各磨口之间的连接。根据被蒸液体量选蒸馏瓶(容积的1/3~2/3),放置30ml无水乙醇。加料时用玻璃漏斗将蒸馏液体小心倒入。(温度计经套管插入蒸馏头中,并使温度计的水银球正好与蒸馏头支口的下端一致)。
放入1~2粒沸石,然后通冷凝水(下进上出),开始加热并注意观察蒸馏瓶中的现象和温度计读数的变化。当瓶内液体开始沸腾时,蒸气前沿逐渐上升,待达到温度计水银球时,温度计读数急剧上升,这时应适当调小火焰,以控制馏出的液滴以每秒钟1~2滴为宜。在蒸馏过程中,应使温度计水银球处于被冷凝液滴包裹状态,此时温度计的读数就是馏出液的沸点。换一个已称量过的干燥的锥形瓶作接受器。收集馏分。记下该馏分的沸程:即该馏分的第一滴t1和最后一滴时的读数t2。若温度计读数会突然下降,即可停止蒸馏。若温度计读数无明显变化,但瓶内只剩下少量(约0.5~1mL)液体时,也不应将瓶内液体完全蒸干,以免发生意外。测量所收集馏分的体积v,并计算回收率。 蒸馏结束,先停止加热,后停止通水,拆卸仪器顺序与装配时相反。
六、实验记录
(须严格按标准格式记录)
七、实验结果
乙醇的沸程为:t1~t2℃,计算回收率。
八、思考题
1、沸石(即止暴剂或助沸剂)为什么能止暴?如果加热后才发现没加沸石怎么办?
2.在蒸馏过程中,加热功率不能太大又不能太小,为什么?
注意:本次实验回收乙醇。
第二篇:乙醇的蒸馏及沸点测定 实验报告


.

报告题目:乙醇的蒸馏及沸点测定
专业班级:生物工程
指导老师:刘明星
学生姓名:何德维
学 号:1108110384
20##年3月30日
乙醇的蒸馏及沸点测定
一.实验目的
1、了解用蒸馏法分离和纯化物质及测定化合物沸点的原理与方法。
2、训练蒸馏装置的安装与操作方法,要求整齐、正确。
3、掌握常量法和微量法测定沸点的原理和方法、蒸馏与沸点测定的原理。
二.实验原理
蒸馏是分离和提纯液体有机物质的最常用方法之一
液体加热时蒸汽压就随着温度升高而加大,当液体的蒸汽压增大到与外压相等时,会有大量气泡从液体内逸出,液体沸腾。这时的温度称为液体的沸点。
蒸馏是将液体加热到沸腾,使液体变为蒸汽,然后使蒸汽冷却再凝结为液体这两个过程的联合操作。因为组成液体混合物的各组分的沸点不同,当加热时,低沸点物质就易挥发,变成气态,高沸点物质不易挥发汽化,而留在液体内,这样,我们就能把沸点差别较大(至少30℃以上)的两种以上混合液体分开,以达到纯化的目的。同时,利用蒸馏法,可以测定液体有机物的纯度,每一种纯的液体有机物质,在平常状况下,都有恒定的沸点(恒沸混合物除外),而且恒定温度间隙小(纯粹液体的沸程一般不超过1-2℃);当有杂质存在,则沸点会有变化(有时升高,有时降低,根据杂质温度高低二变化),而且沸点的范围也会加大。
沸点相近的有机物,蒸汽压也近于相等。因此,不能用蒸馏法分离,可用分馏法分离;对于沸点高、受热易分解的物质,可用减压蒸馏或水蒸气蒸馏来分离提纯。
三.主要药品及仪器
1.工业酒精(滴几滴红汞或其他有色物)20ml(蒸馏用)
2.烧瓶(50ml) 蒸馏头 温度计(100℃) 冷凝管 接引管 三角瓶
3.铁夹 铁环 酒精灯 沸石 量筒(50ml) 铁台
四.实验步骤
1、清洗所有蒸馏装置,并用量筒量取20ml工业酒精装入烧瓶中,再放入2-3颗沸石。
2、安装蒸馏装置。首先将所需要的蒸馏装置均准备齐全(如上仪器),先从热源(酒精灯)处开始,然后“由下而上,由左到右”。在一铁架台上,依次由下往上安放热源、石棉网、烧杯(内盛放大半杯的自来水)、烧瓶(内盛放20ml的工业酒精,再加入2-3颗沸石)以及温度计;再从左到右接上冷凝管,用另一个铁架台将冷凝管中间夹住以固定,再接上接引管,将接引管通入锥形瓶中,在冷凝管上接上两根胶管,下端接到水源上,上端放入水槽中。整个装置要求准确端正,无论从正面还是侧面观察,全套仪器中各个仪器的轴线都要在同一水平面内;所有的铁夹和铁架都应尽可能整齐地放在仪器的背部。
3、开始试验。首先用打火机点燃酒精灯,调整铁台的高度,用酒精灯的外焰给烧杯加热,直到通过水浴加热使烧瓶中的酒精开始沸腾并有液体馏出,开始调整酒精灯的高度,使液体馏出速度为每秒钟1-2滴为宜,当速度趋于平衡时,用计时器开始计时,此时,并重新换一个锥形瓶来接收馏出液体,并记录下此时的温度。通过观察锥形瓶中馏出液体的体积,当差不多达到有2ml时,再换上另一个锥形瓶收集,并记录下此时的时间以及蒸馏气体的温度,用量筒量出换下来的馏出液体的体积并记录。就这样反复收集记录,待到烧瓶中的工业酒精差不多蒸馏完全,灭掉酒精灯,停止实验。
4、将所用的蒸馏仪器拆下来,用水洗干净,放会之前去的地方,注意别将玻璃仪器弄坏。再将实验桌面打理干净。
五.数据记录及其处理
乙醇的蒸馏数据记录

图一:

图二:
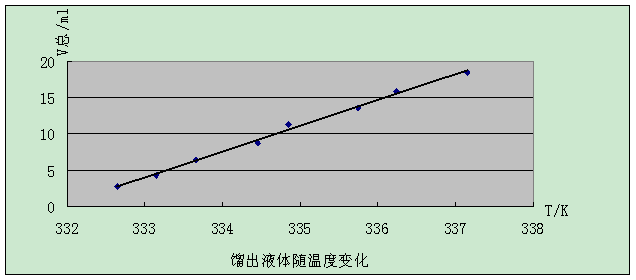
六.实验结果
由上表可以知道:V总=18.5ml
所以其回收率为:u= (V总/20)╳100%
代入数据得 u=(18.5/20) ╳100%=92.5%
七.问题讨论
1.常量法蒸馏与微量法测沸点个适用于那些情况?在高原地区蒸馏时,对沸点是否有影响?偏低还是偏高?
答:微量法一般用于现场监控,对数据准确度要求不高,但是可以监控数据的变化,当提供的液体不足以作沸点的常规测定时一般用微量法。常量法一般用于液体足够时的一般测量。在高原地区沸点会受一定影响,使沸点偏低。
2.为什么蒸馏时要加沸石?若加热时发现未加沸石,为什么一定要冷却后才能补加?
答:加沸石防止暴沸,如果不冷却就加入沸石,会引起严重的暴沸,部分液体会冲出瓶外,如是易燃物,可能引起火灾。
3.如果液体有一恒定沸点,能否认为是纯物质?液体中含有水分,一般引起沸点上升还是下降?
答:不能。一些混合物也有恒定的沸点,比如一些盐的水溶液,乙醇水溶液等。液体中含有水分,其沸点一般会下降。根据道尔顿分压定律,当不溶于水的有机物与水混合在一起时,整个体系的蒸汽压P=PH2O+P,此时混合物各组分的总压大于和等于外界大气压,混合物开始沸腾,这时的温度必小于任一组分的沸点。
