实验十乙酸正丁酯的制备
Experiment 10 Preparation of n-butyl acetate
[教学目的]
1、巩固酯化反应的原理。
2、掌握分水器的用法。
[教学内容]
一、基本原理
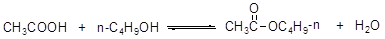
二、实验仪器及药品
仪器:50 mL单口烧瓶,球型冷凝管,分水器,分液漏斗,锥形瓶,直型冷凝管,尾接管;
药品:正丁醇,冰醋酸,浓硫酸,10 %Na2CO3溶液,无水MgSO4.
三、实验内容
1、50 mL圆底烧瓶中,加11.5 mL (0.125 mol) n-BuOH, 7.2 mL CH3COOH (0.125 mol) 和3-4d浓H2SO4(催化反应), 混匀,加2颗沸石。
2、接上回流冷凝管和分水器。在分水器中预先加少量水至略低于支管口(约为1~2 cm),目的:使上层酯中的醇回流回烧瓶中继续参与反应,用笔作记号并加热至回流,不需要控制温度,控制回流速度1~2d/s。
3、反应一段时间后,把水分出并保持分水器中水层液面在原来的高度。
4、大约40 min后,不再有水生成 (即液面不再上升),即表示完成反应。
5、停止加热,记录分出的水量。
6、将分水器分出的酯层和反应液一起到入分液漏斗中,用10 mL水洗涤,并除去下层水层(除去乙酸及少量的正丁醇);有机相继续用10 mL混合物 10mL H2O 有机相(上层)10mL1有机相(上层) 10 mL 10%Na2CO3 洗涤至中性(除去硫酸);上层有机相再用10 mL 的水洗涤除去溶于酯中的少量无机盐,最后将有机层到入小锥形瓶中,用无水可硫酸镁干燥。
7、蒸馏:将干燥后的乙酸正丁酯滤入50 mL 烧瓶中,常压蒸馏,收集124-126 ℃的馏分。
8、计算产率。
四、实验步骤关键和注意事项
1、注意保持分水器中水层液面高度
2、通过分水器中的水面变化判断反应终点
3、根据分出的水量计算反应产率
五、主要试剂及产品的物理常数(文献值)
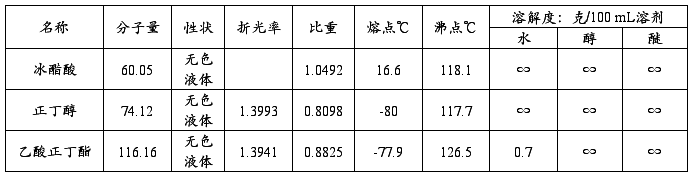
思考题:
1、实验报告
1、酯化反应有什么特点,本实验如何提高产品收率?又如何加快反应速度?
2、计算反应完全应分出多少水?
预习:茶叶中提取咖啡因
第二篇:实验十:乙酸正丁酯的制备报告模版
实验十:乙酸正丁酯的制备
一、实验目的
1.学习羧酸与醇反应制备酯的原理和方法。
2.学习利用恒沸去水以提高酯化反应收率的方法。
3.学习使用分水器回流去水的原理和使用方法。
二、实验原理
主反应式:
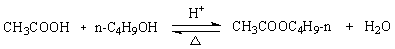
副反应式:
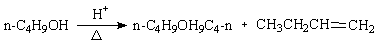
三、主要试剂及产品的物理常数:(文献值)
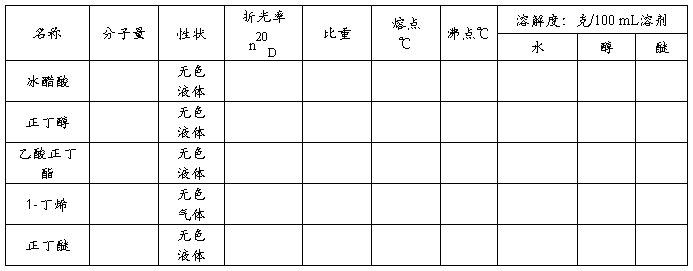
乙酸正丁酯、水及正丁醇形成二元或三元恒沸液的组成及沸点
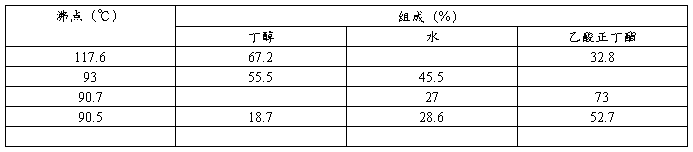
四、实验装置图
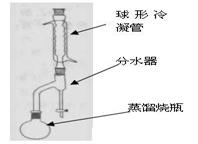
五、操作流程
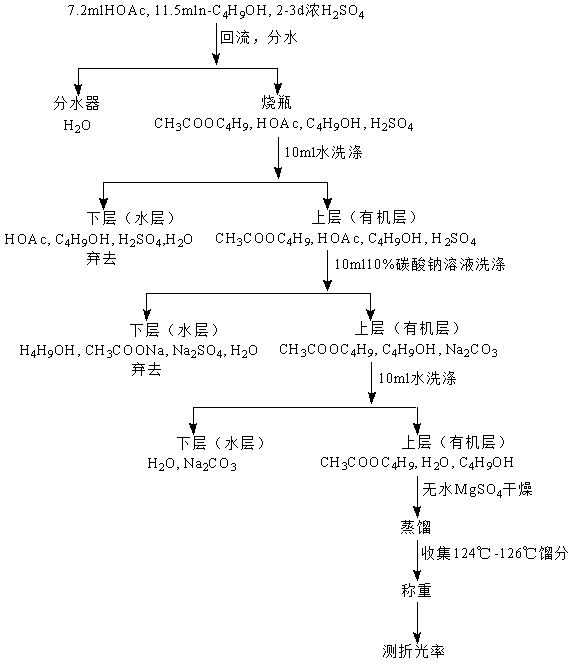
六、思考题
3、问题讨论
1)酯化反应有哪些特点?本实验是根据什么原理来提高乙酸正丁酯产率??又如何加快反应速度?
答:该反应为可逆的,增加某一反应物的量(采用丁醇过量),并使用分水器通过恒沸原理将水除去,破坏反应平衡,提高乙酸丁酯的产率。
2)在提纯粗产品的过程中,用碳酸钠溶液洗涤主要除去哪些杂质?若改用氢氧化钠溶液是否可以?为什么?
实验步骤
1)50 mL圆底烧瓶中,加11.5 mL (0.125 mol) n-BuOH, 7.2 mL CH3COOH (0.125 mol) 和3-4d浓H2SO4(催化反应), 混匀,加2颗沸石。
2)接上回流冷凝管和分水器。在分水器中预先加少量水至略低于支管口(约为1~2 cm),目的是使上层酯中的醇回流回烧瓶中继续参与反应,用笔作记号并加热至回流,不需要控制温度,控制回流速度1~2d/s。
3)反应一段时间后,把水分出并保持分水器中水层液面在原来的高度。
4)大约40 min后,不再有水生成 (即液面不再上升),即表示完成反应。
5)停止加热,记录分出的水量。
6)将分水器分出的酯层和反应液一起到入分液漏斗中,用10 mL水洗涤,并除去下层水层(除去乙酸及少量的正丁醇);有机相继续用10 mL混合物 10mL H2O 有机相(上层)10mL1有机相(上层) 10 mL 10%Na2CO3 洗涤至中性(除去硫酸);上层有机相再用10 mL 的水洗涤除去溶于酯中的少量无机盐,最后将有机层到入小锥形瓶中,用无水可硫酸镁干燥。
7)蒸馏:将干燥后的乙酸正丁酯滤入50 mL 烧瓶中,常压蒸馏,收集124-126 ℃的馏分。
8)计算产率,测折光率。
实验关键及注意事项
1)在加入反应物之前,仪器必须干燥。(为什么?)
2)高浓度醋酸在低温时凝结成冰状固体(熔点16.6℃)。取用时可温水浴热使其熔化后量取。注意不要碰到皮肤,防止烫伤。
2)浓硫酸起催化剂作用,只需少量即可。也可用固体超强酸作催化剂。
3)本实验体系中,二元恒沸混合物有:正丁醇-水,共沸点93.0℃;乙酸正丁酯-水,共沸点90.7℃; 乙酸正丁酯-正丁醇,共沸点117.6℃。三元恒沸混合物有:乙酸正丁酯-正丁醇-水,共沸点90.7℃。在反应进行的不同阶段,利用不同的共沸物可把水带出体系,经冷凝分出水后,醇、酯再回到反应体系。为了使醇能即时回到反应体系中参加反应,在反应开始前,在分水器中应先加入计量过的水,保持油层厚度不变。分水器的旋塞应事先涂润滑脂。加热时,旋塞不要受热,否则旋塞难以转动。
4)洗涤操作(分液漏斗的使用):
(1)洗涤前首先检查分液漏斗旋塞的严密性。
(2)洗涤时要做到充分轻振荡,切忌用力过猛,振荡时间过长,否则将形成乳浊液,难以分层,给分离带来困难。一旦形成乳浊液,可加入少量食盐等电解质或水,使之分层。
(3)振荡后,注意及时打开旋塞,放出气体,以使内外压力平衡。放气时要使分液漏斗的尾管朝上,切忌尾管朝人。
(4)振荡结束后,静置分层;分离液层时,下层经旋塞放出,上层从上口倒出。
5)回流速度的控制及反应终点的判断:反应终点的判断可观察下面两种现象:一是分水器中不再有水珠下沉;二是从分水器中分出的水量达到理论分水量,即可认为反应完成。
6)干燥必须完全,否则由于乙酸丁酯与丁醇,水等形成二元或三元恒沸液,重蒸馏时沸点降低,影响产率。
、折光率
