

实验三 最大压差法测表面张力
一、实验目的
1.掌握最大压差法测定表面张力的原理及方法;
2.测定正丁醇水溶液的表面张力,了解表面张力的概念及影响因素;
3.学习Gibbs公式及其应用。
二、实验原理
在一定温度、压力下纯液体的表面张力是定值。但在纯液体中加入溶质,表面张力就会发生变化。若溶质使液体的表面张力升高,则溶质在溶液相表面层的浓度小于在溶液相内部的浓度;若溶质使液体的表面张力降低,则溶质在溶液相表面层的浓度大于在溶液相内部的浓度。这种溶质在溶液相表面的浓度和相内部的浓度不同的现象叫吸附。
在一定的温度、压力下,溶质的表面吸附量与溶液的浓度、溶液的表面张力之间的关系,可用吉布斯(Gibbs)吸附等温式表示:
Γ=-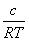
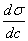 (2-1)
(2-1)
若dσ/dc<0,溶质为正吸附;若dσ/dc>0,溶质为负吸附。通过实验若能测出表面张力与溶质浓度的关系,则可作出σ—c曲线,并在此曲线上任取若干个点作曲线的切线,这些曲线的斜率即为浓度对应的dσ/dc,将此值代人2—1式可求出在此浓度时的溶质吸附量。
测定液体表面张力的方法有许多种。本实验采用最大压差法。测定装置如图1所示。
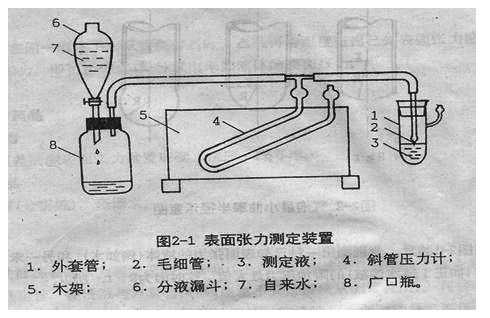
图1:测定装置图
测定时,仪器内压力增加,气泡即可通过毛细管(要求它的尖嘴刚刚与液面接触)。从浸入液面的毛细管端鼓出空气泡时,需要高出外部大气压的附加压力,以克服气泡表面张力。如果毛细管半径很小,则形成的气泡基本上是球形的。此时附加压力与表面张力成正比,与气泡的曲率半径成反比,其关系式如下:
ΔP=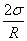 (2—2)
(2—2)
当气泡开始形成时,表面几乎是平的,这时曲率半径最大,随着气泡的形成,曲率半径逐渐变小,直到形成半球形,这时曲率半径与毛细管半径r相等,曲率半径达最小值,这时附加压力达最大值。气泡进一步长大,R变大,附加压力则变小,直到气泡溢出。
分别测出一种已知表面张力的液体(如水)和另一未知表面张力液体(如正丁醇水溶液)的附加压力最大值,这时因为B=r,所以,
ΔP1=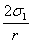 (2—3)
(2—3)
ΔP2=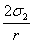 (2—4)
(2—4)
因为两种液体的最大附加压力(即最大压差)是在同一仪器的同一毛细管测的。所以,上两式的r是相同的,若将r消去即得:
σ2=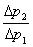 ﹒σ1 (2—5)
﹒σ1 (2—5)
因此,在同一温度下,只要测得ΔP1、ΔP2,再由温度查出已知表面张力液体(水)的表面张力;即可由公式(2—5)求出未知液体的表面张力。
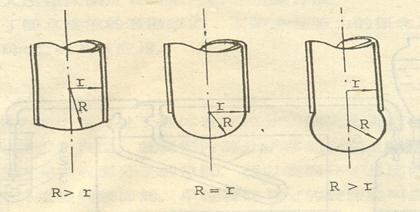
图 2-2 气泡最小曲率半径示意图
三、仪器与药品
1.仪器
最大压差法测表面张力装置一套,洗瓶,洗耳球。
2.药品
正丁醇(分析纯),蒸馏水。
四、实验步骤
1.用洗液洗表面张力测定仪的外套和毛细管。方法是在外套管中放入少量洗液,倾斜转动外套管,使洗液管接触(不要让洗液从侧管流出),再将毛细管插入,这时保持外套管倾斜不动,转动毛细管,使洗液与毛细管接触,再用洗耳球吸洗液至毛细管内,洗毛细管内壁,用完的洗液倒回原来瓶中,然后用自来水充分洗外套管和毛细管,最后用蒸馏水冲洗外套管和毛细管各三次。
2.在外套管中放入蒸馏水,将毛细管插入外套管,塞紧塞子,并使毛细管尖端刚碰到液面。读出斜管压计下面一根管内的零点液位h。。
3.打开分液漏斗的活塞,使分液漏斗中的水慢慢滴入广口瓶中,这时瓶内压力逐渐增加,气泡将通过毛细管端。
从斜管压力计读出第一个气泡通过毛细管端时的最高液位h1,如此重复三次,测三个平行数据,取平均值得h2.
4.测完蒸馏水的最大压差后,倒掉蒸馏水,用0.02mon/L的正丁烷洗一次外套管然后再加入该溶液,像测蒸馏水的最大压差一样,测定该溶液的最大压差。依次测的0.05、0.10、0.15、0.20、0.25、0.30、0.35mon/L的正丁烷溶液的最大压差。
5.记录实验温度。
五、结果处理
1.由附录二查出实验温度下蒸馏水的表面张力。
答:查表可知,当t=21°C时,σ(H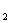 O)=72.59mN/m。
O)=72.59mN/m。
2.由公式σ2=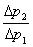 ﹒σ1 计算出不同浓度正丁醇溶液的表面张力,用表格的形式列出计算结果,并取一组数据附一计算实例。
﹒σ1 计算出不同浓度正丁醇溶液的表面张力,用表格的形式列出计算结果,并取一组数据附一计算实例。
3.以表面张力为纵坐标,以浓度为横坐标,画出正丁醇溶液σ—c图。
表1 最大压差测量表面张力数据处理表
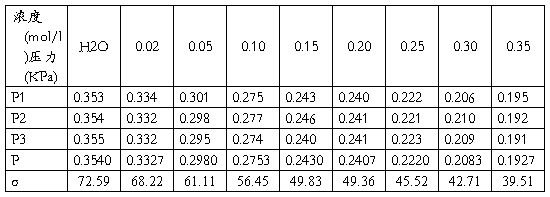
数据处理:
查表 得 水在21℃时的表面张力为72.59mN/m
水 Pw=(P1+P2+P3)/3=0.3540 cm
取 浓度为 0.02mol/L的 正丁醇为例
平均最大压强差 P=(P1+P2+P3)/3=0.3327 cm
σ2=P/Pw×σ1=68.22mN/m
同理 可以得到其他几组数据
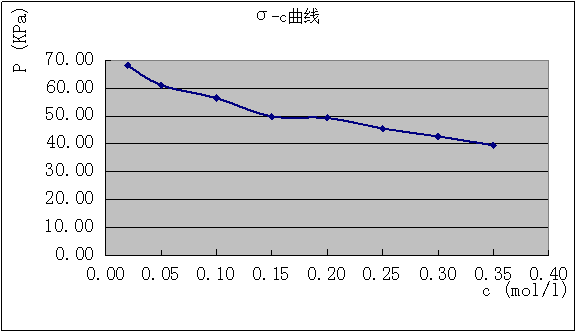
画出σ-c 图表
图1 σ-c曲线
4.在σ—c图上选若干点,做不同浓度曲线时切线,以Gibbs公式(2-1)求出相应的表面吸附量;并在坐标纸上画出正丁醇溶液的吸附等温线。
表2 表面吸附量计算表
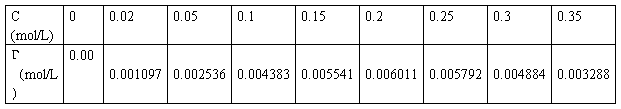
数据处理:取第三组数据进行计算
将下列数据带入公式2-1中
C=0.05mol/L T=294.15K dσ/dc= -124.019 R=8.314 N×m/(K×mol)
得
Γ=0.002536mol/L
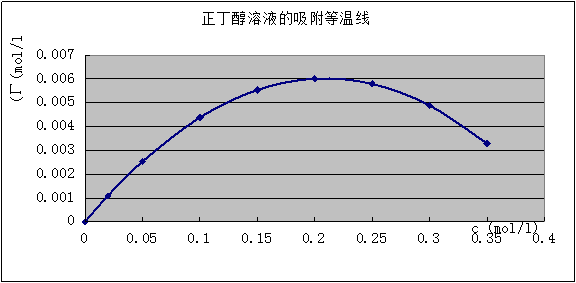
根据8组数据作出正丁醇吸附等温线
图2 表面吸附量与浓度关系曲线
六、思考题
1.实验中,如果毛细管深入液面1mm会造成多大误差?
答:根据液体中压力的公式,P=ρgh可以算得,1mm水产生的压力约为9.8Pa,因此,测得的压力差会比实验值大9.8Pa。
2.实验中,为什么要尽量放慢鼓泡速度?
答:因为测量的仪器会有一定的反应时间,放慢鼓泡速度可以测量更多组数据,并且给仪器足够的反应时间,使实验精度升高。
3.实验中,为什么要求从稀到浓逐个测定不同浓度溶液的表面张力?
答:如果从浓到稀测定,前一毛细管上残留的较高浓度的正丁醇会对低浓度的正丁醇的测定造成较大影响,从而影响实验结果。
4.解释σ—c曲线的趋势。
答:随浓度的增加表面张力逐渐减小,并且切线斜率随着浓度的增大而逐渐减小,切线方向最终逐渐趋于水平,曲线无限趋近于某一值。
5.实验中,影响表面张力测定准确性的因素有哪些?
答:影响因素有,实验装置的气密性是否良好,实验环境的温度变化,溶液浓度是否准确,做多组实验使用不同浓度的溶液之间的互相影响等等。
第二篇:石工12-11班+120xx523+赵润达最大压差法测表面张力+27

实验二最大压差法测表面张力
一.实验目的
1.掌握最大压差法测定表面张力的原理及方法;
2.测定正丁醇水溶液的表面张力,了解表面张力的概念及影响因素;
3.学习 Gibbs 公式及其应用。
二.实验原理
由于净吸引力的作用,处于液体表面的分子倾向于到液体内部来,因此液体表面倾 向于收缩。要扩大面积,就要把内部分子移到表面来,这就要克服净吸引力作功,所作 的功转变为表面分子的位能。单位表面具有的表面能叫表面张力。
在一定温度、压力下纯液体的表面张力是定值。但在纯液体中加入溶质,表面张力 就会发生变化。若溶质使液体的表面张力升高,则溶质在溶液相表面层的浓度小于在溶 液相内部的浓度;若溶质使液体的表面张力降低,则溶质在溶液相表面层的浓度大于在 溶液相内部的浓度。这种溶质在溶液相表面的浓度和相内部的浓度不同的现象叫吸附。 在一定的温度、压力下,溶质的表面吸附量与溶液的浓度、溶液的表面张力之间的
关系,可用吉布斯(Gibbs)吸附等温式表示:
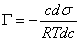
式中 Γ -吸附量(mol/L);
c-吸附质在溶液内部的浓度(mol/L);
σ -表面张力(N/m);
R-通用气体常数(N.m/K.mol);
T-绝对温度(K)。
若 dσ /dc<0,溶质为正吸附;若 dσ /dc>0,溶质为负吸附。通过实验若能测出表 面张力与溶质浓度的关系,则可作出σ -c 曲线,并在此曲线上任取若干个点作曲线的 切线,这些曲线的斜率即为浓度对应的 dσ /dc,将此值代入 2-1 式可求出在此浓度时 的溶质吸附量。
测定液体表面张力的方法有许多种。本实验采用最大压差法,测定装置如图所示。
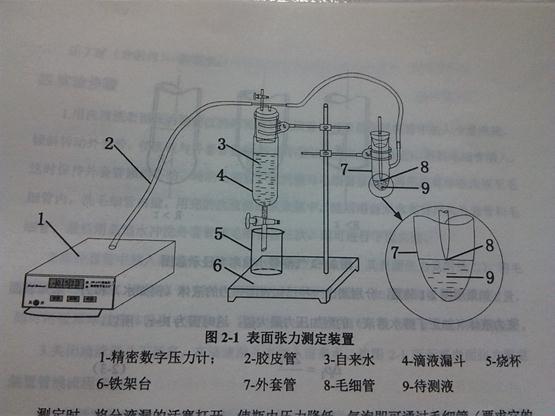
图2-1 表面张力测定装置
测定时,将分液漏的活塞打开,使瓶内压力增加,气泡即可通过毛细管(要求它的尖嘴刚刚与液面接触)。从浸入液面的毛细管端鼓出空气炮时,需要高出外部大气压的 附加压力,以克服气泡表面张力。如果毛细管半径很小,则形成的气泡基本上是球形的(图 2-2)。此时附加压力与表面张力成正比,与气泡的曲率半径成反比,其关系式如下:
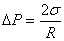
式中 Δ P-广口瓶内滴水形成的附加压力;
R-气泡的曲率半径;
σ-表面张力(N/m)。
当气泡开始形成时 ,表面几乎是平的,这是曲率半径最大,随着气泡的形成,曲 率半径逐渐变小,直到形成半球形,这是曲率半径与毛细管半径 r 相等,曲率半径达最 小值,根据 2-2 式,这时附加压力达最大值。气泡进一步长大,R 变大,附加压力则变 小,直到气泡溢出。
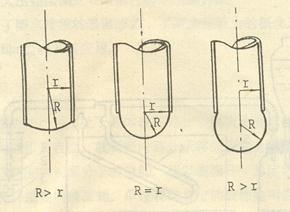
图 2-2 气泡最小曲率半径示意图
如果用图 2-1 装置,分别测出一种已知表面张力的液体(例如水)和另一未知表面 张力液体(如正丁醇水溶液)的附加压力最大值,这时因为 R=r,所以,
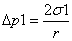
式中:
Δp1 -已知表面张力液体的最大附加压力;
σ1- 已知液体的表面张力。
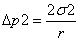
式中:
Δp2 -未知表面张力液体的最大附加压力;
σ2- 未知液体的表面张力。
因为两种液体的最大附加压力(即最大压差)是在同一仪器的同一毛细管测的。所以,上两式的 r 是相同的,若将 r 消去即得:
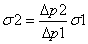
因此,在同一温度下,只要测得ΔP1、ΔP2,再由温度查出已知表面张力液体(水)的表面张力;即可由公式(2-5)求出未知液体的表面张力。
三.仪器与药品
1.仪器
最大压差法测表面张力装置一套,洗瓶,吸耳球。
2.药品
正丁醇(分析纯),蒸馏水。
四.步骤
1.用洗液洗表面张力测定仪的外套管和毛细管。方法是在外套管中放入少量洗液, 倾斜转动外套管,使洗液与外套管接触( 注意不要让洗液从侧管流出 ).再将毛细管插入, 这时保持外套管倾斜不动,转动毛细管,使洗液与毛细管接触,再用洗耳球吸洗液至毛细 管内,洗毛细管内壁.用完的洗液倒回原来瓶中,然后用自来水充分冲洗外套管和毛细管, 最后用蒸馏水冲洗外套管和毛细管各三次,即可进行下面实验;
2.在外套管中放入蒸馏水(作为已知表面张力的液体,其表面张力见附录二),将毛 细管插入外套管,塞紧塞子,并使毛细管尖端刚碰到液面。读出斜管压差计下面一根管内 的零点液位 h0(此时斜管压力计两端都通大气);
3.关闭漏斗下活塞,分液漏斗中装满自来水。按图 2-1 所示装好仪器;
4.打开精密数字压力计电源,然后打开分液漏斗的活塞,将管线内压力放空。按精密数字压力器的采零按钮,使精密数字压力器的示数置零。
5.关闭滴液漏斗上活塞,缓缓打开滴液漏斗下活塞,使分液漏斗中的水慢慢滴入广口瓶中,这时瓶内压力逐渐增加,气泡将通过毛细管端匀速冒出。从精密数字压力计上读出最大压差,重复读取三次,将数据记录在实验记录纸上,取平均值。
6.测完蒸馏水的最大压差后,倒掉蒸馏水,用 0.02mon/L 的正丁醇洗一次外套管 和毛细管,然后再加入该溶液,象测蒸馏水的最大压差一样,测定该溶液的最大压差。 依次侧得 0.05、0.10、0.15、0.20、0.25、0.30、0.35mom/L 的正丁醇溶液的最大压差。
(注意:每更换一次溶液,都应用待定液洗外管套管和毛细管)。
7.记录实验温度.
五.结果处理
1.由附录-查出实验温度下蒸馏水的表面张力。
由公式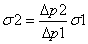 计算出不同浓度正丁醇溶液的表面张力,用表格的形式列出计算结果,并取一组数据附-计算实例。
计算出不同浓度正丁醇溶液的表面张力,用表格的形式列出计算结果,并取一组数据附-计算实例。
3.以表面张力为纵坐标,以浓度为横坐标,在坐标纸上画出正丁醇溶液的σ-c 图。
4.在σ-c 图上选若干点,作不同浓度曲线时切线,依 Gibbs 公式(2-1)求出相应 的表面吸附量;并在坐标纸上画出正丁醇溶液的吸附等温线。

表1.原始数据表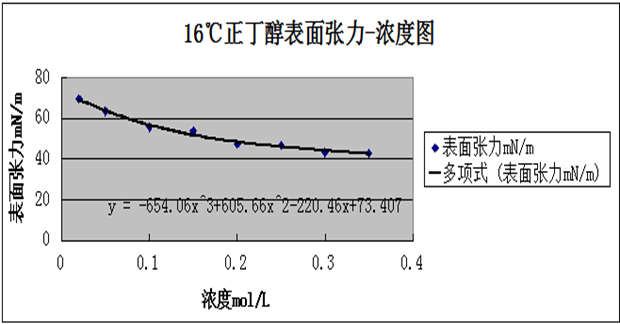

表2. 289K正丁醇的表面张力-吸附量表
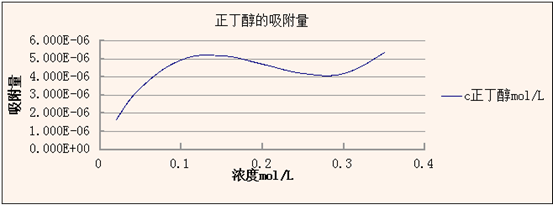
误差分析:因为我们的分液漏斗的活塞稍微有点点漏液,所以造成了一定误差。
六.思考题
1.实验中,如果毛细管深入液面 1mm 会造成多大误差?
答:会使最大附加压力增大很多。从而使表面张力增大很多。
按第一组数据分析1mm液体产生压强P=ρgh=9.8Pa
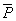 (H
(H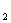 O)=0.351Kp
O)=0.351Kp 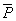 (正丁醇)=0.3428Kp
(正丁醇)=0.3428Kp
δ2=0.3428/0.351*73.34=71.62 相对误差=(71.62-69.70)/69.70=2.8%
.实验中会额外造成误差。
2.实验中,为什么要尽量放慢鼓泡速度?
答:为了让气泡逐渐形成,使曲率半径逐渐变小最后达到与毛细管半径相等,曲率半径达最小。鼓泡过快气泡来不及形成,达不到曲率半径最小,会造成实验测量误差。
3.实验中,为什么要求从稀到浓逐个测定不同浓度溶液的表面张力?
答:减少由于残留正丁醇对于浓度的影响而造成的实验误差,使实验更加的精确。
4.解释σ-c 曲线的变化趋势。
答:开始时,曲线变化速率很快,随浓度增加,变化速率逐渐变慢。因为,①当溶液极稀时,表面活性剂分子在溶液中的分布只有一种动平衡。由于浓度极稀,表面上表面活性剂分子彼此不影响,所以可平铺于液面。因此,表面活性剂对表面张力有显著影响。②由于表面活性剂分子在表面浓度增加,所以他们不能像极稀溶液情况下平铺,而是倾斜于液面,因此对表面张力的影响就减小,表现为表面张力随浓度增加而下降减小。③当浓度增至某一数值,表面活性剂在溶液表面吸附达到饱和,并紧密排列,活性分子开始向溶液内部分布。开始形成胶束。④在浓溶液中,表面活性剂动平衡关系不变,但胶束数量不断增加。变化趋势表现为十分平缓。
5.实验中,影响表面张力测定准确性的因素有哪些?
答:影响准确性的因素主要有仪器的气密性,毛细管与液面的接触距离,以及气泡是否缓慢的鼓出。
