课题:
《对过氧化氢分解速率影响因素的探究》
实验过后的反思
参评教师:淄川一中 于淑东
探究对过氧化氢分解反应速率的影响
新课程的设置中,提倡学生在实验中获得体验和知识的增长,但在具体教学中,由于实验时间过长、实验现象不明显、环境污染等问题的存在使得实验教学大打折扣,因此化学实验在保证实验效果的前提下,一定要直观、明显、省时、准确、安全。在此要求下, 本人采用“多步组合,化繁为简”的方法,对“双氧水分解反应速率影响因素”的实验进行了多项实验并进行了有效改进。
实验1:在不同温度下,用不同浓度过氧化氢进行实验,其实验结果见下表
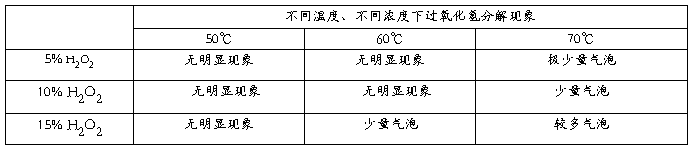
通过上述实验分析发现如下问题:
1. 浓度较低的5%和10%的双氧水即使加热到70℃分解现象也不明显,当将其浓度增加到15%时分解速率明显增加。
2. 常温条件下各种浓度双氧水的分解速率都很小,温度至少在70℃以上,但加热方式不宜使用酒精灯直接加热,这样虽然温度高,能加速过氧化氢的分解,但同时使水蒸发产生水蒸气,随氧气一起放出,影响实验结果。
改进方法:
1. 考虑到浓度不宜增加太多,选择浓度在15%的双氧水较适合。
2. 考虑水浴温度70℃加热时间过长,可以直接使用热水瓶中的水。
3. 在对比不同浓度的双氧水分解速率时可以同时使用0.4mol/LFeCl3溶液做催化剂,能缩短实验时间,对比现象明显。
温度对双氧水分解速率的影响实验(改进)

浓度对双氧水分解速率的影响实验

实验2:在不同催化剂对过氧化氢进行实验,其实验结果见下表

实验改进设想:
1. 将此实验由定性上升到定量。
2. 用医用一次性注射器和小药瓶代替分液漏斗和锥形瓶,省去了气密性的检验的麻烦而且能做到将液态一次性注入,时间上保证同步。
3. 量气装置化繁为简,由在量气管中气泡上升的高度决定。
催化剂对双氧水分解速率的影响(改进)

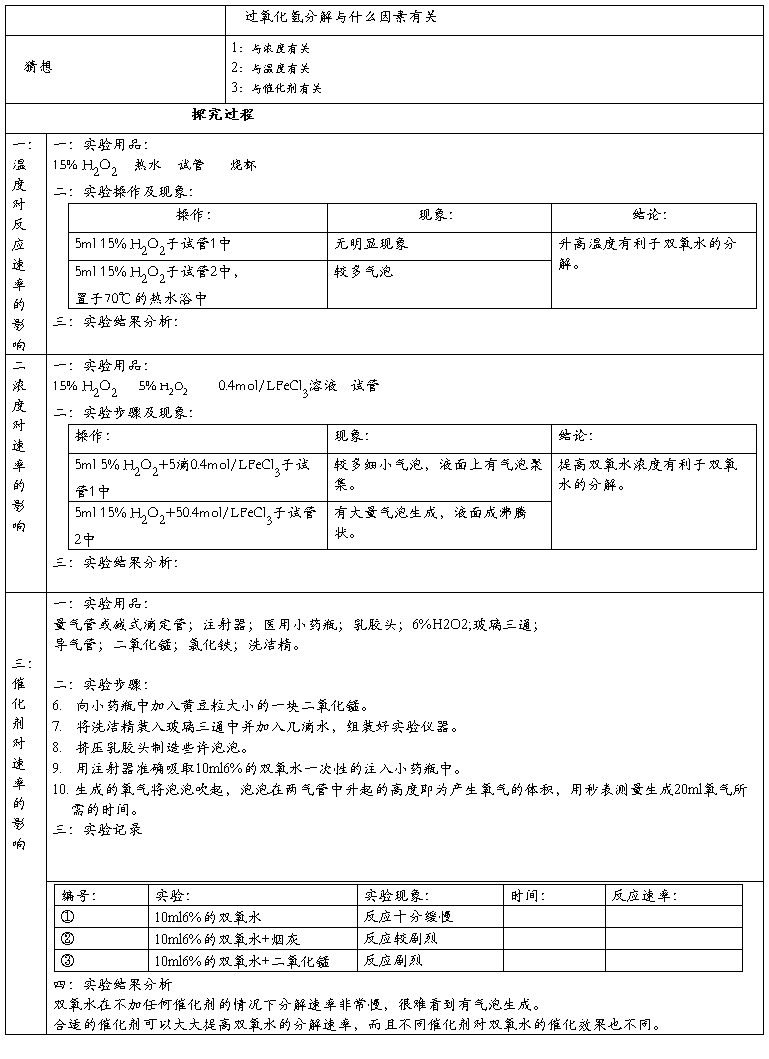
实验报告
探究实验名称:影响过氧化氢分解反应速率的因素。
探究实验目的:了解影响化学反应速率的因素,学会对比实验操作,提供实验能力。
第二篇:过氧化氢催化分解
实验七 过氧化氢催化分解
Catalyzed Decomposition of Hydrogen Peroxide
实验类型:基础性
实验学时:5
教学对象:临床药学专业
一.实验目的
1. 熟悉一级反应的特点,了解浓度、温度、催化剂等因素对反应速率的影响。
2. 用量气法测定过氧化氢分解反应的速率常数和活化能。
二.实验原理
过氧化氢的催化分解是一级反应:
H2O2 → H2O + 1 / 2 O2
ln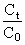 =–kt (3-1)
=–kt (3-1)
在分解过程中,放出的氧气的体积与分解了的H2O2浓度成正比:
C0 ∝ V∞
Ct ∝(V∞–Vt)
代入式(3-1),整理后可得:
ln(V∞–Vt)=–kt + ln V∞
用ln(V∞–Vt)对t作图,从直线的斜率可求出速率常数k,由两个不同温度的k值可以求出活化能Ea:

三. 实验准备
1. 仪 器:恒温槽,量气管装置,锥形瓶,移液管,秒表。
2. 药 品:3%H2O2溶液,KI溶液(0.1mol·mol–3)。
四.仪器安装要点
【插入录像】 安装量气管装置
五.操作要点(各实验步骤中的操作关键点)
1. 在量气管内读数时,一定要使水位瓶和量气管内液面保持同一水平。
2. 每次测定时振摇锥形瓶的速率要合适,且在测定过程中应恒定。
3. 过氧化氢溶液应该现用现配。
六.本实验的成败关键
1. 整个量气装置一定要不漏气。
2. 恒温槽的温度要恒定。
七.思考题及解答
(一)单选题
1. 本实验对反应物过氧化氢的级数为:
A. 一级 B. 二级 C. 三级 D. 零级
2. 本实验中V∞的测定是采用:
A. 加热法 B. 外推法 C. 内插法 D. 化学分析计算法
(二)判断题
1. 装配仪器后,一定要检查是否漏气。
2. 本实验所用的反应物过氧化氢一定要事先测出其准确浓度。
3. 用ln(V∞–Vt)对t作图,从图形的形状可以判断反应的级数。
答案:单选题:1 A 2 A 判断题:1 (对)2 (错)3(对)
执笔人:向阳
