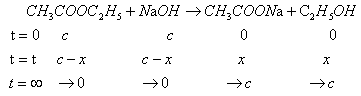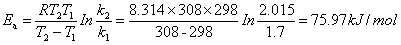电导法测定乙酸乙酯皂化反应的速率常数
一.目的要求
1.了解二级反应的特点,学会用图解计算法求取二级反应的速率常数.
2.用电导法测定乙酸乙酯皂化反应的速率常数,了解反应活化能的测定方法.
二.基本原理
乙酸乙酯皂化是一个二级反应,其反应式为:

在反应过程中,各物质的浓度随时间而变.某一时刻的OH-离子浓度可用标准酸进行滴定求得,也可通过测定溶液的某些物理性质而得到.用电导仪测定溶液的电导值G随时间的变化关系,可以监测反应的进程,进而可求算反应的速率常数.二级反应的速率与反应物的浓度的2次方有关.
若反应物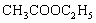 和NaOH的初始浓度相同(均设为c),设反应时间为t时,反应所产生的
和NaOH的初始浓度相同(均设为c),设反应时间为t时,反应所产生的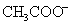 和
和 的浓度为x,若逆反应可忽略,则反应物和产物的浓度时间的关系为:
的浓度为x,若逆反应可忽略,则反应物和产物的浓度时间的关系为:

t=0 c c 0 0
t=t c-x c-x x x
t=∞ →0 →0 →c →c
上述二级反应的速率方程可表示为:
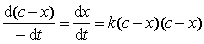 .........(11.1)
.........(11.1)
积分得:
 或
或  .........(11.2)
.........(11.2)
显然,只要测出反应进程中任意时刻t时的x值,再将已知浓度c代入上式,即可得到反应的速率常数k值.
因反应物是稀水溶液,故可假定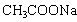 全部电离.则溶液中参与导电的离子有Na+、OH-和
全部电离.则溶液中参与导电的离子有Na+、OH-和 等,Na+在反应前后浓度不变,OH-的迁移率比
等,Na+在反应前后浓度不变,OH-的迁移率比 的大得多.随着反应时间的增加,OH-不断减少,而
的大得多.随着反应时间的增加,OH-不断减少,而 不断增加,所以体系的电导值不断下降.在一定范围内,可以认为体系电导值的减少量与
不断增加,所以体系的电导值不断下降.在一定范围内,可以认为体系电导值的减少量与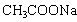 的浓度x的增加量成正比,即:
的浓度x的增加量成正比,即:
t=t x=β(G0 - Gt) .........(11.3)
t=∞ c=β(G0 - G∞) .........(11.4)
式中,G0和Gt分别是溶液起始和t时的电导值, G∞为反应终了时的电导值,β是比例系数.将(11.3)、(11.4)代入(11.2)得:
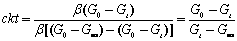 .........(11.5)
.........(11.5)
据上式可知,只要测出G0、G∞和一组Gt值,据(11.5)式,由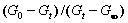 对t作图,应得一直线,从其斜率即可求得速率常数k值.
对t作图,应得一直线,从其斜率即可求得速率常数k值.
三.仪器与试剂
DDS-307型数字电导率仪 1台 恒温器 1套
秒表 1块 双管电导池 1个
移液管(20 mL) 2支 DJS-1型铂黑电极 1支
洗耳球 1只 NaOH(0.0100、0.0200 mol/L) 若干
CH3COONa(0.0100 mol/L) 若干 CH3COOC2H5(0.0200 mol/L) 若干
四.实验步骤
1.开启恒温水浴电源,将温度调至所需值(做两个相差10℃的温度下进行实验,低温应高于室温5℃以上!),如25℃/35℃或30℃/40℃。开启电导率仪的电源预热。
2. G0的测定
(1)洗净双管电导池并烘干,倒入适量0.01 mol/L NaOH溶液(以能浸没铂黑电极并高出1cm为宜)。
(2)用电导水洗涤铂黑电极,再用0.01 mol/L 溶液淋洗,然后插入电导池中。
(3)将安装好的双管电导池置于已恒温的水浴中恒温10分钟。
(4)测量溶液的电导(率)值,每隔2 min测量一次,共3次。
(5)更换0.01 mol/L NaOH溶液,重复(3)(4)两步测定.若两组数据的测量误差超出允许范围内,则必须再次重复测定,直至符合要求为止。
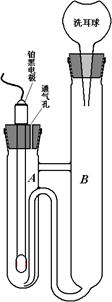
3.G∞的测定 图11.1 双管电导池
实验测定过程不可能进行到t=∞,且反应也并不完全可逆,故通常以0.01 mol/L 的CH3COONa溶液的电导(率)值作为G∞,测量方法与G0的测量方法相同。但必须注意,每次更换测量溶液时,须用电导水淋洗电极和电导池,再用被测溶液淋洗三次。
4.Gt的测定
(1)电导池和电极的处理方法与上述相同,安装后置于恒温浴中恒温.
(2)用移液管量准确取20 mL 0.0200 mol/L NaOH溶液放入洗净并干燥的电导池的A管,盖上装好电导电极的橡皮塞; 用另一支移液管吸取20 mL 0.0200 mol/L CH3COOC2H5溶液注入电导池的B管中,盖上带洗耳球的橡皮塞,置于恒温水浴中恒温至少10 min。
(3)用洗耳球从B管压气,将CH3COOC2H5溶液快速压入A管中,溶液压入一半时,开始记时,并继续压气,将B管中的溶液全部压入A管,放手,让洗耳球将A管中的溶液吸入B管,约到一半时,再用力压洗耳球,使B管中溶液再次全部进入A管.如此反复几次,使溶液光天化日之下均匀,并立即测量溶液的电导(率)值.压气时注意不要使溶液冲出!
(4)每隔1 min测量一次,直至电导(率)值基本不变为止。除记录第一个数据的外,其它各数据在测量时,应该尽量保持在整数分钟时测定,以便于进行数据处理。整个反应约需时45 min~1 h。
(5)反应结束后,倒掉反应液,洗净电导池和电导电极.按步骤3方法重新测量G∞,若所得结果与前次基本一样,则可进行下一步实验。
5.反应活化能的测定
按前述各步,重新测定另一温度下的反应速率常数,按阿仑尼乌斯(Arrhenius)公式计算反应的活化能:
 或
或  .........(11.6)
.........(11.6)
式中,k1、k2分别是温度T1、T2时反应的速率常数,Ea即为反应的活化能。
第二篇:实验18 电导法测定乙酸乙酯皂化反应的速率常数
班别:化工本101
学好:1011401107
姓名:邓建杰
实验18 电导法测定乙酸乙酯皂化反应的速率常数... 1
一、目的要求... 1
二、基本原理... 1
三、仪器与试剂... 3
四、实验步骤... 4
1.仪器预热... 4
2.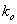 的测定... 4
的测定... 4
3. 的测定... 4
的测定... 4
4.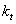 的测量... 5
的测量... 5
5.反应活化能的测定... 5
五、数据处理... 5
实验18 电导法测定乙酸乙酯皂化反应的速率常数
一、目的要求
(1)掌握电导法测定反应速率常数的原理和方法。
(2)了解二级反应的特点,学会用图解计算法求二级反应的速率常数。
(3)用电导法测定乙酸乙酯皂化反应的速率常数,了解反应活化能的测定方法。
二、基本原理
乙酸乙酯造化反应是一个二级反应,其反应式为
反应速率为
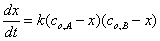 (2-18-1)
(2-18-1)
在反应过程中,各物质的浓度随时间而变。测定该反应体系组分浓度的方法很多,本本实验电导率仪测量造化反应进程中体系电导值G随时间的变化,从而达到跟踪反应物浓度随时间的变化目的,进而求算反应的速率常数。
若反应物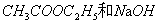 的初始浓度相同,设反应时间t时,反应所产生的
的初始浓度相同,设反应时间t时,反应所产生的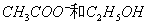 的浓度为x。若逆反应可忽略,则不同时刻反应物和产物浓度为
的浓度为x。若逆反应可忽略,则不同时刻反应物和产物浓度为
上述二级反应的速率方程克表示为
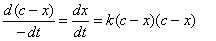 (2-18-2)
(2-18-2)
积分得
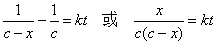 (2-18-3)
(2-18-3)
显然,只要测出反应进程中任意时刻t时的x值,再将已知浓度c 代入上式,即可得反应速率常数k值。
在一定范围内,可以认为体系电导率的减少量与的浓度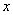 的增加量成正比 ,即
的增加量成正比 ,即
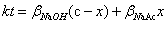 (2-18-4)
(2-18-4)
反应刚开始时,溶液的电导完全由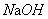 贡献,而反应完毕后全部由
贡献,而反应完毕后全部由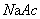 贡献,即
贡献,即
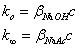 (2-18-5)
(2-18-5)
由式(2-28-4)—式(2-18-6)得
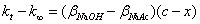 (2-18-7)
(2-18-7)
由式(2-18-5)—式(2-18-4)得
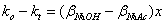 (2-18-8)
(2-18-8)
由式(2-18-8)/(2-18-7)得
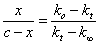 (2-18-9)
(2-18-9)
将式(2-18-9)代入式(2-18-3)得
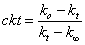 (2-18-10)
(2-18-10)
根据式(2-18-10)知,只要测出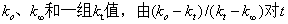 做图得到一条直线,从直线斜率即可求得速率常数
做图得到一条直线,从直线斜率即可求得速率常数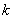 值。
值。
三、仪器与试剂
数字电导率仪 1台 恒温器 1套 秒表  1 块 双管电导池 1 个 移液管(2 0ml) 2支 铂黑电级 1支 洗耳球 1个 烧杯 5支
1 块 双管电导池 1 个 移液管(2 0ml) 2支 铂黑电级 1支 洗耳球 1个 烧杯 5支
四、实验步骤
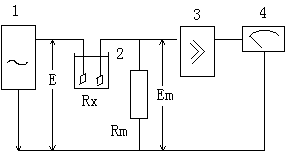
电导率仪测量原理图
1.仪器预热
开启恒温水浴电源,将温度调至所需值,开启电导率仪的电源,预热至少15min。
2.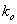 的测定
的测定
(1)洗净双管电导池并烘干,倒入适量0.0100mol/L的标准溶液。
(2)用电导水洗涤铂黑电极,在用标准溶液淋洗,然后插入电导池中。
(3)将安装好的双管电导池置于恒温水浴中恒温10min。
(4)更换标准溶液,重复(3)、(4)两步测定。
3. 的测定
的测定
实验测定过程不可能进行到时间最大,而且反应并不完全可逆,故通常以0.0100mol/L的标准溶液作为电导率,每次更换溶液测量时,需用电导水淋洗电极和电导池,再用被测液淋三次。
4.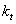 的测量
的测量
分别用移液管取10ml的0.0200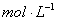
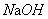 溶液及10ml的0.0200
溶液及10ml的0.0200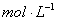 的乙酸乙酯溶液注入到两个试剂瓶中,盖紧盖子,以免挥发,然后置于恒温水槽中,恒温10~15min,然后将二瓶中的溶液迅速摇匀。注意当一个瓶中的溶液(例如
的乙酸乙酯溶液注入到两个试剂瓶中,盖紧盖子,以免挥发,然后置于恒温水槽中,恒温10~15min,然后将二瓶中的溶液迅速摇匀。注意当一个瓶中的溶液(例如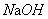 )倾入另一瓶中1/2十,开始计时,将电极插入反应溶液中,每隔5min测量一次电导率,测半个小时后停止。
)倾入另一瓶中1/2十,开始计时,将电极插入反应溶液中,每隔5min测量一次电导率,测半个小时后停止。
5.反应活化能的测定
按上述个步,重新测定另一温度下的反应速率常数,根据阿仑尼乌斯公式计算反应的活化能:
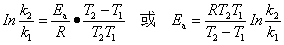
五、数据处理
1.测得25℃时的实验数据如表:
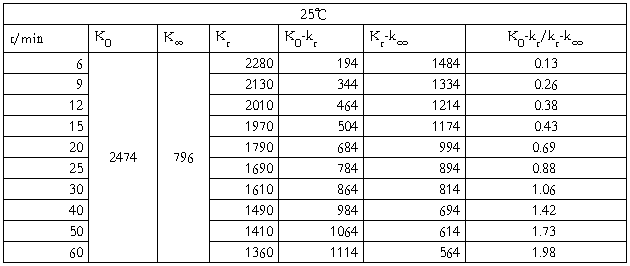
表1
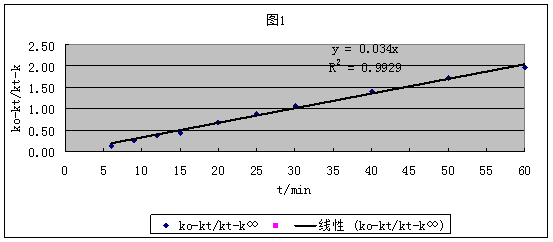
2.根据表1绘制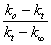 图得:
图得:
图1
3.由图1 可知直线斜率为0.034,则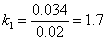
4. 测得35℃时的实验数据如表:
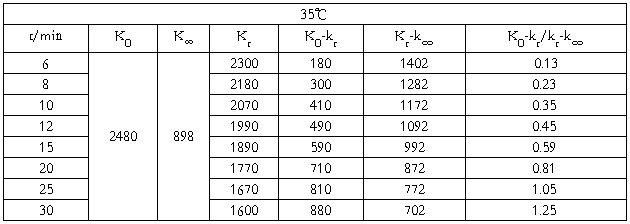
表2
5. 根据表2绘制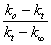 图得:
图得:
 图2
图2
6. 由图2 可知直线斜率为0.0403,则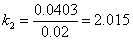
7. 根据阿仑尼乌斯公式计算反应的活化能:
实验18 电导法测定乙酸乙酯皂化反应的速率常数... 1
一、目的要求... 1
二、基本原理... 1
三、仪器与试剂... 3
四、实验步骤... 4
1.仪器预热... 4
2.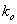 的测定... 4
的测定... 4
3. 的测定... 4
的测定... 4
4.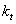 的测量... 5
的测量... 5
5.反应活化能的测定... 5
五、数据处理... 5