安全生产风险分析管理制度
一、 识别生产活动中的主要危险源
二、 每月组织一次安全生产风险分析会
三、 查找隐患、认真分析、分级管理、做好预警、提出超前防范
四、 按有关规定每月把风险分析结果上报上级有关部门
禹州平禹矿用产品有限公司
二0一四年二月十三日
第二篇:安全风险管理报告模板
医疗器械风险管理报告(有源医疗器械)
医疗器械风险管理报告 (XXX型XX诊断仪)
文件编号:
批准人:
批准日期:
医疗器械风险管理报告(有源医疗器械)
目录
第一章 综 述 ..................................................................................................................................................... 3
第二章 风险管理评审输入 ................................................................................................................................... 4
第三章 风险管理评审 ........................................................................................................................................... 8
第四章 风险管理评审结论 ................................................................................................................................... 6
附录1 ...................................................................................................................................................................... 1
附录2 ...................................................................................................................................................................... 5
附录3 ...................................................................................................................................................................... 1
附录4 ...................................................................................................................................................................... 1
2
医疗器械风险管理报告(有源医疗器械)
第一章 综 述
1、产品简介
XXX型XX诊断仪其工作原理、产品组成、产品功能??。
(产品外形示意图)
2、风险管理计划及实施情况简述
XXX型XX诊断仪于20XX年开始策划立项。立项同时,我们就针对该产品进行了风险管理活动的策划,制定了风险管理计划(文件编号:XXXX 版本号XX)。
该风险管理计划确定了XXX型XX诊断仪的风险可接受性准则,对产品设计开发阶段(包括试生产阶段)的风险管理活动以及生产和生产后信息的获得方法的评审要求进行了安排。
公司成立了风险管理小组,确定了该项目的风险管理负责人。确保该项目的风险管理活动按照风险管理计划有效的执行。
3、此次风险管理评审的目的
本次风险管理评审的目的是通过对XXX型XX诊断仪产品在上市前各阶段风险管理活动进行总体评价,确保风险管理计划已经圆满地完成,并且通过对该产品的风险分析、风险评价和风险控制,以及综合剩余风险的可接受性评价,证实产品的风险已进行了管理,并且控制的可接受范围内。
4、风险管理评审小组成员及其职责

3
医疗器械风险管理报告(有源医疗器械)
第二章 风险管理评审输入
1、风险可接受准则
见附件1。
2、风险管理文档
风险管理计划 文件编号:XXXX 版本号:XX
XXX型XX诊断仪安全性特征问题清单 文件编号:XXXX 版本号:XX
初始危害判断及初始风险控制方案分析 文件编号:XXXX 版本号:XX
风险评价表、风险控制措施记录表 文件编号:XXXX 版本号:XX
??
3、相关法规
??
关于执行GB 9706.1-2007《医用电气设备 第1部分:安全通用要求》有关事项的通知(国食药监械【2008】314号
??
4、相关标准
GB 9706.1-2007
GB 9706.25-1999
YY 0505-2005
??
5、相关文件和记录
风险管理控制程序 文件编号:XXXX 版本号:XX
产品设计开发文档(主要包括设计图纸、工艺、DFFEA表XXXX、PFMEA表XXXX等) ??
4
医疗器械风险管理报告(有源医疗器械)
第三章 风险管理评审
1、风险管理计划完成情况
评审小组对风险管理计划的完成情况逐一进行了检查,通过对相关风险管理文档的检查,认为XXX型XX诊断仪风险管理计划已经基本落实实施。
2、综合剩余风险可接受评审
评审小组对所有剩余风险进行了综合分析,考虑所有剩余风险共同影响下的作用,评审结果认为:产品综合剩余风险可接受。具体评价方面:
1)单个风险的风险控制是否有相互矛盾的要求?
结论:尚未发现现有风险控制有相互矛盾的情况。
2)警告的评审(包括警告是否过多?)
结论:警告的提示清晰,符合规范。
3)说明书的评审(包括是否有矛盾的地方,是否难以遵守)
结论:产品说明书符合10号令及产品专用安全标准要求,相关产品安全方面的描述清晰易懂,易于使用者阅读。
4)和同类产品进行比较
结论:通过与XXX公司的XXX型XX诊断仪进行的临床比较;以及与YYY公司的XXX型XX诊断仪进行性能、功能比较分析,认为产品与目前市场上反映较好的这两款机型从性能指标到功能及临床使用上是相同的。
5)与类似功能产品进行比较(必要时)
6)专家结论
结论:风险管理评审小组在分析了以上方面,并与临床应用专家进行了充分的沟通后,一致评价,本产品的综合剩余风险可接受。
3、关于生产和生产后信息
生产和生产后信息获取方法参见《风险管理控制程序》(文件编号:XXX版本号XX)中《生产和生产后信息获取方发表》。
评审组对《生产和生产后信息获取方发表》的适宜和有效性进行了评价,认为:该方法是适宜和有效的,XXX型XX诊断仪的生产和生产后信息的获取可使用此方法。
该项目风险管理负责人对得到的生产和生产后信息进行管理,必要时,风险管理小组开展活动实施动态风险管理。
5
医疗器械风险管理报告(有源医疗器械)
4、评审通过的风险管理文档
本次评审后最终确定的风险管理文档:
??
《XXX型XX诊断仪安全特征问题清单》 文件编号:XXXX 版本号:XXX(见附件2)
《初始危害判定和初始风险控制方案分析》 文件编号:XXXX 版本号:XXX(见附件3)
《风险评价、风险控制措施评价表》文件编号:XXXX
??
6 版本号:XXX(见附件4))
医疗器械风险管理报告(有源医疗器械)
第四章 风险管理评审结论
风险管理评审小组经过对XXX型XX诊断仪产品评审,认为:
-----风险管理计划已被适当地实施;
-----综合剩余风险是可接受的;
-----已有适当方法获得相关生产和生产后信息。
XXX型XX诊断仪全部剩余风险处于风险可接受准则的可接受范围内,且受益超过风险。同意批准XXX型XX诊断仪申报注册。
签名:
批准:
7
风险评价和风险可接受准则
附录1
风险评价和风险可接受准则
1 风险的严重度水平

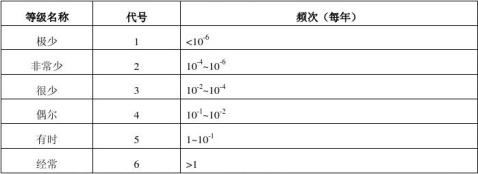
2 风险的概率等级
3 风险评价准则
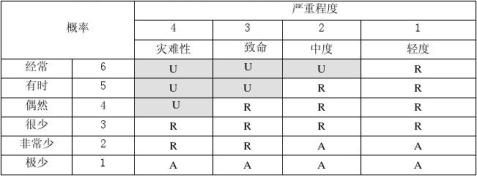
说明:A:可接受的风险;R:合理可行降低(ALARP)的风险;U:不经过风险/收益分析即判定为不可接受的风险。
1
1
安全问题的特征清单
附录2
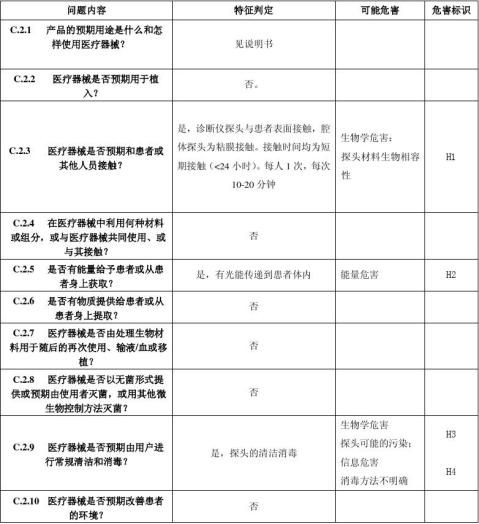
XXX型XX诊断仪安全特征问题清单
该清单依据YY/T0316-2008标准的附录C的问题清单,补充了有关XXX型XX诊断仪产品的特有的安全性问题。
1
安全问题的特征清单
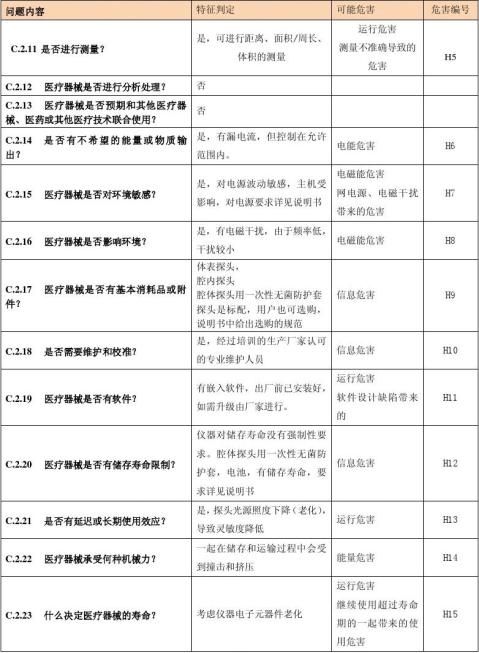
安全问题的特征清单
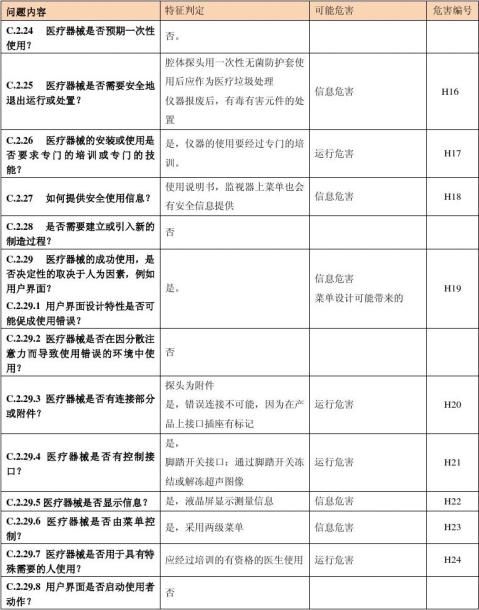
3
安全问题的特征清单
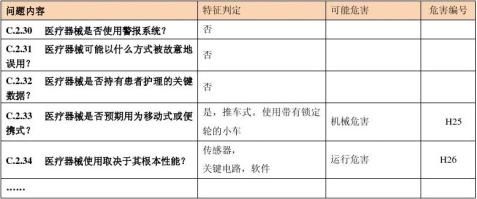
4
初始危害分析
附录3
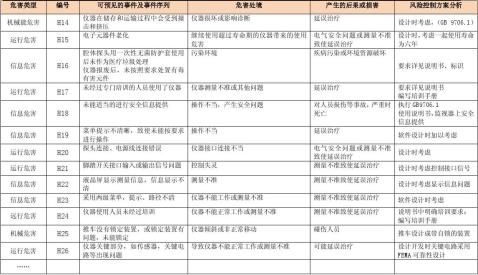
XXX型XX诊断仪的初始危害分析(PHA),包括可预见的事件序列、危害处境和可发生的损害及初始风险控制方案分析
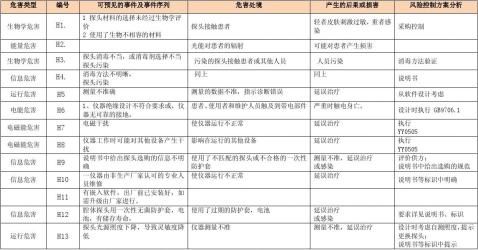
5
6
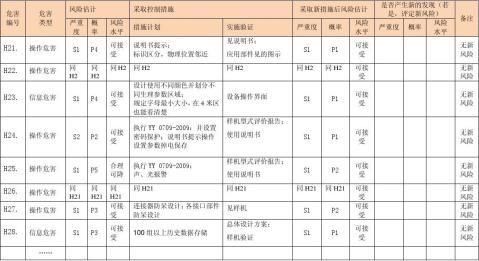
风险评价、风险控制措施记录表
附录4
风险评价、风险控制措施记录表
1
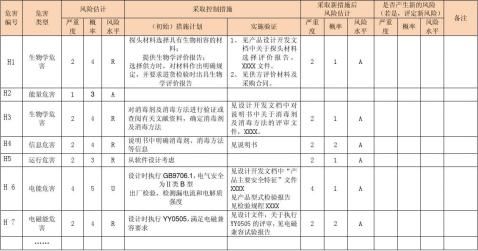
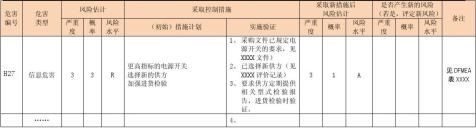
说明:
本报告仅作为医疗器械产品上市前,制造商的风险管理评审活动所形成的风险管理报告的案例。 本报告中斜体字表示提示内容要求。
本报告可以作为风险管理报告的模版,但制造商在使用时应考虑的特定要求。
2
风险评价、风险控制措施记录表
3
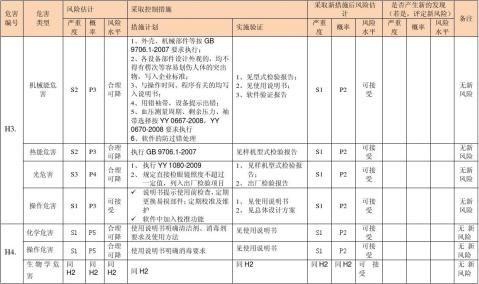
风险评价、风险控制措施记录表
4
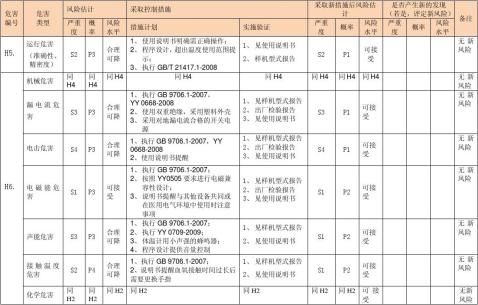
风险评价、风险控制措施记录表
5
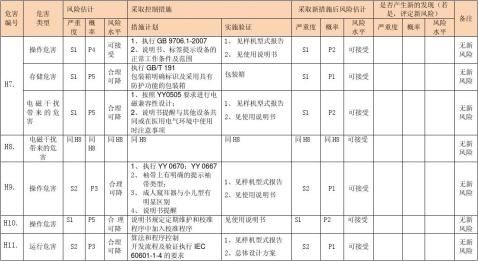
风险评价、风险控制措施记录表
6
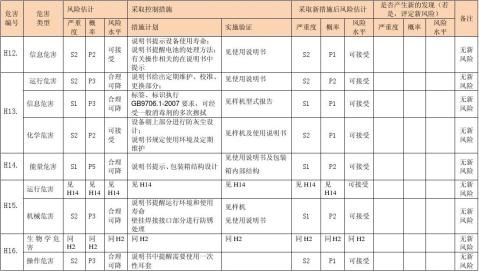
风险评价、风险控制措施记录表
7
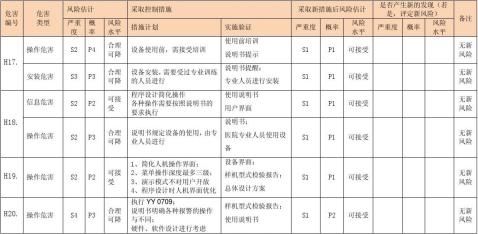
风险评价、风险控制措施记录表
8