二氧化碳的实验室制取与性质(学生实验课)
姓名:_______________ 组长:__________ 组员:________________________
试验时间:___________ 天气:______
实验名称:二氧化碳的实验室制取与性质
实验目的:1.练习实验室里制取二氧化碳和用向上排空气法收集气体。
2.加深对二氧化碳性质的认识。
3.培养学生的逻辑思维能力和实验操作能力以及团队精神。
实验用品:烧杯、集气瓶、玻璃导管、胶皮管、单孔橡胶塞、铁架台(带铁圈)、试管、试管夹、玻璃片、酒精灯。
大理石、稀盐酸、澄清石灰水、紫色石蕊溶液、蜡烛、木条、水、火柴。
实验重点:实验室制取二氧化碳以及收集。
实验难点:二氧化碳与紫色石蕊溶液反应的现象分析。
课型: 实验课
 课时安排:一课时
课时安排:一课时
实验过程:
一:知识回顾:(同组讨论,指定一人回答)
1.实验室制取二氧化碳的药品,原理,反应装置和收集装置。
2.检查装置气密性的方法是什么?
3.用向上排空气法收集二氧化碳时,怎样检验二氧化碳已收集满?
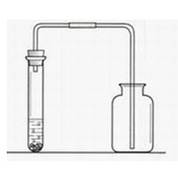
制取二氧化碳装置图
二:实验步骤:(教师指导,学生实验)
<一>制取二氧化碳:
1.如图所示连接仪器,并检查装置的气密性。
2.在试管中放入2药匙大理石,然后小心的注入稀盐酸,不能超过试管容积的1/2,立即用带有导管的橡胶塞塞住试管口,观察试管里发生的现象以及产生气体的颜色(现象:________,气体颜色为__________)。过一会儿,用向上排空
气法收集二氧化碳,并检验集气瓶中是否收集满二氧化碳。用玻璃片盖住已收集

满二氧化碳的集气瓶,备用。 验满装置图
<二>验证二氧化碳的性质:
1.向盛有少量澄清石灰水的试管中通入二氧化碳,观察现象。(现象为:_________________).
2.向盛有少量紫色石蕊溶液中通入二氧化碳,观察现象.(现象为:______________).然后给该试管中的液体加热,观察现象.(现象为:_______________________).
3.把一支短蜡烛固定在烧杯内,点燃.拿起收集满二氧化碳的集气瓶中,向烧杯中缓慢倒入二氧化碳,观察现象.(现象为:______________________________,说明二氧化碳_______(“能”或”不能”)燃烧,也______支持燃烧,密度比空气密度_______).
三:问题与讨论:(学生讨论,教师分析总结)
1.在收集二氧化碳时,当有气体产生时,为什么要过一段时间再收集?
2.在检验二氧化碳是否收集满时,为什么要把燃着的木条放在集气瓶口,而不伸入到集气瓶中?
3.长期盛放澄清石灰水的容器内壁会产生一层白膜,请问是澄清石灰水与空气中的什么发生了化学反应,应该怎样除去?
4.总结实验室检验二氧化碳的方法。
5.向紫色石蕊溶液中通入二氧化碳后,溶液颜色为什么会由紫色变为红色?当加热变成红色的溶液后,溶液为什么又会变回紫色?
四.实验小结。
五.作业:回顾本实验并完善实验报告。
六.实验完毕,整理实验桌。
第二篇:甲烷的制法与性质实验报告
甲烷的制法与性质
李俊
(2009级1班第8实验小组,电话:137xxxxxxxx)
一、实验目的:
掌握甲烷的实验室制法;了解甲烷的性质;练习不同的实验教学方法。
二、实验原理:
CH3COONa+NaOH
CH4+2O2 点燃 △ CaO Na2CO3+CH4↑(其中CaO能稀释NaOH,防止NaOH腐蚀玻璃) 2H2O+CO2
三、主要材料与试剂:
铁架台、酒精灯、托盘天平、研钵、水槽、药匙、玻璃棒、火柴、集气瓶、毛玻璃片、大试管、小试管、导气管、无水醋酸钠、NaOH、Fe2O3、KMnO4、溴水、澄清石灰水
四、实验内容
1.试剂的预处理
由于氧化钙,无水醋酸钠,三氧化二铁,氢氧化钠大都为块状颗粒为使反应物充分接触,使用前必须先在研钵中分别研细。由于氢氧化钠极易潮解,所以应最后研,待药品都研细后在研钵中用玻璃棒搅拌混合均匀,通过纸槽装入大试管。
2.甲烷制取的改进
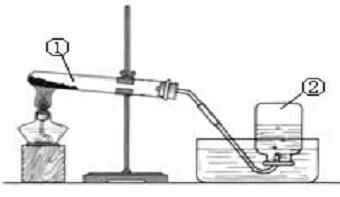
如图组装实验装置
(a)检验装置气密性:把导管的下端侵入水槽中,用双手紧握试管底部,如果观察到导气管口有气泡逸出,证明装置气密性良好。
(b)收集过程
①称取4.5g醋酸钠和1.2g碱石灰及氢氧化钠1.2g,研细混合均匀后装入预先卷成筒状的纸内,再装入试管,可避免加热时试管的破裂。将仪器如制O2装置一样装好。先均匀预热,再集中火力由管前向管尾加热。用试管收集气体应先验纯(CH4的爆炸极限的体积比为5%~15%)后收集或点燃。
第 1 页,共 3页
②或者取2药匙(约3g)无水醋酸钠,1药匙(约2g)NaOH,1药匙(约2g)Fe2O3,分别研细混匀。将药品装入干燥试管,管口略向下倾斜,塞上带导管橡皮塞并固定于铁架台上。预热1min后,再对试管底部加热,约1~2min,即有大量CH4生成。点燃,火焰高度达4~5cm,5min可收集500mL CH4。该反应不需烘干药品,产气快,气流稳,气量多,火焰大,节省时间,操作简便。
(c)验纯:
用排水法收集一试管甲烷气体,用大拇指按住试管口,将试管口向下略倾斜靠近酒精灯火焰,如果甲烷安静的燃烧或发出“噗”的一声,则说明甲烷纯净,可以进行下面的性质实验。
4.甲烷的性质
(1)甲烷与酸性高锰酸钾溶液反应。取一支试管,加入约3mL酸性高锰酸钾溶液,通入甲烷,观察颜色变化。
(2)甲烷与溴水反应。用排水法收集满一试管甲烷,然后再加入约3mL溴水,塞上塞子振荡,观察颜色变化。
(3)甲烷在空气中的燃烧,甲烷经验纯后点燃,可看到浅蓝色火焰。在甲烷火焰上方倒置一个干燥的小烧杯,可观察到烧杯壁上有水珠生成。换一个用石灰水浸润的烧杯罩在甲烷火焰上方,可观察到石灰水变浑浊,说明有CO2生成。
(5)甲烷与氧气混合爆鸣实验。以H2O2为原料,用排水法收集2/3体积的氧气,再收集1/3体积的甲烷,盖好瓶口,用抹布包住集气瓶,瓶口对住火焰点燃,发生爆鸣;
五、注意事项
1.此实验成功与否的关键取决于药品是否无水。即使是新购回的无水醋酸钠,亦应事先干燥后再使用。
2.此实验制取甲烷时试管容易爆炸,在加热时应注意。同时也应先加热药品前面,防止生成的气体将前面的药品带出去。
六、思考与讨论
1.醋酸钠和氢氧化钠反应制取甲烷的反应一般认为是自由基反应,它由以下过程组成。 链引发:CH3COONa→·CH3+·COONa
甲烷生成:·CH3+NaOH→CH4+·ONa
碳酸钠生成:·ONa+CH3COONa→·CH3+Na2CO3
链终止:·ONa+·COONa→Na2CO3
当反应的温度过高时:
·CH3+CH3COONa→CH3COOCH3+·ONa
链终止时产生CO:2·COONa→CO+Na2CO3
2.甲烷点燃后火焰呈黄色的原因有:燃烧不充分﹔甲烷气不纯。如制气加热过猛或NaOH用量不足,还会发生两分子醋酸钠生成丙酮:2CH3COONa→CH3COCH3+Na2CO3 当丙酮混入甲烷,火焰就夹带有黄色。
第 2 页,共 3页
评价:通过此次实验,巩固了初中制取甲烷的实验,对于甲烷的制取和性质有了更深入的了解,对于实验过程中细节部分也尽量达到了精准化。
七、相关文献与重点文献综述
1.本实验按照课本介绍的方法, 用无水NaAc 与市售碱石灰加热制取甲烷, 温度要求高且反应速度很缓慢, 产气量少, 不仅集气时间长, 而且可燃性实验往往无法进行。其主要原因是在市售的碱石灰试剂中,NaOH 的含量只占1/ 7, 含有水分相当多, 不适用于制甲烷, 通过实践, 我们使用新的自配制试剂后加热只需要一般酒精灯, 而且反应速度快, 产气量足。
2.甲烷制取是中学、大学基础化学实验的一项重要内容对其制备方法,尤其是金属氧化物
的催化作用, 已有大量的研究报导看法也不一致。按现在教科书方法进行甲烷制取实验, 效果不佳, 产气量不足杂质气体量多, 反应速度慢, 点燃实验焰色未能达到理想要求。本文针对上述问题进行了大系统性的对照实验, 在多次的反复验证中, 提出了甲烷的最佳制取案, 并讨论其反应机理。
3.甲烷的制取实验是中学有机化学的一个重要实验, 也是不容易做成功的一个实验。利用
新出炉的煤渣代替“石灰”,作吸水剂制取甲烷, 实验效果好。
八、参考文献
[1]袁国新.甲烷制取和性质实验的改进[M].江苏省启东中学,2000,(09).
[2]郭南芳,游利坚,周文富.影响甲烷制取的因素研究[J].中学化学参考 ,1997,(02).
[3]熊 英.甲烷制取实验的改进[M].武汉市三十中学1996,(03).
[4]王文丽,叶俊丽. 甲烷制取实验的几点改进[M].铜川市第3中学1995,(12)
[5]任有良,李晓霞,邓忠朝. 甲烷制备实验中两个问题的探讨[J].商洛师范专科学校学报, 2004,(04) .
[6]李圣菊. 对《甲烷的制备》实验的探究[J].教学仪器与实验(中学版), 2006,(03) .
[7]石启英,任有良. 甲烷制备实验中有关副反应的探讨[J].纺织高校基础科学学报, 2003,(02) .
[8] 任有良,石启英,周春生. 甲烷制备实验中掺入物的选择[J].教学仪器与实验, 2005,(11).
第 3 页,共 3页
