 实验十二 兔膈肌放电观察
实验十二 兔膈肌放电观察
【实验目的】
1. 观察多种因素对动物呼吸运动的影响
2. 了解反映呼吸运动动物模型
3. 熟悉BL–410生物机能实验系统的操作
【实验原理】
平静呼吸运动是由包括膈肌和肋间外肌在内的呼吸肌收缩和舒张活动,引起胸廓的扩大和缩小的运动,为自动节律性活动。当延髓吸气中枢兴奋时传出冲动达到脊髓时,引起支配吸气的运动神经元兴奋,发出神经冲动经膈神经和肋间神经传到膈肌和肋间外肌,引起膈肌和肋间外肌收缩,胸廓扩大产生吸气。延髓吸气中枢活动暂停,膈神经和肋间神经放电停止,膈肌和肋间外肌舒张,胸廓缩小产生呼气。这种起源于延髓呼吸中枢的节律性呼吸运动,受到来自中枢和外周的各种感受器,特别是化学感受器和机械感受器传入信息的反射调节。当动脉血中PO2、PCO2或[H+]发生变化时,通过延髓腹外侧浅表的中枢化学感受器和外周化学感受器来影响呼吸运动。当肺过度扩张或过度萎陷时,通过气道平滑肌中的牵张感受器发出冲动经迷走神经到达延髓,反射性抑制或兴奋吸气。家兔的肺牵张反射在其呼吸调节中起着重要作用。膈神经放电活动和膈肌收缩代表吸气运动的开始,而膈神经放电活动停止和膈肌舒张与呼气运动同步。此外,膈神经的放电活动状态的变化,反映了呼吸中枢神经系统机能活动的变化。
【实验对象】
家兔
【实验器材】
哺乳动物手术器械,兔解剖台,20%氨基甲酸乙酯,20ml注射器,约1m长内径0.7cm橡皮管一根,CO2气囊,0.9%氯化钠生理盐水,监听器,引导电极支架,刺激电极及相连的刺激线,BL—410生物机能实验系统。
【实验步骤】
1. 动物手术
(1)称重
(2)麻醉耳缘静脉氨基甲酸乙酯5ml/kg 麻醉药:20%
麻醉指征:肌张力下降、角膜反射消失、呼吸平稳、痛觉明显减退或消失
(3)仰卧固定
(4)气管插管术:颈前正中纵切口倒“T”型切口
(5)分离双侧迷走神经并各穿一细线打松结备用
(6)暴露膈肌并安置记录电极:在上腹部正中找到剑突所在部位,在剑突下3-4cm的地方依次剪去皮肤,沿腹白线在剑突下剪2-3cm切口,打开腹腔,用止血钳夹持剑突尖部并向动物头端翻转剑突,在剑突内表面可见贴附的膈肌,将两根刺激电极平行插入膈肌恢复剑突至原位。
(7)安放引导电极:将引导电极支架置于适当的位置,用玻璃分针轻轻挑起膈神经放在电极上,稍稍提高电极,使之悬空与周围组织脱离接触,但切不可将
神经拉得过紧,防止损伤。接地电极置于皮肤切口,随仪器并联接地。
2.实验观察
(1)BL-410操作:打开电脑,进入BL-410生物机能实验系统,1通道选择肌电,点击开始按钮, 正常呼吸时的膈神经放电:观察动物正常呼吸时胸廓的运动、呼吸运动和膈神经放电曲线的关系,通过监听器监听与吸气运动
相一致的膈神经放电声。
(2)于一侧气管插管上连接长橡皮管,待放电活动稳定后堵住插管的另一侧
开口一分钟,观察解剖无效腔明显增加时,放电的变化。
(3)通过气管插管向气管内缓慢注入CO2,观察吸入气中CO2浓度增加时放电
的变化。
(4)肺牵张反射:肺扩大和肺萎缩,观察放电变化。
(5)先切断一侧迷走神经,再切断另外一侧迷走神经,观察膈神经和膈肌的放电的变化。
(6)重复上述(1)、(2)、(3)步,对比结果的不同。
 【实验结果】
【实验结果】
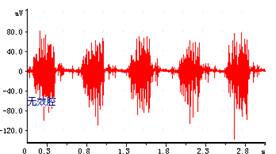
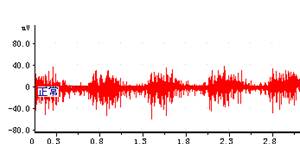
图1.正常呼吸 图2.增大无效腔
(由于操作失误,无法完整截取增大无效腔时膈肌放电的变化情况,实验结果请结合图1观察。—)
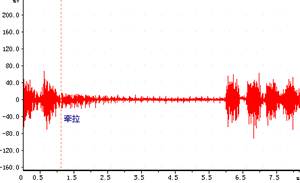
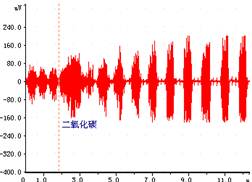
图3.注入二氧化碳 图4.肺扩张
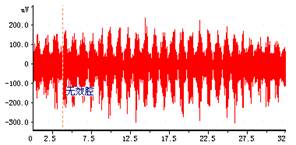
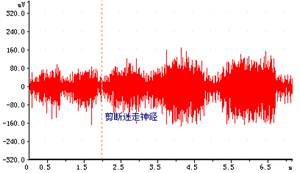
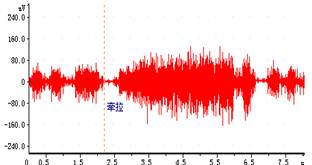 图5.肺萎陷 图6.剪短迷走神经
图5.肺萎陷 图6.剪短迷走神经
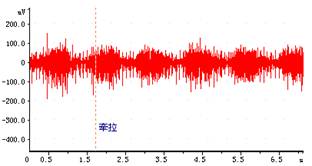

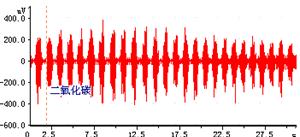 图7.注入二氧化碳(剪短迷走神经) 图8,增大无效腔(剪短迷走神经)
图7.注入二氧化碳(剪短迷走神经) 图8,增大无效腔(剪短迷走神经)
图9.肺扩张(剪短迷走神经) 图10.肺萎陷(剪短迷走神经) 【实验结果讨论】
1. 正常呼吸曲线:在正常麻醉状态下,实验动物保持平稳的呼
吸节律,其中上升支为吸气,下降支为呼气;曲线疏密反映呼吸频率,曲线高度反映呼吸幅度。
麻醉后仍产生节律性呼吸的原因:呼吸中枢延髓的吸气神经元自主放电,冲动经膈神经传到膈肌,使膈肌收缩向下运动,肺内压下降,当低于大气压时,开始吸气.随着吸气,肺泡扩张,位于气管到细支气管平滑肌内的牵张感受器兴奋,冲动经迷走神经传入到延髓,抑制吸气神经元, 吸气神经元停止放电,吸气转为呼气。
2. 增加无效腔→增加气道长度后家兔呼吸张力增加,呼吸频率增加。
增加无效腔从而减少了肺泡的通气量,使肺泡气体更新率下降造成动脉血PO2降低,PCO2升高,刺激中枢和外周化学感受器引起呼吸运动会加深加快:另外,气道加长使呼吸气道阻力增大,减少了肺泡通气量,反射性呼吸加深加快;增加家兔气道长度可使家兔通气量增加,呼吸频率加快。
3. 增大二氧化碳浓度→呼吸运动加深加快
CO2是调节呼吸运动最重要的生理性因素,它不但对呼吸有很强的刺激作用,并且是维持延髓呼吸中枢正常兴奋活动所必须的。每当动脉血中PCO2增高时呼吸加深加快,肺通气量增大,并可在一分钟左右达到高峰。由于吸入气中CO2浓度增加,血液中PCO2增加,CO2透过血脑屏障使脑脊液中CO2浓度增多,
(CO2十H2O→ H2CO3 → HCO3-+H+ )CO2通过它产生的H+刺激延髓化学感受器,间接作用于呼吸中枢,通过呼吸机的作用使呼吸运动加强,此外,当PCO2增高时,还刺激主动脉体和颈动脉体的外周化学感受器,反射性地使呼吸加深加快。
4. 肺牵张反射 肺扩张→抑制吸气活动的反射 肺萎陷→引起吸气活动的加强
肺牵张反射的感受器主要分布在支气管和细支气管的平滑肌层中,称为肺牵张感受器。吸气时,当肺扩张到一定程度时,肺牵张感受器兴奋,发放冲动增加,经走行在迷走神经中的传入纤维到达延髓,使吸气切断机制兴奋,抑制吸气,从而抑制吸气肌的收缩而发生呼气。呼气时,肺缩小,对牵张感受器的刺激减弱,传入冲动减少,解除了抑制吸气中枢的活动,吸气中枢再次兴奋,通过吸气肌的收缩又产生吸气。这个反射起着负反馈作用,使吸气不致于过长,它和脑桥的调整中枢共同调节呼吸的频率和深度。切断迷走神经后上述反应消失,说明这是由迷走神经参与的反射性反应。
5. 切断双侧迷走神经→呈现很明显的深而慢的呼吸
迷走神经的作用:迷走神经中含有肺牵张反射传入纤维,当吸气运动使肺扩张时,该神经纤维兴奋,冲动传入中枢后引起吸气切断机制,吸气神经元活动抑制,吸气停止转为呼气运动,从而加速吸气→呼气运动的交替。
当切断迷走神经后,中断了肺扩张反射的传入通路,反射作用减弱,从而出现了呼吸程度加深,呼吸速度减慢的现象。(另外,迷走神经是外周化学感受性反射的传入神经,切断两侧迷走神经,呼吸中枢将不能感受外周的化学性刺激,失去外周的化学感受器反射调节作用)
【实验结论】
增大无效腔、增加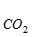 浓度、呼吸加深加快;切断迷走神经呼吸加深变慢; 【思考题】
浓度、呼吸加深加快;切断迷走神经呼吸加深变慢; 【思考题】
1. 实验中动物吸入高浓度的二氧化碳后,可能引起呼吸产生怎样的改变,它产生的机制是什么?可能兴奋的化学感受器是哪一个?
动物吸入高浓度的二氧化碳后呼吸运动加深加快,产生机制:呼吸频率加快是由于吸入空气中的PCO2增加,使得血液中PCO2增加,CO2通过血脑屏障进入脑脊液中溶于水,在碳酸酐酶的作用下分解成HCO3- + H+,H+刺激延髓化学感受器,间接作用于呼吸中枢,通过呼吸肌的作用使呼吸加强。PCO2增加,还刺激主动脉体和颈动脉体的外周化学感受器,反射性地使呼吸加深加快。
2.切断迷走神经以后牵张反射消失的原因是什么?
迷走神经的作用:迷走神经中含有肺牵张反射传入纤维,当吸气运动使肺扩张时,该神经纤维兴奋,冲动传入中枢后引起吸气切断机制,吸气神经元活动抑制,吸气停止转为呼气运动,从而加速吸气→呼气运动的交替。当切断迷走神经后,中断了肺扩张反射的传入通路,反射作用减弱,从而出现了呼吸程度加深,呼吸速度减慢的现象。
第二篇:实验针灸学实验
第二章 实验针灸学实验
实验一 动物实验基本操作实验方案
【实验目的】
掌握动物实验的基本操作技术和方法。
【实验对象】
2.0~2.5kg健康家兔。
【实验材料】
兔台、动物秤,手术刀、手术剪、止血钳、注射器、镊子、玻璃分针。
【实验步骤】
1. 称重:用动物秤称重,以千克(kg)计算。
2. 麻醉:以20%氨基甲酸乙酯按5ml/kg的标准,于耳缘静脉注射,实行全身麻醉。应注意:
(1)在实验中,常选用耳外缘皮下静脉进行注射,拔去耳背外缘部分的毛,用手指轻弹血管,使静脉扩张。
(2)术者用一手的食指和中指夹住静脉近心端耳部,使静脉充盈,另一人用拇指和无名指固定兔耳的远端,并把住头部,避免家兔躁动。
(3)术者手持注射器,尽量在血管的远侧端,与血管的角度呈15度左右,将针头刺入静脉。然后用一手的拇指和食指、中指将针头夹持固定在耳上,另一手缓缓推动注射器筒芯,将药物注入静脉。
(4)如果注射阻力较大或出现局部肿胀,说明针头没有刺入静脉,应立即拔出针头,在原注射点的近心端重新刺入。
(5)在进行静脉注射时,首先需将注射器内的空气驱尽,以免将空气注入静脉形成气栓。
(6)此外,注射速度应尽量缓慢而均匀,以免扰乱循环和呼吸系统的功能而致家兔死亡。
3. 手术:
(1)将麻醉后的家兔仰卧固定于手术台上。
(2)于颈部正中,上腹部及大腿内侧剪毛。
(3)在颈部沿正中线切开皮肤5~7cm ,用止血钳于正中线分开肌肉,暴露气管,在气管两侧可见到与气管平行的左右颈总动脉,伴颈总动脉而行有神经束,其中包含迷走神经、交感神经及减压神经。(粗细:迷走神经—交感神经—减压神经)
要点:①分离颈神经时用左手托起颈部,使颈部组织充分暴露。②用止血钳、玻璃分针轻轻剥离组织,然后用四根线分别将颈总动脉、迷走神经、交感神经、减压神经作以标记。
(4)于剑突下3~4cm纵行切口,剥离空肠。
(5)于下肢股内侧纵行切口,剥离股动脉,坐骨神经。
(6)观察子宫(雌兔)。
4. 处死:于耳缘静脉注射空气,造成气体栓塞致死。
【思考题】
1. 在麻醉动物时应注意哪些问题?
2. 家兔耳缘静脉注射时应注意哪些问题?
实验二 针刺(灸)“素髎”穴对失血性休克家兔血压的调整作用
【实验目的】
本实验旨在通过观察针刺(灸)“素髎”穴对失血性休克家兔血压的调整作用,进而理解“素髎”穴用于急救的部分机理,并掌握动物血压测量的实验方法。
【实验对象】
2.0~2.5kg健康家兔1只,雌雄不拘。
【实验材料】
Digitallab生物医学信号采集处理系统、血压换能器、动脉插管、静脉套管、动脉夹、常用手术器械1套、20ml和5ml注射器、5号注射针头、艾条、兔台、量筒(100ml)、烧杯(500ml)、三通管、生理盐水、20%氨基甲酸乙酯、5%枸椽酸钠、纱布、棉球、缝线。
【实验步骤】
1. 调整生理记录仪及血压换能器至正常工作状态。动脉插管通过一段胶管(不宜过长)与血压换能器相联,换能器另一开口与三通管联结牢固。经三通管向血压换能器压力仓及胶管和动脉插管中注人5%枸椽酸钠,勿使其中有气泡。
2. 取家兔1只称重,用20%氨基甲酸乙酯溶液,按5ml/kg剂量于腹腔注射麻醉。将家兔仰卧固定于兔台上,颈部及腹股沟部剪毛备皮。
3. 分离出一侧颈总动脉,长约2.0~3.0cm,穿入双股缝线,先于远心端结扎,用动脉夹夹住动脉的近心端,用眼科剪在动脉中部剪开一小口,用注射器注入少许5%枸椽酸钠,插入动脉插管,结扎固定。
4. 切开腹股沟处皮肤,切口2.0~3.0cm,分开肌肉,在股静脉下方找出较细、颜色淡红的股动脉,分离出股动脉2.0~2.5cm,穿双股结扎线,结扎其远心端,用动脉夹夹住其近心端,在其上用眼科剪剪一小口,注射入少许5%枸椽酸钠,插入动脉插管,结扎固定,以备放血。
5. 为防止实验过程中凝血,在耳缘静脉注入5%枸椽酸钠适量(1ml/kg)。约3分钟后,打开颈部动脉夹,记录一段正常血压为对照值。兔正常血压通常在13.3kPa(100mmHg)左右。
6. 待血压稳定后,迅速于股动脉处放血,使血压下降至6.6kPa(50mmHg)左右,立即停止放血,并量出其放血量,放血量约为体重的2%左右。
7. 待血压稳定在某一较低水平后,针刺(灸)“素髎”穴,观察并记录血压的变化。
8. 停针刺(灸)后观察血压变化情况15~20分钟。
9. 比较针刺(灸)后血压变化程度及持续时间,写出实验报告。
【注意事项】
1. 注射麻醉药时,前1/2量可较快注入,待动物较安静后,后1/2剂量应缓慢注入。同时注意兔的呼吸情况,出现异常情况立即停止注射。
2. 在分离颈总动脉时,小心勿损伤其附近的神经(迷走神经、交感神经及减压神经),勿损伤通向甲状腺的血管。
3. 注意动脉插管与颈动脉的位置,勿使其扭转而影响血压测量。
4. 气候较冷时,要有手术灯照射动物以保温。
【实验结果】
记录家兔颈动脉血压值(mmHg)

【思考题】
1. 若欲验证针刺(灸)对失血性休克家兔血压的调整作用需注意哪些实验环节?
2. 请设计一个验证穴位功能相对特异性和补泻手法效应差异性的针灸升压抗休克实验。
实验三 针刺对家兔心肌缺血性心电图的影响
【实验目的】
熟悉动物心电图描记方法,学会一种心肌缺血动物模型的复制,验证针刺“内关”穴对家兔心肌缺血的治疗作用。
【实验对象】
2.0~2.5kg健康家兔2只,雌雄不拘。
【实验材料】
Digitallab生物医学信号采集处理系统、20%氨基甲酸乙酯,毫针,G—6805电针,兔台,手术器械一套。
【实验方法】
1. 两只家兔一只作实验兔,一只对照,分别称重。
2. 将两只家兔以20%氨基甲酸已酯5ml/kg于腹腔麻醉后仰卧固定于兔台上。
3. 于家兔胸骨处剪毛。
4. 将黑色检测电极联于右下肢、白色检测电极联于左上肢、红色检测电极联于胸骨柄左侧1cm处。
5. 将检测电极与微机连接,记录心电图(程序:开机→输入信号→选择通道3→心电图→描记心电图,增益选择、显速、参数设置视实验情况而定)。
6. 将实验家兔电针“内关”处理20分钟,于耳缘静脉注射垂体后叶素(2.5u/kg),于注射后1’、3’、5’、10’各记录数据一次,对照兔除不做针刺外,其他处理与实验兔相同。
7. 比较二者心电图变化之异同。
【思考题】
1. 垂体后叶素导致心肌缺血的特点是什么?
2. 为什么“内关”穴可治疗心肌缺血?
实验四 针刺对实验性肺水肿家兔呼吸状态的影响
【实验目的】
本实验在于了解哮喘动物模型制作方法及针刺对其呼吸状态的影响。
【实验对象】
2.0~2.5kg健康家兔1只,雌雄不拘。
【实验材料】
Digitallab生物医学信号采集处理系统、兔台、手术器械1套、气管套管、5ml和1ml注射器、20%氨基甲酸乙酯、50%葡萄糖注射液、生理盐水、15mm毫针、缝线、棉球、纱布。
【实验步骤】
1. 家兔称重后,按5ml/kg由耳缘静脉注入20%氨基甲酸乙酯麻醉家兔。
2. 将家兔仰卧位固定于兔台上,并在颈部、剑突下剪毛备用。
3. 作气管切开后插入气管插管;剑突下切皮,连接膈肌放电测量装置(注意:连结膈肌的针灸针互相不能接触)。
4. 由呼吸和膈肌放电测量装置记录家兔呼吸运动正常值。
5. 由气管沿管壁缓慢注入50%葡萄糖注射液0.5ml/kg,分别记录注入葡萄糖后即刻,5分钟,10分钟时呼吸波形,观察其呼吸频率、幅度的变化;膈肌放电情况变化。
6. 针刺家兔的足三里穴,加电针5分钟后出针。分别记录行针时,取针后5分钟,10分钟的呼吸波形。
7. 再次按半量注入50%葡萄糖注射液,记录数据变化。针刺家兔的合谷穴,持续运针5分钟后出针。分别记录行针时,取针后5分钟,10分钟的呼吸波形。
8. 对比二穴对哮喘模型的治疗效果。
【注意事项】
实验过程中呼吸波形如接近正常状态时,可向气管内补注50%葡萄糖注射液0.5ml。
实验五 针刺不同穴位对小白鼠耐缺氧时间的影响
【实验目的】
针刺对能量代谢有明显影响。本实验在于观察针刺对健康小白鼠耐缺氧时间的影响以及不同穴位是否存在功能相对特异性。
【实验对象】
20克左右小白鼠9只,雌雄不拘。
【实验材料】
50ml广口瓶9只、15mm毫针6支、秒表9只、钠石灰、胶布若干。
【实验步骤】
1. 小白鼠禁食12h。
2. 在广口瓶内分别装入钠石灰2g,盖上盖子备用。
3. 9只小白鼠随机分为A、B、C三组,做好标记。
4. 实验时,分别将每只小白鼠用胶布固定在木制实验板上,A组小白鼠针刺双侧足三里穴,B组小白鼠针刺双侧环跳穴,手法以捻转为主,平补平泻,行针5分钟后拔针。C组为对照组,除不给予针刺外,余同针刺组。
5. 将上述处理后的每只小白鼠分别装入盛有钠石灰的广口瓶内,迅速盖紧盖子,立即用秒表开始计时。
6. 随时观察瓶内小白鼠情况,发现小白鼠呼吸停止,立即按下秒表,记录死亡时间。
7. 从小白鼠开始装入瓶内至呼吸停止为小白鼠耐缺氧时间,比较各组小白鼠耐缺氧时间有无差异。或将全班同学的实验结果按上述实验分组后分别整理,以对小白鼠耐缺氧时间进行统计学的显著性检验。
【注意事项】
1. 小白鼠装入瓶内后,瓶盖要塞紧,必要时用蜡烛熔化封住瓶塞四周,防止漏气。
2. 钠石灰要新鲜干燥。
3. 每只小白鼠体重尽量相近,差异保持在±1g范围内。
【思考题】
针刺对小白鼠耐缺氧时间影响的可能机制是什么?
实验六 针刺对家兔奥狄括约肌肌电的影响
【实验目的】
胆石症是常见急腹症之一,发病率较高。针刺“日月”、“期门”穴有明显的治疗作用,能促进胆汁分泌,调节胆囊、胆管运动和奥狄括约肌活动。本实验以奥狄括约肌肌电活动为指标,观察针刺对其调整作用。
1. 掌握奥狄括约肌肌电的记录方法。
2. 观察针刺“日月”、“期门”穴对家兔奥狄括约肌肌电的调整作用并进行比较。
【实验对象】
2.0~2.5kg健康家兔1只,雌雄不拘。
【实验材料】
Digitallab生物医学信号采集处理系统、兔台、30号1寸毫针、手术器械1套、20%氨基甲酸乙酯溶液、浓盐酸、液体石蜡。
【实验步骤】
1. 家兔禁食18~20小时。
2. 兔称重,麻醉(20%氨基甲酸乙酯溶液5ml/kg)后,仰卧位固定于兔台上,颈部、上腹部剪毛备用。
3. 做气管插管手术,接人工呼吸机。
4. 在剑突下正中做8cm切口,暴露奥狄括约肌。用直径200μm铜漆包线2根,两端分别用细砂纸刮去漆膜约lcm长,端面用剪刀剪成斜面,横向穿过奥狄括约肌表面的浆膜层,反转后套人预先套在铜线上的塑料管内,向下推动塑料管接触组织,弯曲铜线以防止脱落。周围用消毒干棉球封盖,并滴加适量的37℃~38℃石蜡油。术后30~40分钟开始实验。肌电信号输人生物信号处理系统记录,定标电压1Omm/1mV,纸速1mm/s,时标为10秒。
5. 标记正常奥狄括约肌肌电活动。
6. 针刺“日月”、“期门”穴(手法运针,平补平泻,每秒捻转1次)5分钟,观察肌电活动变化。
【注意事项】
1. 导电极铜丝一定要处理好,两电极越近越好。地线置于切口皮下。
2. 注意防止动物挣扎导致电极脱落,一旦电极脱落,要重新安放电极,重新实验。
3. 如果奥狄括约肌损伤可影响实验结果。
【思考题】
1. 正常家兔奥狄括约肌肌电有何特点?
2. 针刺“日月”、“期门”穴后家兔奥狄括约肌肌电发生哪些改变,为什么?
实验七 针刺对家兔小肠蠕动的调整作用
【实验目的】
观察针刺“足三里”对家兔小肠蠕动的调整作用。
【实验对象】
2.0~2.5kg健康成年家兔1只,雌雄不拘。
【实验材料】
Digitallab生物医学信号采集处理系统、张力换能器、25mm毫针4支、万能支架、竹夹、双凹夹、兔台、手术器械1套、喇叭型玻璃管、20%氨基甲酸乙酯。
【实验步骤】
1. 取家兔1只,称重,耳缘静脉注射20%氨基甲酸乙酯(5ml/kg),仰卧固定于兔台。
2. 于剑突下2cm处向下切开皮肤肌肉3~4cm,暴露腹腔即可见小肠。选取蠕动状态好的一段小肠按下法固定。
(1)在此段小肠的两端(相距2cm左右)穿线,在两端中间,用小号手术带线缝合针穿过空肠浆膜及肠壁,留线一段。
(2)取喇叭管先把小肠一端丝线穿管缘孔结扎,再把小肠另一端丝线穿管缘孔结扎。同时将穿起空肠肠壁的留线悬于管中央,上接张力换能器。
(3)将喇叭管用木夹固定于万能支架上,调整好位置,使线垂直并避免碰在喇叭管壁上,保持一定紧张度。
(4)用纱布覆盖局部,同时用侧灯照射以保持体温。
3. 打开记录仪,记录正常肠蠕动曲线。待记录曲线较稳定后,进行下步实验。
4. 针刺双侧“足三里”穴,直刺1.5~2.5 mm。加电针,强度以下肢微动为度,留针10分钟后,记录肠蠕动曲线。
5. 停针10分钟。
6. 针刺双侧“合谷”穴,直刺2.5~3.0mm,强度以上肢微动为度,留针10分钟,记录肠蠕动曲线。
【实验结果】
【思考题】
影响针灸对小肠蠕动调整作用的因素是什么?还有哪些穴位可调节,如何设计实验?
实验八 艾灸“至阴”穴对兔子宫收缩的影响
【实验目的】
艾灸“至阴”穴可矫正胎位,这在历代针灸文献中均有记载。本实验旨在观察艾灸“至阴”穴对家兔子宫活动的影响。
【实验对象】
2.0~2.5kg健康成年雌性家兔1只。
【实验器材】
Digitallab生物医学信号采集处理系统、手术器械1套(刀、剪、止血钳大小各2、缝合针(圆针、皮针个1)、缝扎线、纱布线)、兔台、艾条、火柴、侧灯、20%氨基甲酸乙酯、10毫升注射器、生理盐水。
【实验方法及步骤】
1. 将雌兔以20%氨基甲酸乙酯按5ml/kg于耳缘静脉注射、麻醉,并仰卧位固定于兔台上,于下腹部备皮。
2. 从耻骨联合上沿正中向上做下腹正中切口长约3~5cm,逐层切开打开腹腔(有出血点时应及时止血结扎之),在膀胱后上可见羊角状子宫(双角子宫),找到一侧子宫角,分离周围组织使之游离,在子宫角的阴道端和卵巢端穿线,并在此段子宫体中央穿一缝扎线,将此线与张力传感器相连。为防止开腹后温度和水分丧失,可用温盐水纱布覆盖切口周围,并用侧灯适当照射以保温。
3. 调试三道生理记录仪及传感装置,记录正常状态下的子宫收缩活动曲线。
4. 艾灸“至阴”穴(用清艾条点燃后,正对穴位,距皮肤1.5~2.0cm,双侧同时施灸20~30分钟,观察记录其子宫收缩活动有无变化。
【思考题】
对各种不同处理引起子宫收缩变化及其差异的原因、临床实用价值进行探讨分析。
实验九 针刺得气时的穴位肌电变化
【实验目的】
学会一种肌电引导记录方法,并通过观察针刺得气时的穴位肌电变化与施针者的手下感觉的关系探讨得气的组织学和生理学定义。
【实验对象】
健康人(同学间互测)。
【实验材料】
示波器或JD-2型肌电图机、电极板、消毒针灸针(针刺涂绝缘漆)、酒精棉球、生理盐水、触压角计、检查床、血压计。
【实验步骤】
1. 受试者安静、仰卧于检查床上,要求体位舒适持久,全身尽量放松。
2. 测量血压,测后将气带暂留上臂备用。
3. 调试记录装置及准备记录。
(1)将仪器组装连接,并进行调试。
(2)开启电源,预热3~5分钟后调节总灵敏度在20μV/cm,放大器时间常数为0.035左右,示波器扫描速度为0.7s/cm;标准电压调至50μV/cm。
4. 用酒精棉球消毒合谷、阳溪、三阴交部皮肤,将垫有生理盐水棉球的电极板置于三阴交穴部固定并与放大输入的接地相连,无关电极接放大输入的正极并与刺入阳溪穴的针灸针体相连,放大输入的负极与准备刺入合谷穴的针灸针体相连。
5. 针合谷,行针催气并细心体会手下感觉强弱,待有手感时(记住强、中、弱程度),将手放开立即记录肌电,并观察其幅度大小(肌电幅度有:强者≥50μV,小者<50μ),有无及其密集程度和持续时间。比较手感强弱与肌电幅度大小及有无是否呈现一致关系。
6. 再次行针,比较手下感最强时和手下感最弱时的肌电差异。并与受试者得气感的强弱进行对照比较(受试者主述针感强弱差异)。
7. 找到针下手感最强、肌电发放最明显的部位后,给止血带充气至超过肱动脉压40mmHg以上阻断血流后,每2分钟再行针1次,观察手感和肌电变化及触压觉变化,直至肌电活动停止。比较触压觉和穴位肌电消失的时间。
【思考题】
1. 针刺得气时术者手下感觉强弱有无与穴位下肌电幅度大小、密集程度和持续时间之间有无一致关系?
2. 得气的组织学和生理学含义是什么?
3. 阻断血流后,从触压角和肌电与针下手感消失时间的先后说明了什么问题?
实验十 针刺抗惊厥作用
【实验目的】
针刺对惊厥具有良好的缓解作用。本实验以小白鼠惊厥程度、次数、持续总时间及死亡时间为指标,观察针刺小白鼠水沟穴对胰岛素过量而致惊厥的缓解效应及针刺的急救效果。
【实验对象】
20~22克同性别的健康小白鼠9只。
【实验材料】
天平、秒表6只、1ml和2ml注射器、5号针头2个、50ml烧杯2个、25mm毫针4支、40u/ml胰岛素注射液、生理盐水(pH调至2.5~3.5)、胶布若干。
【实验步骤】
1. 小白鼠禁食14~16h(不禁水)。
2. 取40u/ml胰岛素注射液1ml,用pH2.5~3.5的酸性生理盐水配制成4u/ml胰岛素注射液10ml备用。
3. 取小白鼠9只,称重,编号,随机分成针刺组2组与对照组一组,每组3只。
4. 按1u/10g比例给小白鼠腹腔注射胰岛素,注射时要掌握好进针的位置、角度、深度,注意避开肝、脾、膀胱。回抽无血及液体时再注射,注射后轻揉小鼠腹部促进吸收。继而观察小白鼠活动情况。
5. 当小白鼠发生惊厥时,迅速取出该小鼠,予以针刺“水沟”、“足三里”穴,平补平泻(以捻转手法为主,手法轻柔)。行针3分钟后出针,观察并记录小鼠惊厥程度、次数、惊厥持续总时间及死亡时间。
6. 惊厥程度评价标准
(1)强阳性:角弓反张,四肢伸直和抽搐反应强烈者,或身体呈直线性滚动者,以(++)表示。
(2)弱阳性:轻微的角弓反张,或伴有四肢伸直,或伴有四肢抽搐者,以(+)表示。
(3)阴性:无角弓反张,仅表现为四肢伸直,或四肢微微抽动者,以(-)表示。
7. 对照组除不针刺外,其他同针刺组。
【注意事项】
实验过程中避免各种因素对小白鼠的刺激,以尽量减少实验误差。
【思考题】
针刺抗惊厥作用的可能机制是什么?
实验十一 针刺退热作用
【实验目的】
电针家兔大椎穴以观察针刺对实验性发热的退热效应。
【实验对象】
健康成年家兔2只,性别、体重均相同。
【实验材料】
肛温计2支、兔台2个、脱脂牛乳若干,5ml注射器2支、注射用针头2个、G-6805治疗仪2台、25mm毫针4支、凡士林适量、胶布若干。
【实验步骤】
1. 称重。
2. 兔耳缘静脉麻醉。
3. 将家兔仰卧固定于兔台上。
4. 反复测肛温3次(记录均值),每次间隔2分钟,描记温度曲线。
5. 于耳缘静脉注射脱脂牛乳1.3ml/kg。
6. 15分钟后反复测肛温3次,每次间隔2分钟,描记温度曲线。
7. 30分钟后电针刺激1只家兔“大椎”穴、“合谷”穴5分钟。
8. 再测肛温3次,每次间隔2分钟,描记温度曲线。
9. 将针刺组与非针刺组肛温曲线进行比较。
实验十二 针刺镇痛实验
【实验目的】
学会一种痛阈测定方法,练习痛阈测定仪的使用,验证针刺镇痛作用。
【实验对象】
健康人群(同学间互测)。
【实验材料】
痛阈测定仪、生理多用仪(或G-6805治疗机)、针灸针、饱和KCl溶液、生理盐水、棉球、检查床等。
【实验步骤】
1. 受试者安静平卧,将痛阈测定仪调试到5mA量程测试档,并将其阳极(K+刺激点)固定于耳垂部,参考电极握于受试者左手,并瞩其感到痛时关闭手控开关。
2. 先将痛阈测定仪开到小阶梯档,然后打开刺激开关,于是测定仪的电流强度开始逐步升级,至受试者觉痛,关闭手控开关时,指针即停于此位置,这时指针指示的电流强度即是引起疼痛的电流强度阈值,也即基础痛阈。记录数值后,关闭刺激开关,于是电流指示回到零位。又可进行下次测定。如是测3次,取其均值为基础痛阈。(注意:受试者必须在刚感觉刺痛时关闭手控开关,而且每次关闭手控开关时的痛感觉程度尽可能相同;受试者打开手控开关后才能进行下次测定,但操纵机器的人不可让受试者知道打开刺激开关的时机,以防条件反射干扰)
3. 针合谷(双侧)得气后行针,留针30分钟,加G-6805电针仪刺激。
4. 于针刺开始后20分钟,30分钟各测3次痛阈(间隔2分钟),取均值,与针前进行比较。
【思考题】
对全班或全组15个受试者在针刺前后之痛阈变化进行统计学处理,比较其差异性,并对本实验结果进行讨论分析,对针刺镇痛效果的作用机理及影响因素进行讨论。
实验十三 针麻下动物阑尾切除术实验
【实验目的】
了解针麻基本方法、步骤和取穴规律,掌握针麻下动物阑尾切除术的实验方法。
【实验对象】
2.0~2.5kg健康成年家兔2只,雌雄一致。
【实验材料】
G6805电针治疗仪、28~30号1寸毫针、碘酒和乙醇棉球、20%氨基甲酸乙酯溶液、阑尾切除手术器具2套(方盘2个、手术刀柄2把、手术刀片2个、止血钳:大弯钳、小直钳、小弯钳各4把、手术镊子:有齿镊子、无齿镊子各2把,持针器4个,缝合针、缝合线、圆针、皮针各4枚)、纱布块、5ml和2ml注射器、胶布、兔台、台秤。
【实验步骤】
1. 家兔2只,分别称重,以20%氨基甲酸乙酯按5ml/kg的1/3量于耳缘静脉注射麻醉。
2. 将2只家兔分别仰卧位固定于手术台上。其中一只家兔用毫针分别针刺双侧“足三里”穴、“唇麻I”穴(位于上门齿之间中线,距牙龈向上3mm左右,针尖向上刺至鼻中隔,深约5~10mm)、“唇麻Ⅱ”穴(下唇下缘中点向下2mm,针尖向下沿中线平刺10~15mm),连接电针仪或针麻仪,开启开关,选连续波,高频,输出强度由0开始,逐渐增加,以动物局部肌肉轻微抖动而无不安挣扎为度。于针麻诱导25~30分钟后,开始按常规剪毛、消毒,行阑尾切除术。另一只家兔不用针麻诱导,亦待25~30分钟后开始按常规剪毛、消毒,行阑尾切除术。
3. 手术中分别观察两只家兔的反应,并作记录,其中动物安静无挣扎者用“一”表示,稍有挣扎者用“+”表示,挣扎较剧者用“++”表示,挣扎激烈以致不能手术者用“+++”表示。
4. 实验中动物挣扎不安,或挣扎激烈不能手术者,提示动物有明显的疼痛感,可用适量20%氨基甲酸乙酯溶液静脉注射进行麻醉,以减轻疼痛(常规麻醉剂量为5ml/kg)。
5. 针麻镇痛效果的评价标准:实验中,针麻动物在手术过程中安静,无明显挣扎,呼吸平稳,手术经过顺利,手术全程未用氨基甲酸乙酯溶液者为针麻效果优;若手术中动物挣扎剧烈,20%氨基甲酸乙酯溶液用量为常规用量的1/3以下即挣扎很快停止,并能顺利完成手术者为良;若20%氨基甲酸乙酯溶液用量大于常规用量的1/3才能完成手术者为针麻失败。
6. 分析比较两只家兔的反应和用药情况,写出实验报告,对针刺麻醉效果进行评价,并对针麻镇痛的原理及本实验的选穴进行讨论。
【注意事项】
1. 实验中,所用家兔应属于同一种系,雌雄应一致,体重、年龄基本相同,以确保实验观察结果的可比性。
2. 家兔的阑尾较长,且有大量的内容物,切除前应仔细辨认后再分离肠系膜,并结扎阑尾动脉,然后进行阑尾切除。
【思考题】
根据观察记录结果分析本实验选穴的依据是什么?
实验十四 循经感传的测定
【实验目的】
掌握循经感传的检测方法,了解循经感传的基本特征。
【实验对象】
健康人(同学间互测)。
【实验材料】
探测电极、无关电极、G6805电针治疗仪,生理盐水,75%酒精棉球。
【实验步骤】
1. 每组5~6人,轮流担任受试者,观察、记录者。
2. 试者安静休息5分钟后接受检测。观察者标定出各经的井穴。
3. 将无关电极置同侧内关穴(测下肢感传时),或同侧三阴交穴(测上肢感传时)。探测电极置于同侧肢体的井穴后,以20次/秒的连续波刺激井穴,同时逐渐增加电流强度至受试者能耐受为度(此感应应强烈,但无疼痛)。
4. 当受试者出现感传感觉时,将其感传情况依下列标准记录:
(1)感传不超过腕、踝关节者以“-”表示;
(2)感传超过腕、踝关节但不超过肩、髋关节者以“+”表示;
(3)感传超过肩、髋关节但不能到达经脉终点者以“++”表示;
(4)感传能贯通经脉全程者以“+++”表示。
5. 循经感传特征的探讨
选择一条感传超过肩、髋关节的经,由受试者主诉感传方向、路线、宽度和感传所到的器官的效应,测定感传速度,观察感传线上有无客观变化,艾灸观察能否加速感传,或以手指用力按压经脉,观察有无阻滞现象。
【注意事项】
1. 循经感传出现率与环境温度有关,因此实验尽可能安排在22℃~30℃的室温条件下进行。
2. 井穴刺激的电流强度应以受试者感觉强烈而无疼痛感为度,太弱与太强均不易激发循经感传。
【讨论】
1. 试述你所观察到的循经感传的基本特征。
2. 如何提高循经感传的显著程度?
实验十五 腧穴低电阻特性探测
【实验目的】
研究认为穴位具有低电阻的特性,本实验用一种探测穴位电阻的方法以观测穴位的电学特性。
【实验对象】
健康人(同学间互测)。
【实验材料】
腧穴电阻测定装置等物品
【实验环境】
1. 实验室室温在23℃上下波动不超过2℃。湿度:23℃上下波动不超过2℃。
2. 实验在屏蔽室内进行,周围无声音干扰。
【实验步骤】
1. 受试者入室后,自然卧位休息10分钟,身体充分放松;
2. 打开实验用仪器,预热10分钟;
3. 选取经典穴位并以穴点为中心直径1㎝作为穴区。
4.用穴位探测仪找寻敏感点,以探穴档测试,受试者手握无关电极,测试者以探测电极端轻放于被测穴区,并选用不同刺激强度,标出受试者最强的敏感点。
5.在敏感点外距离1㎝外取4个点为对照点,作出标志。
6.计算出每位受试者的敏感点与对照点的穴位符合率。
【注意事项】
检测时根据受检经脉,选择不同体位。无论何种体位必须做到充分放松,无疲劳感。
实验十六 健康成人两侧井穴、原穴皮肤电阻对称性观察
【实验目的】
通过探测健康成人两侧同名井穴、原穴的皮肤导电量,以观察其皮肤电阻的对称性,验证经络平衡理论。
【实验对象】
健康人(同学间互测)。
【实验材料】
腧穴电阻测定装置等物品
【实验环境】
1. 实验室室温在23℃上下波动不超过2℃。湿度:23℃上下波动不超过2℃。
2. 实验在屏蔽室内进行,周围无声音干扰。
【实验步骤】
1. 受试者入室后,自然卧位休息10分钟,身体充分放松;
2. 打开实验用仪器,预热10分钟;
3. 用经典方法点出受试者的井穴原穴共48个穴。
4.用穴位探测仪,以探穴档测试,将无关电极固定在受试者前臂内侧。测试者以探测电极端轻放于被测穴区,2秒钟后移开测另一点,每一对同名穴为一组,测定后再测另一组,记录出受试者的敏感点数值。
5.计算出每位受试者的对称情况用相对数Hy表示。。
【注意事项】
检测时根据受检经脉,选择不同体位。无论何种体位必须做到充分放松,无疲劳感。
