实验报告
纳米氧化锌的制备
一、实验目的:
1、了解纳米ZnO的性质及应用。
2、掌握制备纳米ZnO的原理和方法,并比较不同方法的优缺点。
3、掌握检验纳米ZnO光催化性能的一般方法。
4、查阅资料,计算产品的利润。
二、纳米ZnO的性质:
纳米级ZnO同时具有纳米材料和传统ZnO的双重特性。与传统ZnO产品相比,其比表面积大、化学活性高,产品细度、化学纯度和粒子形状可以根据需要进行调整,并且具有光化学效应和较好的遮蔽紫外线性能,其紫外线遮蔽率高达98%。同时,它还具有抗菌抑菌、祛味防酶等一系列独特性能。
纳米ZnO粒子为球形,粒径分布均匀,平均粒径20~30纳米,所有粒子的粒径均在50纳米以下。纳米ZnO粉体的BET比表面积在35m2/g以上。
由于纳米ZnO具有比表面积大和比表面能大等特点,自身易团聚;另一方面,纳米ZnO表面极性较强,在有机介质中不易均匀分散,这就极大地限制了其纳米效应的发挥。因此对纳米ZnO粉体进行分散和表面改性成为纳米材料在基体中应用前必要的处理手段。
三、实验原理:
制备纳米ZnO的方法有很多。按物质的原始状态分为固相法、液相法、气相法3类。固相法包括沉淀法;气相法包括化学气相沉积法、 气相反应合成法、化学气相氧化法、喷雾热分解法; 3液相法包括溶胶—凝胶法、微乳液法、水解加热法、水热法等。
本次试验采用沉淀法制备纳米ZnO。本实验以锌焙砂(主要成分为氧化锌、锌并含有少量铁、铜、铅镍、镉等杂质,杂志均以氧化物形式存在)和硫酸为主要原料,制备七水硫酸锌,以碳酸氢铵为沉淀剂,采用碱式碳酸锌分解法制备活性氧化锌。
四、实验仪器与试剂:
仪器:
分析天平、托盘天平、温度计、蒸发皿、胶头滴管、马弗炉、烧杯、量筒、玻璃棒、恒温水浴锅、布氏漏斗、抽滤机、坩埚、研磨、200目筛子、石棉网、药匙、锥形瓶、洗瓶、滤纸、真空泵、PH试纸。
试剂:
锌焙砂、去离子水、3mol/l硫酸溶液、碳酸氢铵、0.1mol/l高锰酸钾溶液、锌粉、氧化锌、二氧化钛粉、碳酸钙、滑石粉、凡士林、0.05mol/lAgNO3溶液、水合肼。
五、实验步骤:
1、酸解
取10.0g锌焙砂加入到锥形瓶中,加入45ml 3mol/l的硫酸溶液,将锥形瓶放到70℃左右的水浴锅中,并不断搅拌①。反应50min后用布氏漏斗抽滤②,得滤液待用。主要的反应有:
ZnO+H2SO4→ZnSO4+H2O;Fe+H2SO4→FeSO4+H2↑
2、除铁
(1) 在溶液中加入0.1mol/L的KMnO4溶液并不断搅拌至溶液变为粉红色为止③。主要的反应为:
(2) 加入约3gZnO调节PH值在5~6(大约加入了2.1g),煮沸2~3分钟,用布氏漏斗过滤④,保留溶液待用。
主要的反应为:
2KMnO4+10FeSO4+8H2SO4→K2SO4+2MnSO4+5Fe2(SO4)3+8H2O
Fe2(SO4)3+3ZnO+3H20→3ZnSO4+2Fe(OH)3↓
3、除重金属,制ZnSO4·7H2O
向溶液中加入锌粉0.1g,水浴70℃下不断搅拌,10min后用布氏漏斗抽滤,得到过滤溶液⑤。
4、制备ZnO
(1) 在上述滤液中先加入100ml蒸馏水稀释,在温度小于35℃下分批加入9g NH4HCO3,不断搅拌,加压过滤,充分洗涤滤饼(洗涤2~3次)。
(2) 将洗涤后的滤饼在烘箱内240℃烘干10min,制成半成品。
(3) 将干燥后的半成品放于600℃温度下煅烧2h,得到成品即纳米ZnO⑥(图1所示)。
主要的反应为:
3ZnSO4·7H2O+6NH4HCO3→ZnCO3·2Zn(OH)2·H2O↓+3(NH4)2SO4+5CO2+20H2O
 ZnCO3·2Zn(OH)2·H2O→2ZnO+CO2+4H2O
ZnCO3·2Zn(OH)2·H2O→2ZnO+CO2+4H2O
5、ZnO-Ag的制备
取4.0042g ZnO于坩埚中加入19.8ml 0.05mol的AgNO3溶液(按照物质的量比为Zn:Ag=100:2),然后在水浴上蒸干。再在蒸干后的坩埚中加入3.0ml的水合肼还原Ag+⑦,再在水浴上蒸干得到ZnO-Ag。
6、5% ZnO水溶液的制备
用电子天平称取2.0g负载Ag的ZnO溶解在38ml的去离子水中⑧。
7、药膏的制备
用电子天平称取2.0g负载Ag的ZnO放于表面皿上加入一定量的凡士林搅拌均匀,装入小瓶(图2所示)。
8、防晒霜的制备
分别用天平称取ZnO1.0g、二氧化钛粉末1.2g、碳酸钙2.0g、滑石粉10.0g混合于研钵中研细,用200目的筛子筛选,得到粉末状的防晒霜(图3所示)。
六、实验现象:
①处液体变成灰褐色且不断有气泡冒出。
②过滤后滤纸上出现白色ZnSO4·7H2O晶体,加水后溶解。
③目的是将Fe2+转化为Fe3+。
④目的是出去Fe(OH)3 和 Cu(OH)2。
⑤制备氧化锌抽滤过程后得到乳白色滤饼。
⑥焙烧后得到产品为白色粉末,底部产品略发红(坩埚底部的原因),得到5.5174g纳米ZnO。
⑦加入AgNO3溶液后蒸干得到灰色固体,加入水合肼后蒸干得到青绿色固体。
⑧5%ZnO水溶液中ZnO-Ag主要以固体形式存在。
七、实验数据处理:
(1)、锌焙砂中氧化锌的含量未知,实验过程中用氧化锌调节PH,导致无法准确计算产率。
(2)、成本合算:
锌焙砂产品市场价格走势每吨价格:
通过老师对我们的产品分析后估价为25元/kg,那么我们的产品为25000元/吨。如果每吨除去10000元的其他成本费,并且锌焙砂按6500元/吨,那么每吨的剩余价值就是8500元。如果每个月能产100吨,那么利润为85万,这对于一家企业来说才可以运行。
八、实验小结:
(1)用ZnO调节PH而不用氨水,加氨水容易使PH太高而锌离子沉淀。
(2)AgNO3中Ag+的还原:可以采用紫外光来对银离子还原,但是由于需要紫外光照射时间比较长,所以在本实验我们采用水合肼来还原银离子(水合肼比较廉价)。
(3)5%ZnO水溶液除异味液效果分析:
将其喷入鞋中然后放于太阳光下照射对除异味效果更好(由于ZnO-Ag主要以固体形式存在于水中所以不易喷出,对除异味效果有一定的影响,并且这样的产品不已销售。应考虑溶解性)。
(4)防晒粉效果不明显,可能与近期日照不强烈有关。
九、注意事项:
1.煅烧温度要适当。煅烧温度过高,时间过长,易使产品烧结,影响产品的活性;温度太低,时间过短,又不能使其完全分解。
2.锌焙砂在称取使应尽可能选取颗粒小的,否则影响溶解速度。
3.在抽取滤饼时,由于颗粒较小所以在向布氏漏斗中倒时要注意倒速。
4.在煅烧之前的烘干阶段应经可能使样品中的水分烘干,如果不敢可能影响产品质量。
图1:纳米ZnO

图2:药膏

图3:防晒粉

第二篇:CdS纳米粒子的制备实验报告
中南民族大学
实 验 报 告 实验课名称:化学综合实验 指导老师: 学生姓名: 专业:材料化学 班级:一班 学号: 实验名称:CdS纳米粒子的制备和性能研究
实验日期: 组别: 实验成绩:
一.实验目的
1.学会查阅和总结文献。
2.学习Ⅱ-Ⅵ型纳米粒子的制备方法,表征方法。
3.了解Ⅱ-Ⅵ型纳米粒子的应用领域和研究现状。
二.实验原理
1、水热法
水热法是指在特定的密闭反应器(高压釜)中,采用水溶液或有机溶液作为反应体系,通过将反应体系加热至临界温度(或接近临界温度),在反应体系中产生高压环境而进行制备无机合成与材料制备的一种有效方法。在水热法中,溶液起到了两个作用:液态或气态是传递压力的媒介:在高压下,绝大多数反应物均能完全或部分溶解于水,促使反应在液相或气相中进行。
2、液相法
液相法制备纳米粒子由两个过程构成:一是成核过程;另一个是核的长大过程。当成核速率小于生长速率时,有利于生成大的粒子;反之,有利于生成小的粒子。因此,为了控制纳米级粒子的尺寸和形貌,必须调整其成核和生长坏境,保证成核速率大于生长速率。 液相法准备纳米粒子时,在成核生长过程控制因素方面具有自习的特征和规律。影响粒度的因素很多,最主要的因素有反应时间和温度,反应物浓度,表面活性剂种类、浓度配比,还原剂或者沉淀剂浓度及原料加入方式等。
纳米激光粒度仪工作原理
本实验在研究CdS性能时用的是纳米激光粒度仪。其原理是当纳米颗粒分散在液体中时,纳米颗粒在液体分子布朗运动的撞击下进行不规则的运动。当激光束照射到纳米颗粒时将产生脉动散射信号,这些信号强度的变化率与颗粒的运动状态(速度和幅度)有关,也就是与粒径有关,通过光电倍增管将这些脉动的散射光信号接收并转化成电信号,再通过数字相关器中进行处理,识别出有效动态光散信号,再通过特殊软件的反演处理,利用方程计算出纳米颗粒粒径及粒径分布。
三.仪器与药品
药品:
氯化镉CdCl2·2.5H2O 硫脲SC(NH2)2 氢氧化钠NaOH 蒸馏水H2O 无水乙醇C2H5OH
仪器:
紫外-可见分光光度计 (PE 美国) 荧光分光光度计(PE 美国) X-射线粉末衍射仪(Bruker 德国) 透射电子显微镜(FEI 荷兰) 纳米激光粒度仪 高压反应釜(50ml)
pH计 烘箱
电动离心机 玛瑙研钵
DF-101S集热式恒温加热磁力搅拌器
四.实验步骤
1、纳米粒子的制备(本组采用水热法制备)
水热法制备CdS
分别量取15ml0.1mol/L CdCl2·2.5H2O溶液装入两个50ml的聚四氟乙烯内衬的高压釜中。用3 mol/LNaOH调节其pH值至一个为9.06,另一个为12.00。调节pH值的过程中可以观察到有乳白色颗粒沉淀出现,碱度越大颗粒物越多。调节pH值后再加入15ml0.1mol/L SC(NH2)2,立即出现亮黄色乳浊液。待反应液混合均匀后将反应釜放入130℃下恒温反应12h。待反应结束后,得黄色糊状物(pH=9.06)和橙色糊状物(pH=12.00),将反应物用去离子水和无水乙醇各洗涤3次,得到的产物在60℃真空干燥4h,结果得黄色粉末(pH=9.06)和橙色粉末(pH=12.00)。
附:液相法制备CdS的实验步骤
液相法制备CdS
称取1.8g CdCl2,用20ml水溶解,然后慢慢滴加10ml巯基乙酸,开始出现浑浊现象,再向其中慢慢滴加浓NaOH调节pH为4.72,浑浊逐渐消失;然后称取0.9g硫化钠溶于5ml水中,慢慢滴加到上述溶液中,呈有微黄色乳浊液,然后再加入稀盐酸调节pH为4.86,然后于95℃水浴搅拌加热4h,得到黄色浑浊液,然后将产物离心,用水和醇依次洗涤2~3次,转移至试剂瓶中,在60℃下真空干燥12h,得黄色粉末。
2、纳米粒子的表征
用纳米激光粒度仪研究CdS的性能
(1)开机:开机顺序:纳米激光粒度仪——打印机——显示器——电脑(注意顺序不能颠倒)。
(2)启动粒度仪分析系统:在电脑桌面上打开BT-90纳米激光粒度分析系统ver1.0,即进入测试系统。
(3)样品制备:用称量纸取少量的产品倒入小烧杯中,加适量的蒸馏水,在超声波中分散几分钟使其溶解并混合均匀。用比色皿装取稀释后的溶液,放入激光粒度仪中。在测量窗口观察光子数是多少,一般光子数最佳范围是20-40之间。若高于40再稀释溶液,低于20就增加溶质。
(4)填写实验信息:单击“测量—文档”项即可在文档窗口填写样品名称、介质名称、检测单位、测试日期和测试时间等原始信息,这些信息将在测试报告单中打印出来。
(5)测试与结果:单击测试即可进入测试窗口,进行相关测试。单次测试过程大约需要10分钟。点击结束按钮,显示当前的测试结果,将其保存。
(6)重复(3)-(5)的实验步骤对另一个产品进行检验测试。
(7)关机:实验结束后,先退出软件程序,关闭电脑,最后关闭仪器电源。
纳米激光粒度分布仪测试结果
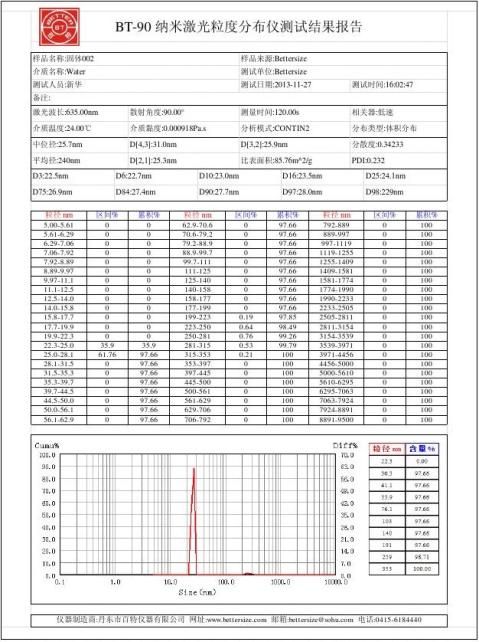
a. pH=9.06
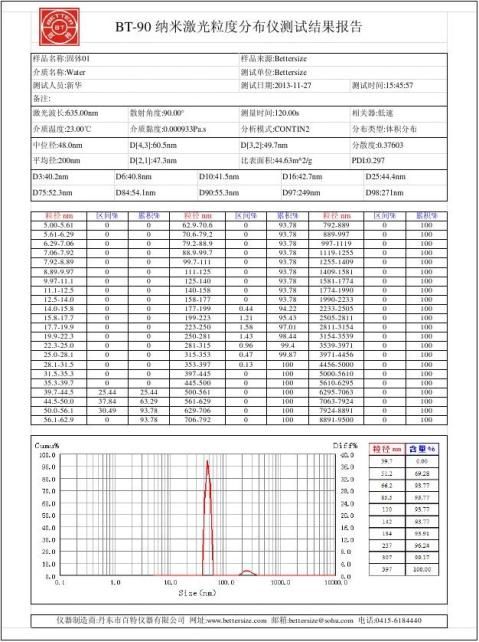
b. pH=12.00
300000
Cd 3p
a
Counts/s
200000
O 1s
Cd 3d 3/2Cd 3d 5/2
表征结果
100000
1000800600400
Binding energy/eV
C 1sS 2sS 2pCd 4sCd 4pCd 4p
2000
6000050000
b
3d 5/2
3d 3/2
Counts/s
40000300002000010000
0400
405410415
Binding energy/eV
80007000
c
S 2p
counts/s
600050004000
155
160
165
170
Binding energy/eV
图1 样品的XPS谱图 (a)全谱 (b)Cd 3d (c)S 2p
50(111)
Counts/10s40

30(220)3
20
10
020(311)304050607080
2?
图2 CdS量子点的XRD谱图
图3 CdS量子点的透射电子显微镜照片
0.8a
Absorbance0.60.4
0.2
0.0300400500
Wave length/nm600700 700
Relative Fluorescence Intensity600500400300200
100
400500
Wave length/nm600b700
图4 CdS量子点的紫外-可见光谱(a)和荧光光谱(b)
五.结果与讨论
1.由图1(a)全谱可见Cd和S是样品中的主要元素,表明产品纯度较高。同种元素可以激发出多组电子峰,最强的光电子线是谱图中强度最大、峰宽最小、对称性最好的谱峰,称为XPS的主谱线。每一种元素都有自己的具有表征作用的光电子线。它是元素定性分析的主要依据。由(b)可得Cd 3d 3/2的电子结合能大于Cd 3d 5/2的电子结合能。比较(b)和(c)得Cd 3d的电子结合能大于S 2p的电子结合能。
2.由图2中三个峰(111)、(220)、(311)都比较尖锐且无杂峰可知CdS的结晶度良好,产物均以六方晶型存在。比较三个峰可知产物的结晶存在择优生长趋势。
3.由图3可见CdS纳米粒子以单分散形式存在,分散性良好,颗粒均匀,呈球形。
4.图4(a)表明样品在400nm处有较强的紫外吸收峰;(b)表明样品在480nm处有较强的荧光吸收峰,荧光强度较大,说明样品的光学性质较好。
CdS的性质极大地受制备方法的影响,本次实验采用水热法制备的两个样品主要差别在于体系的pH值不同,因此粒径的大小,表面吸附的杂质含量等会有差异。
六.思考与讨论
1、影响产物性能的因素有哪些?
答:①反应物的浓度
CdS的制备通常选择一定的硫源和镉源通过适当的方法进行制备,而硫源和镉源之间的相对会影响制备出的CdS颗粒的性质,其主要原因是因为反应体系中晶粒的生成存在成核和生长两个过程。
②反应体系的酸碱性
通过改变反应体系的pH值,也可以改变制备出的CdS颗粒的性质。用液相法制备CdS颗粒时,溶液中存在一定的酸碱平衡。CdS的制备是离子之间的反应,其生成速率主要取决于传质速率和水解平衡的移动方向。不同的pH值会使平衡向不同的方向移动,使颗粒的表面电荷和吸附性质发生改变,从而影响颗粒的大小等性质,也会造成制备出的CdS颗粒的性质不同。
③反应体系的温度
随着温度的升高,CdS的晶型由非晶向立方晶型转变,最后向六方晶型过渡。使用水热法制备时,当加热温度低于160℃时,样品表现为非晶结构;加热温度高于160℃时,样品开始向立方向结构转化。升高加热温度,晶体会向六方晶结构转化,而当温度高于240℃样品完全呈六方晶结构。随着焙烧温度的升高,颗粒的粒径增大,比表面积降低,催化活性降低。
④稳定剂的影响
稳定剂在反应体系中可以抑制晶粒的成长,使制备的颗粒大小均匀,并使颗粒保持在很小的粒径级别。稳定剂有阴离子型、阳离子型、非离子型。稳定剂的用量影响到颗粒的性质。稳定剂的用量增大,制备的颗粒粒径减小,但是稳定剂的用量过多,颗粒表面吸附过多的稳定剂带来更多杂质,降低光催化活性。
2、如何根据实验结果调整实验的条件。
答:在反应物浓度及用量相等的条件下选取适宜的反应温度和pH值。
