合肥市理科实验操作考试化学试题(A)
题目:二氧化碳的制取和性质
 实验目的:
实验目的:
1.掌握实验室制取二氧化碳的方法,掌握用向上排空气法收集气体。
2.加深对二氧化碳性质的认识。
实验步骤:
1.按照装置图连接装置,并检验装置的气密性。
2.向一支试管中加入2—3ml澄清的石灰水,备用;
3.在大试管里放入几小块石灰石,然后加入10—15ml稀盐酸,立即用带有导管的橡皮塞塞住管口,观察试管里发生的现象: 。将导管通入澄清的石灰水里,观察现象: 。反应的化学方程式为: 。
4.用向上排空气法收集气体,过一会儿,用燃着的木条放在集气瓶口,木条火焰 ,说明 。用玻璃片盖住已收集的集气瓶。
5.点燃铁架上的短蜡烛,放入烧杯。拿起盛满二氧化碳的集气瓶,向烧杯里倾倒二氧化碳。观察现象: 。
评分表 二氧化碳的制取和性质

取小烧杯接半烧杯的自来水放在试验台中,将导气管的橡皮塞旋转塞入大试管口。导气管放入烧杯中用双手握住试管的中部和底部观察到有气泡冒出。将导气管从烧杯中取出后将小烧杯放回原处,再将导气管从试管拔出,导气管放回原处,大试管正放在试管架上。将石灰水试剂瓶取出放在试验台中,取下瓶塞倒放在桌面上后再用左手取小试管,用手指拿住接近试管口的位置,右手握住石灰水试剂瓶并使其标签正对手心。双手举高与肩同宽,将瓶口靠紧试管口缓慢倾倒并注意观察试管底部液体的量,当液体量达到试管的四分之一左右时停止。将小试管正放在试管架上,盖上石灰水瓶塞放回原处。取出石灰石的试剂瓶放在试验台中间,取下瓶塞倒放桌面,左手拿住大试管平放,右手用镊子夹取五六块小石子放在试管口,然后慢慢倾斜试管让石子滑落至试管底部。盖上瓶塞放回原处,将大试管放回试管架。取出盐酸试剂瓶将盐酸倒入大试管中(盐酸量约为试管容积三分之一,具体操作与取石灰水相同)。加完盐酸后立即旋紧橡皮塞并将导气管插入石灰水的小试管中,大试管同样放在试管架上,观察现象。当石灰水变浑浊后取出集气瓶,将导气管从小试管中取出并放入集气瓶中,再盖上玻璃片开始收集二氧化碳(调节集气瓶位置使导气管能接触到瓶底,玻璃片粗糙的一面朝下)。等待的时间可以填写部分已完成操作的实验报告,约一分钟时间后取火柴点燃放在集气瓶口(左手将玻璃片稍稍从瓶口抽离一部分,右手将燃着的火柴放在瓶口,可将火柴稍稍深入一点),火焰熄灭(若没熄灭在等一会重复上述操作直至熄灭)。取出导气管盖上玻璃片,大试管中的反应暂时不管。取出放有蜡烛的烧杯,点燃一根火柴后用另一只手将固定有蜡烛的金属架一并取出,在烧杯外点燃蜡烛后放回烧杯中。将积满二氧化碳的集气瓶移至烧杯口(右手握住集气瓶,左手指按住玻璃片),将集气瓶平放,瓶口轻轻搭在烧杯口。边倾斜集气瓶边抽离玻璃片,至整个集气瓶完全瓶口朝下玻璃片完全抽离,观察到蜡烛熄灭(整个操作大概三秒中完成)。将烧杯,集气瓶放回原处填写剩余实验报告。最后清理实验台,将大小试管内物质倒入废液缸中,清洗试管后将其倒插入试管架。提交实验报告,考试结束。
合肥市理科实验操作考试化学试题(B)
题目:燃烧的条件
【实验目的】
1.加深对燃烧条件的认识,进一步了解灭火的原理。
2.体验实验探究的过程。
【实验内容】
1.分别用滴管向棉花上滴酒精和水,放到酒精灯火焰上加热片刻,观察现象。通过此实验可以说明燃烧的条件之一是 。
2.用坩埚钳取一小片纸片(一次性纸杯上剪下来的),放在酒精灯火焰上加热;再取一只空纸杯,放入小半杯水,用坩埚钳夹住杯口一侧,放在酒精灯火焰上加热(加热底部中央,用外焰),观察。通过此实验可以说明燃烧的条件之一是 。
3.利用蜡烛和烧杯,设计一个简单的实验,说明燃烧的条件之一:需要有氧气(或空气)。

先取出酒精灯并点燃。
1. 取出酒精试剂瓶和烧杯,再用镊子夹取一团棉花球,另一只手用滴管吸取酒精滴加4到5滴在棉球上至完全浸湿(此操作在烧杯口完成防治液体滴落在桌面),再将试剂瓶放回原处。将棉球放在外焰上点燃,看到棉球燃烧后将其放入到废液桶中。
2. 将酒精换成蒸馏水同上部操作,棉球没有燃烧。
3. 用坩埚钳纸片一端放在外焰加热,纸片燃烧后放入废液桶。4. 取一空纸杯倒入约半杯的水(操作同液体的倾倒)。
5. 用坩埚钳夹住杯口一侧。
6. 用外焰对准杯底中央加热片刻,纸杯没有燃烧。盖上酒精灯放回原处。
7. 取出蜡烛点燃并固定在桌面或玻璃片上(滴几滴蜡烛油在桌面或玻璃片上后再固定)。
8. 用一只烧杯罩在蜡烛的外焰上方至火焰熄灭。
9. 回答实验报告。
10.清理实验,将纸杯中的水倒入废液桶后放回原处,桌面或玻璃片上的蜡烛油用指甲或镊子去掉,所以仪器药品放回原处摆放整齐实验结束。
合肥市理科实验操作考试化学试题(C)
题目:金属的某些物理性质和化学性质
实验目的
1、巩固和加深对金属性质的认识
2、培养实验设计能力
实验步骤
1、用砂纸打磨铝片和铜片,观察颜色:铝片 ,铜片 。
2、用打磨后的铝片和铜片相互刻画,得出铜片的硬度 (填“大于”或“小于” )铝片。
3、用坩埚钳夹取打磨后的铜片,在酒精灯上加热,观察铜片表面的变化,现象为 。
4、用镊子将打磨后的铝片放入试管中,倒入2—3mL稀盐酸,观察现象,写出发生反应的化学方程式:
5、用胶头滴管取硫酸铜溶液约2mL滴入试管中,再向其中放入打磨过的铁丝,观察现象。该实验说明铁的活泼性比铜 。
评分表:金属的某些物理性质和化学性质

操作要领:
1 .用镊子或手分别夹持铝片和铜片一端,左手拿砂纸前后夹住铝片和铜片,来回搓动砂纸,观察到金属片变亮即可,然后观察得出铝片颜色是银白色,铜片颜色是紫红色。
2. 把铜片放在桌面上,用铝片尖角在它上面刻划并观察;再把铝片放在桌面,用铜片尖角在它上面刻划并观察。铝片上有划痕而铜片上没有划痕,说明铜片硬度大于铝片。
3. 点燃酒精灯,用坩埚钳夹住打磨以后的铜片一端,放在酒精灯火焰上加热,观察到铜片的加热处颜色变为黑色。然后将铜片放在石棉网上
4. 取一支试管,用镊子夹住打磨后的铝片,放在横放的试管口处,然后将试管缓缓竖起,使铝片慢慢滑到试管底部;右手拿住盐酸试剂瓶,使瓶上标签对着手心,左手拿住盛有铝片的试管,试管稍稍倾斜,试剂瓶口紧挨着试管口,将盐酸缓慢地倒入试管中,观察到液体柱约有2cm左右即可,放回盐酸。可以观察到铝片和稀盐酸反应,放出气泡。然后将试管放到试管架上。
5. 另取一支试管,左手拿住试管,右手拿住吸满硫酸铜溶液的胶头滴管,竖直悬空在试管口上,将胶头滴管内的硫酸铜溶液挤入试管内(挤入两胶头滴管的硫酸铜溶液即可)。然后将试管放到试管架上。
6 .用镊子夹住一段铁丝,左手拿砂纸包住铁丝来回抽动,打磨铁丝上的铁锈,观察到铁丝呈现银白色(打磨铁片和第1步相同)。
7. 左手拿盛有硫酸铜溶液的试管并倾斜月四五度角,右手用镊子夹住铁丝,慢慢将铁丝沿试管内壁放入,观察到铁丝上有红色金属生成。
8. 填写实验报告,然后把反应后的金属片分别放回回收容器内,把试管内的废液倒入废液缸,洗涤试管,再将洗净后的试管倒放在试管架上,把桌面试剂瓶和仪器摆放整齐,用抹布擦净桌面。
9. 提交实验报告,考试结束,离开考场。
合肥市理科实验操作考试化学试题(D)
题目:配制质量分数为6%的氯化钠溶液
实验目的:
1.加深对溶质质量分数概念的理解。
2.练习配制一定溶质质量分数的溶液。
实验步骤:
1.计算:配制50g质量分数为6%的氯化钠溶液,所需氯化钠 g,水 g 。
2.称量:用托盘天平称量所需的氯化钠的质量,倒入烧杯里。
3.量取:把水的密度近似看作1g/cm3。用 ml(量程)的量筒量取 ml水。
4.溶解:把量好的水倒入小烧杯里,用玻璃棒搅拌,使氯化钠溶解。
5.把配制的溶液倒入指定的容器中。
注意事项:1.称量3.0 g食盐时,将游码移到3.0g刻度处,不需要再另加砝码。称量食盐时,在天平两边托盘上各垫一张相同大小的纸片。加食盐时,用药匙取适量食盐,倾斜药匙,左手叩击右手手腕,将食盐慢慢洒到纸片上,至天平恰好平衡时为止。
2.量取47.0 mL水用100 mL量筒,若有50 mL量筒,则用50 mL量筒。
评分表 配制质量分数为5%的氯化钠溶液

浏览实验报告填写步骤一。
1.正确取出天平放在试验台中间,取下天平底座的橡皮垫,用镊子游码拨到零再调节平衡螺母至天平平衡。
2.在托盘两边各放一张滤纸,左手扶住天平杠杆,右手用镊子将游码调节到3克。
3.取出食盐试剂瓶,取下瓶塞倒放,用药匙取食盐添加在左盘滤纸上至天平平衡(第一勺可直接加入,第二勺要有左手轻轻拍打右手腕,如果多加了可用药匙取出重新添加,剩余食盐要放入指定回收的容器中)。
4.将食盐倒入烧杯中备用。再将滤纸取下,用镊子将游码拨回零处,塞上橡皮垫后将天平放回原处。
5.取出50毫升量筒(若没有可有100毫升)与试验台中。
6.取出蒸馏水试剂瓶向量筒中直接倾倒接近47毫升的水(次操作学生离开板凳蹲下,左手按住量筒底部,右手握住蒸馏水试剂瓶倾倒)。再改有胶头滴管吸取蒸馏水滴加,滴管要始终垂直于量筒口正上方,视线与47毫升刻度保持水平。当凹液面达到47刻度时停止滴加,将滴管内多余液体挤入到废液缸中,放回滴管。盖上瓶塞将蒸馏水放回原处。 7.将量筒内水倒入到放有食盐的烧杯中,并将量筒放回原处。取玻璃棒搅拌至食盐完全溶解(一只手的手指用力拿紧玻璃棒顺时针搅拌,另一只手稳住烧杯底部,尽量不要接触到烧杯壁和底部发出碰撞声)。
8.将配好的溶液倒入指定容器中。
9。清洗烧杯和玻璃棒。填写实验报告。提交报告,考试结束。
第二篇:20xx年初中化学实验操作考试题
一、实验室制取氧气
(一)实验目的
1、学会氧气的实验室制取及验满方法。
2、学会仪器的组装,装置气密性的检查,药品的取用。
(二)实验用品
铁架台(带铁夹)、大试管、带导管的单孔橡胶塞(与大试管配套)、烧杯、镊子、药匙、水槽、酒精灯、纸槽、高锰酸钾、棉花、集气瓶、玻璃片、火柴、试管刷。
(三)实验操作过程、现象及结论
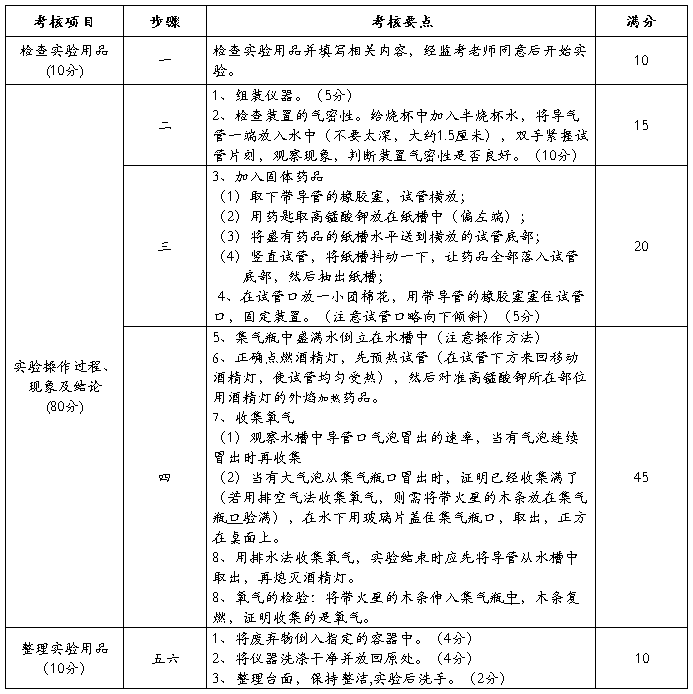
二、实验室制取二氧化碳
(一)实验目的
1、学会二氧化碳的实验室制取、验满及检验的方法。
2、学会仪器的组装,装置气密性的检查,药品的取用。
(二)实验用品
铁架台(带铁夹)、大试管、带导管的单孔橡胶塞(与大试管配套)、烧杯、镊子、大理石(或石灰石)、稀盐酸、澄清石灰水、集气瓶、玻璃片、火柴、试管刷。
(三)实验操作过程、现象及结论
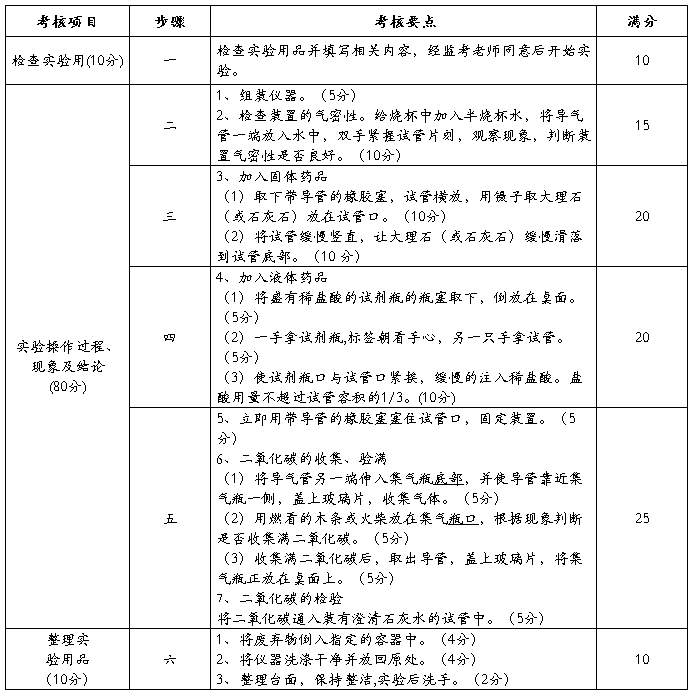
三、金属的主要化学性质
(一)实验目的
1、认识金属的主要化学性质。
2、会用化学方法探究金属的活动性顺序。
3、学会液体和固体药品的取用。
(二)实验用品(10分)
镁带、锌粒、铁丝、铜片、稀盐酸、硫酸铜溶液、硝酸银溶液、胶头滴管、试管、镊子、砂纸、试管架、试管刷。
(三)实验操作过程、现象及结论
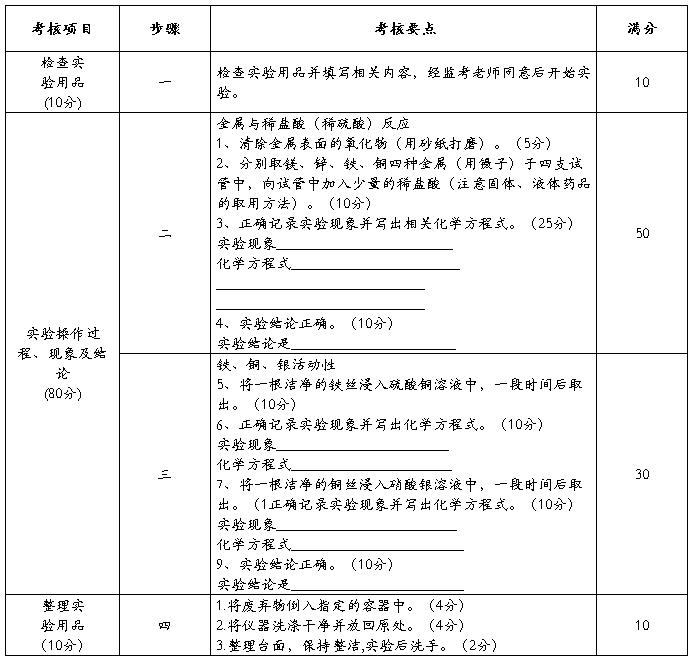
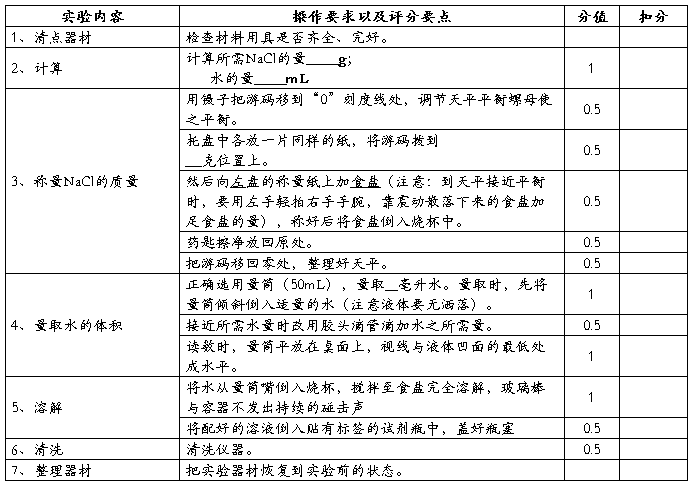
四、配制50g溶质质量分数为2%的氯化钠溶液
实验用品:
蒸馏水、食盐、托盘天平、镊子、烧杯、量筒、药匙、玻璃棒、试管刷、胶头滴管(放在盛水的烧杯中)、贴有一定溶质质量分数的氯化钠溶液标签(2%的氯化钠溶液)的试剂瓶、白纸片(大小质量相同)、抹布、废物杯。
实验要求:
(1)使用托盘天平称量一定质量的固体物质,选择适合量程的量筒量取一定体积的液体。
(2)配制一定溶质质量分数的溶液。
过程评分要点:
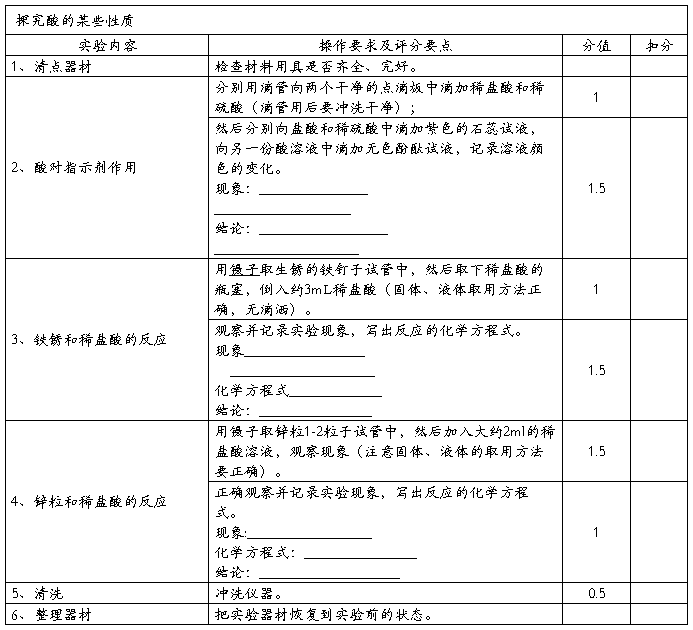
五、酸的化学性质
实验用品:
试管、点滴板、点滴板、胶头滴管、稀盐酸、稀硫酸、生锈的铁钉、石蕊试液、酚酞试液、氢氧化钠溶液等。
实验要求:
探究酸的化学性质。
过程与记录:
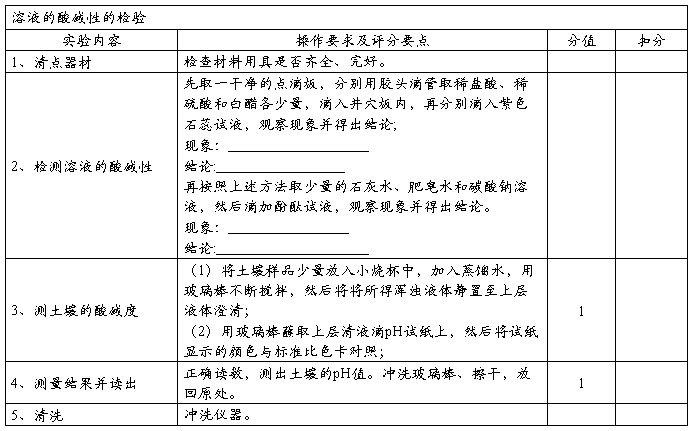
六、溶液酸碱性的检验
实验用品:
稀盐酸、稀硫酸、白醋、氢氧化钠溶液、石灰水、肥皂水、碳酸钠溶液、玻璃棒、试管、试管架、点滴板、pH试纸、标准比色卡、清洁纸、污物杯、抹布、土壤样品等
实验要求:
1、测定溶液pH值。
2、正确判断溶液的酸碱性。
评分要点:
七、粗盐中难溶性杂质的去除
实验用品:
粗盐(盛放在广口瓶中)、铁架台(带铁圈)、漏斗、胶头滴管(放在盛水的烧杯中)、滤纸(圆形)、玻璃棒、100mL烧杯(2个)、蒸发皿、坩埚钳、石棉网、酒精灯、药匙、试管刷、纸片、抹布、火柴、污物杯等。
实验要求:
1、溶解、过滤和蒸发的基本操作。
2、混合物分离的方法。
过程评分要点: