2007届高考新课程标准“化学实验”版块分析
(含必修I 从实验到化学 化学选修VI实验化学)
一、新课程标准与06版高考考纲对比
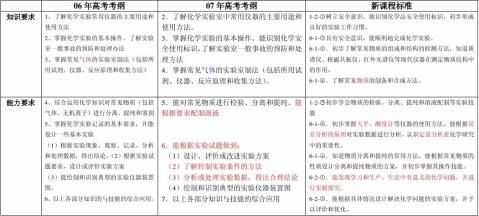
1
二、人教版新旧教材的对比
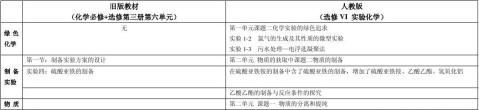
2

现人教版选修VI 与原人教版教材比较:
3
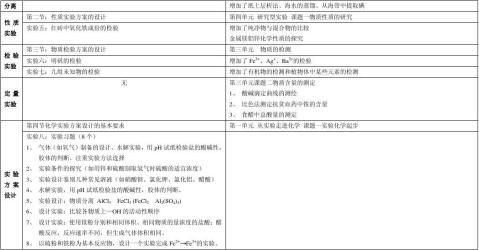
四个单元9个课题从不同的方向对实验进行研究,其中每个课题都有2-3个实验。 1、 注重与过去学过的知识的联系,在讨论与方案设计阶段,注重知识体系的完整性。 2、 注重实验方案的优化 3、 注重实验中现象的观察 4、 注重对实验结果的讨论
5、 注重了对数据处理能力的要求(特别是图形与图表的内容)。
三、化学高中新课程标准建议探究点与各版本教材的对比

4
5
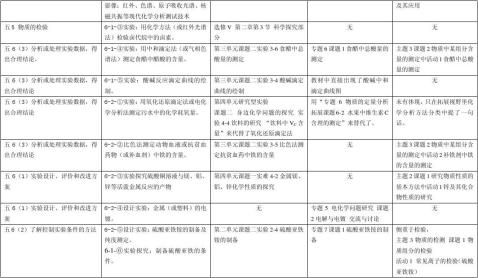
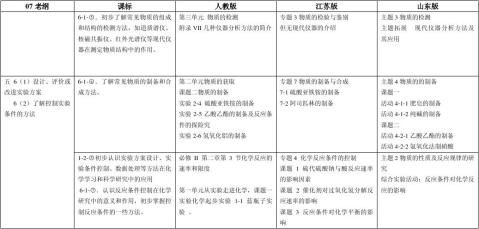
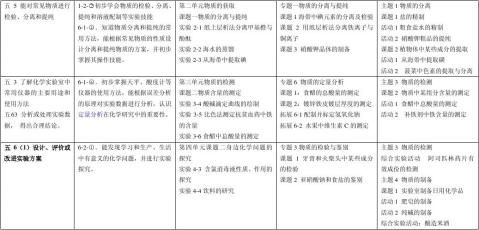
高中化学新课程标准与教材内容的对应
6
7
8
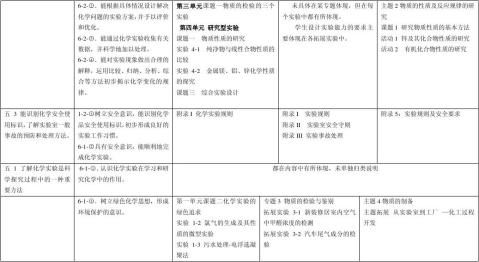
四、不同版本教材编排方式的比较
1、人教版、江苏版、山东版的实验化学教材中,实验方案设计大多数都是以程序图的方式来体现。因此要训练学生学习用程序图的方式来进行实验设计过程。
2、三个版本的教材基本都覆盖了课标上所有内容,但都对课标的建议的探究点进行了取舍与补充。
3、从新实验仪器的使用方法和新技术的应用方面,江苏版几乎为空白,而人教版和山东版都有所涉及。但仪器的布氏漏斗和移液管(课程标准解读里专门提出),人教版一点也未提及,特别是移液管的使用,需要补充。
4、对实验方法的整理与归纳方面,从系统性和科学性的角度出发:江苏版与山东版比人教版设计得更加出色。但从学生自主构建知识体系的角度,人教版更能体现学生的参与精神。
5、从实验方案设计这方面教材设计,人教版从一般到规律,层层深入,更符合学生认知规律,再用学生实验加深与巩固规律,从这一点来看更加出色。
6、从讨论与交流的设置上看:人教版更注重对方法的体悟,但依学生的实际情况,可能也更需要教师的指引。
7、从三个版本的实验设计上看,大量用到元素化合物的知识,这个部分也是人教版必修I中比较薄弱的一部分,需要教师引领的复习。(在实验手册中有相关的应知应会内容,教师可根据其复习)
五、复习中的教学建议
1、化学选修VI不作为考试内容,但选修VI中的实验思想和实验方法还是有必要进行梳理和归纳。
2、部分新仪器的使用如pH计、色度计与图表和数字分析结合紧密,有必要从原理上进行分析。
3、部分新方法如纸层析法可能会作为一种分离方法的补充,可能重要性不会太强。
4、建议部分实验在相关内容复习部分把这些实验思想和实验方案以题目的形式渗透和补充进去。
5、建议复习中,在元素化合物复习完毕后,把物质制备,物质的提纯等部分实验仪器用途、操作;实验方案设计、表达等进行个小专题复习。以便引领有机和化学反应原理部分实验的复习。
6、实验中数据分析和处理能力(含误差分析),有结论的要求,但也会联系到数据的计算。
7、如果不进行选修六实验内容的渗透,可考虑挖掘其它五个模块的的实验内涵,进行各专项的重点复习。
9
六、实施教学中的建议:
1、教学模式实施步骤:
(1)课堂组织形式:
对于以前接触过的实验:
“讨论+总结+设计+实验+讨论+练习”的模式
对于以前没接触过的实验:
“阅读+讨论+实验+总结+讨论+练习”的模式
(2)学生实验取舍的问题:
对于类型相同的实验,可以选用其中一个来重点做,其它的选做;对于三本教材上不同的实验可以选做。
2、学生实验能力的培养方式
(1)实验用品选取
让学生在实验设计中,填写要选用的仪器和药品,培养学生对药品和仪器用途的认识。大量的实验全部让实验员在短时间去准备完毕也是不现时的,考虑学生在实验用品选取方面的需要,分批安排学生去协助实验员准备实验,加深对实验药品与仪器选用的理解。经过一两次实验准备后,仪器与药品学生实验仪器和药品选用的“科学性”和“适用性”在方案设计中大大提高。
(2)实验方案的设计与评价
在课堂教学中,根据教材介绍的实验方法,对学生上交的典型实验设计进行讨论和评价。再让学生修改自已的实验设计,让其更为合理。如在含氯消毒液性质作用的研究中,方法有很多种,全让学生实验是不可能实现的,对于某些实验室不能提供的实验,采取同学讨论和点评的方法来评价。当然由于现在的学生对价格不敏感,很多方案从原理上说是可行的,但在实际中不可能采用,但作为一种方案也要给予肯定和表扬。
(3)实验操作的规范性
实验规范操作一向是化学实验考查的重点,两名同学一组进行实验,一人操作一人记录错误操作和提醒实验注意事项;然后两人互换。老师注意巡视同学发现不了的一些错误操作。
(4)实验数据的处理能力
针对一些定量实验得出的实验数据,要求进行对比分析,误差分析。并让学生学会用图形去求解(如pH曲线及比色曲线)
(5)实验结论的讨论
针对真实实验中出现的结论,通过同学讨论进行分析,排除错误结果,并进行错误分析。如在比色法中有同学就因为H2O2加入的量不足导导致溶液不变红,结果无法比色。如在纸色谱进行物质分离时,由于点的大小导致分离不完全的现象。
10
11
第二篇:仪器分析实验
实验一 紫外-可见分光光度法测定水中苯酚的含量(3学时)
一、实验目的
1. 学习使用UV757CRT紫外可见分光光度计。
2.掌握紫外-可见分光光度法测定水中微量苯酚含量的方法。
二、实验原理
紫外-可见吸收光谱属分子吸收光谱法,当分子吸收到外来的辐射能量(光区范围在200-800 nm)时,分子外层价电子发生能级跃迁,进而产生吸收光谱。紫外光谱具有灵敏度高、准确度好、仪器价格低廉、操作简便等许多优点,主要应用于化合物的定量分析。其定量分析的主要依据为朗伯-比尔定律
A = ebc
式中,A---吸光度,e--化合物的摩尔消光系数(L/(mol cm)),b—比色皿厚度(cm),c—溶液浓度(mol/L)。
根据上述公式,吸光度与溶液浓度呈线性关系,如已知某物质的摩尔吸光系数,就可以根据吸光度值得出待测溶液的摩尔浓度。
三、实验仪器、试剂

四、实验步骤
1. 打开电源,开机进行自检。
2. 配制苯酚标准溶液
a. 精确称取苯酚0.3000 g,放入1 L容量瓶中,加蒸馏水摇匀,定容至刻度;
b. 分别精确量取上述标准液2.0、3.0、4.0、5.0、6.0 ml,分别定容至50 ml,按序编号。
3. 绘制苯酚的标准吸收曲线
取上述3(4)号标准液,放置于1 cm的吸收池内(4/5),以蒸馏水为参比溶液,在190-400 nm波长范围内进行扫描,绘制苯酚的标准吸收曲线,并选取272 nm附近最大吸收波长为本实验的入射波长。
4. 绘制吸光度-浓度工作曲线
分别取上述配制的5组溶液,放置于1 cm的吸收池内(4/5),以蒸馏水为参比溶液,以上述选定的入射波长为测定波长,测定其吸光度值,并绘制成吸光度-浓度曲线,计算得到回归方程。
5. 待测溶液浓度的测定
取待测苯酚溶液,放置于1 cm的吸收池内(4/5),以蒸馏水为参比溶液,以上述选定的入射波长为测定波长,测定其吸光度值,代入回归方程中,计算待测溶液的克浓度和摩尔浓度(mol/L);并通过朗伯-比尔公式计算苯酚的摩尔吸光系数。
五、结果与讨论
1. 标准溶液

回归方程: 相关系数:R2 =
吸光度-浓度工作曲线
2. 待测溶液

3. 摩尔吸光系数
文献: L.mol -1.cm -1 实测: L.mol -1.cm -1
六、注意事项
1. 除去扫描苯酚的标准吸收曲线外,其余的每组实验均须平行做三次,然后取平均值;
2. 在自检过程和扫描过程中,不要按动任何键,不要打开样品室的盖子;
3. 注意保护吸收池,特别是石英比色皿,吸收池的光学面必须保持清洁,严禁用手触摸,如果光学面有污渍或尘土时,可用擦镜纸轻轻拭去;
4. 吸收池内部应用去离子水进行清洗,然后用少量丙酮或乙醇除水,常温下放置干燥;
七、思考题
在苯酚的吸收曲线中有两个吸收峰,本实验选用272 nm作为入射波长,是否可以用210 nm作测定波长,为什么?
实验二 固体、液体样品红外吸收光谱的测定与分析(2学时)
一、实验目的
1. 了解红外光谱仪的基本构造、组成及各部件的作用、使用维护过程中应注意的事项等;
2. 掌握红外光谱分析固体样品的制样技术;
3. 掌握红外光谱分析液体样品的制样技术;
4. 掌握根据红外光谱特征吸收峰鉴别特定官能团。
二、实验原理
1. 当样品受到频率连续变化的红外光照射时,物质分子吸收了某些频率的辐射,并由其振动或转动运动而引起偶极矩的净变化,产生分子振动和转动能级从基态到激发态的跃迁,使相应于这些吸收区域的透射光强度减弱。记录红外光的百分透射比(或吸光度)与波数关系曲线,就得到红外光谱,根据谱带的位置、峰形及强度,对待测样品进行分析。
2. 将固体样品与卤化碱(通常是KBr)混合研细,并压成(半)透明片状,然后放到红外光谱仪上进行分析,即为压片法。
3. 液体池通常由后框架、窗片框架、垫片、后窗片、间隔片、前窗片以及前框架七部分组成。使用时,将液体池倾斜30°,用注射器(不带针头)吸取待测样品,由下孔注入直到上孔有样品溢出为止,用聚四氟乙烯塞子塞住上、下注射孔,然后用高质量的纸巾擦去溢出的样品后,即可进行测试。
三、实验仪器、试剂

四、实验步骤
1. 取出红外光谱仪样品仓中的干燥剂,打开电脑及红外光谱仪主机电源,预热10 min;
2. 打开相应的红外操作软件,检查仪器工作状态并设置实验参数(分辨率2 cm-1,扫描次数32次);
3. 取少量 (1-2 mg) 待测的固体样品,然后与一定比例(样品量的100-200倍)的KBr在玛瑙研钵中仔细研磨均匀(平均粒径﹤2 μm),放入红外快速干燥箱中,加热干燥2分钟;
4. 将研磨干燥好的样品分散均匀地装入模具中,然后用压片机进行压片,压力不能超过20 MPa,并维持此压力1 min左右;
5. 在压片的同时,点击操作软件菜单中的“采集样品”,待采集完背景后,将压好的片放入红外光谱仪主机的样品架上;
6. 点击软件操作窗口的“确定”,开始采集样品的红外光谱图,采集完毕后进行自动(或手动)标峰,并保存谱图;
7. 对所得谱图进行解析,给出可能的结构。
五、结果与讨论
要求给出样品A、B可能的结构式,并给出特征吸收峰及相应在的官能团。
六、注意事项
1. 溴化钾样品的浓度和片的厚度应适当,在样品研磨、放置的过程中应特别注意干燥;
2. 切不可用手触摸NaCl,KBr盐片表面,用丙酮清洗盐片,用镜头纸或脱脂棉擦拭后,放入干燥器中保存;
3. 取下压制好的片时,应十分小心,防止将片弄裂;
4. 一张合格的红外光谱图,其最低透光率不应低于65%,且不能出现毛刺峰和平头峰等非正常峰。
七、思考题
1. 压片实验中加KBr的作用是什么?
2. 影响固体样品红外光谱图质量的因素是什么?
实验三 高效液相色谱法的应用-芳香烃的分离(3学时)
一、实验目的
1. 熟悉高效液相色谱仪的基本结构组成,初步掌握其使用方法;
2. 理解色谱分离分析原理,了解实验条件选择的依据;
3. 掌握根据保留时间定性和积分面积归一化法(外标)定量的分析方法。
二、实验原理
色谱法是利用混合物中各组分物理化学性质(吸附力、分配系数等)的差异使各组分在两相(固定相、流动相)中的分布程度不同,从而使各组分以不同速度移动而达到分离的目的。
高效液相色谱法是在经典色谱法的基础上,引用了气相色谱的理论,将流动相改为高压输送,色谱柱以特殊方法用小粒径填料填充,同时柱后配有高灵敏度的检测器,具有很高的分离效果,可实现定性和定量分析。
采用非极性的十八烷基键合相 (ODS) 为固定相和极性的甲醇-水溶液为流动相的反相色谱分离模式特别适合于同系物如苯系物等的分离。苯系物和稠环芳烃具有共轭双键,但因共轭体系的大小和极性不同,在固定相和流动相之间的分配系数不同,在柱内的移动速率不同而先后流出柱子。苯系物和稠环芳烃在紫外光区有明显的吸收,可以利用紫外检测器进行检测。在相同的实验条件下,可以将测得的未知物的保留时间与已知纯物质作对照而进行定性分析。
由于各组分在检测波长的摩尔吸收系数不同,同样浓度组分的峰面积不相等,因而,在以峰面积或峰高为依据进行归一化定量分析时,需经校正因子校正后方可达到准确定量的要求。但在以外标法进行定量分析时,由于是在相同实验条件下对同一组分进行检测,因而不需要考虑校正因子,可根据试样和标样中组分的色谱峰面积(或峰高)Ai和As及标样中的质量分数w。直接计算出试样中组分的质量分数。

三、实验仪器、试剂

四、实验步骤
1. 配制样品和标准溶液,并用相应的0.45微孔滤膜过滤
用甲醇分别配制苯、萘、联苯单组分及三组分混合样品各一份,浓度约为0.1-0.5 g/L。
2. 开启总电源,依次开启低压泵、高压泵、检测器、色谱工作站和电脑电源;单击桌面上EC2000图标,打开色谱工作站。
3. 在高压泵控制面板上设置实验参数:a: 流速1.0 ml/min b: 流动相为甲醇:水=80:20 c: 检测波长:254 nm。
4. 用本实验所使用的流动相(流动相使用前须经超声脱气)冲洗系统管路,同时进行基线的平衡,检查各管路是否有漏液,观察高压泵控制面板上的压力波动(不应超过1 MPa)。
5. 待基线平衡后,准备进样:将手动进样阀旋纽旋到Load的位置,用50 ml平头微量进样器抽取40 ml待测样品,排除进样器中的气泡,将样品注入手动进样阀中,再将旋纽旋到Inject的位置,点击开始,进行数据采样。
共测5组数据:苯标样、萘标样、联苯标样、混和标样、待测样品,每次采样完,均须用流动相清洗色谱柱(至少10分钟)。
6. 全部采样结束后,更换甲醇流动相,清洗管路和色谱柱(20-30 min左右)。与开机顺序相反,依次关闭色谱工作站、检测器、高压泵、低压泵。保存实验数据,生成HPLC检测报告,进行分析。
五、结果与讨论
1. 标准样品

2. 待测样品

六、注意事项
在实验过程中,必须排掉管路中所有的气泡;
七、思考题
1. 紫外检测器是否适用于所有有机化合物,为什么?
2. 高效液相色谱与气相色谱相比,有何优点?
