金属及其化合物
一. 金属的物理性质:
钠:银白色,有金属光泽,质软,密度小于水,大于煤油,熔点低,电和热的良导体。
铝:银白色,有金属光泽,质软,有良好的延展性,是热和电的良导体。
铁:纯铁是银白色的有金属光泽的固体,有磁性,可以被磁铁吸引,有延展性,是电和热的良导体。
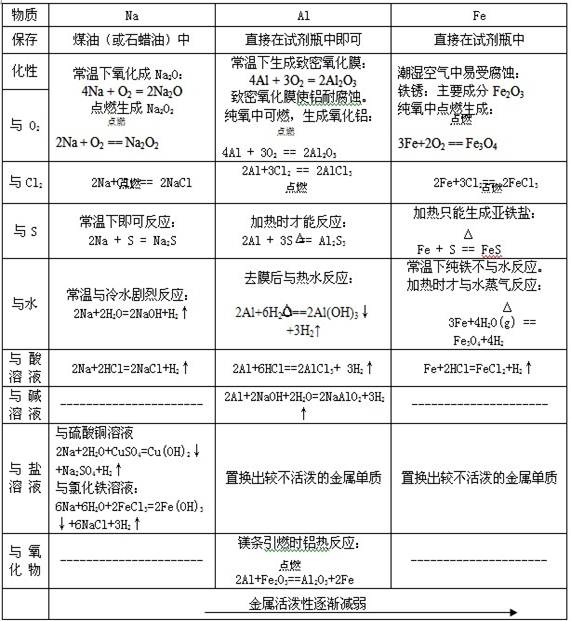
单质
1、与非金属反应(O2、Cl2、S):表现强还原性,被氧化
1)常温下:4Na + O2=== 2Na2O (白色)
常温下金属钠在空气中表面变暗,生成氧化膜,说明钠比Al、Fe活泼得多
(应用)钠保存在石蜡油或煤油中,因为钠易与水或者空气中的氧气反应,而钠不与煤油反应,且钠的密度大于煤油的密度,所以保存在煤油中。
2)受热时:2Na + O2=== Na2O2 (淡黄色)
(现象)钠在空气中受热后,先熔化成闪亮的小球后剧烈燃烧产生黄色火焰,生成淡黄色固体
2、与水反应:2Na + 2H2O == 2NaOH + H2↑ (分析电子得失)
现象:

(应用)钠燃烧引起火灾,怎么办?(一般用砂土盖灭)
3、与酸反应:2Na + 2HCl == 2NaCl + H2↑(比水更剧烈)
小练:
1、将一小块新切的不规则形状的金属钠投入到滴有酚酞溶液的水中,观察到下列现象,其中可说明钠与水反应放出气体的现象是( )
A、金属钠浮在水面上 B、金属钠形成小球状
C、金属钠在水面上迅速游动 D、反应后的溶液呈现红色
2、将一小块钠投入到盛有煤油和水的试管中(煤油和水均足够多),可以观察到的现象是 ( )
A.钠浮在煤油层上,不反应 B.钠沉在煤油层下,不反应
C.钠沉在煤油层下,浮在水层上,在交界处剧烈反应 D.钠沉在水层下剧烈反应
3、能正确表示下列反应的离子方程式的是( )
A.钠与水反应:2Na+2H2O===2Na++2OH-+H2↑B.钠与CuSO4溶液反应:2Na+Cu2+===Cu+2Na+
C.钠与盐酸反应:Na+2H+===Na++H2↑D.钠跟氯化钾溶液反应:2Na+2H2O===2Na++2OH-+H2↑
典型例题:1、将Na、Mg、Al各0.3mol分别放入100ml1mol/L
的盐酸中,同温同压下产生的气体体积比是 ( )
A.1:2:3 B.6:3:2 C.3:1:1 D.1:1:1
2. 金属钠露置在空气中最后生成什么物质?用图表示之。
3、在盛有5mL饱和石灰水的试管中放入一小块块钠,不可能观察到的现象是 ( )
A.钠熔成小球并在液面上游动 B.有气体生成 C.试管底部有银白色物质生成 D.溶液变浑浊
4. 相同质量的铝,分别与足量的强酸、强碱反应,产生氢气体积比为__________.
5. 某无色溶液中放入铝片后有氢气放出,则下列离子在该溶液中肯定可以大量共存的是( )
 A.Na+ B.Mg2+ C.S2- D.HCO3-
A.Na+ B.Mg2+ C.S2- D.HCO3-
6.如图在玻璃管中放入还原铁粉和石棉绒的混合物.加热并通入水蒸气.用试管收集产生的经干燥的气体,并靠近火焰点火。
(1)所观察到的现象是 ____________________,有关反应的化学方程式是 ____________________。
(2) 干燥管内可装入的试剂是___________,其作用是___________。干燥管还可用___________(装置)代替。
(3) 玻璃管中石棉绒的作用是__________________。实验开始时应先点燃____________,实验结束时,应先熄灭____________________。
三、金属氧化物的性质
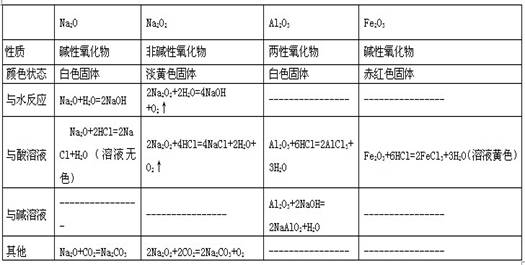
四.金属氢氧化物
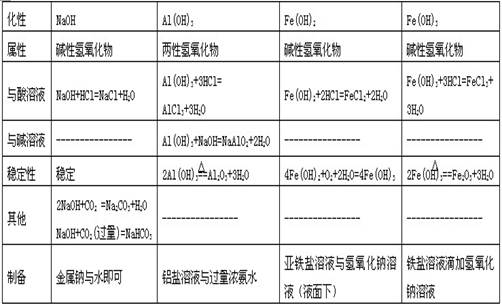
典型例题:1不能用NaOH溶液 除去括号中的杂质的是( )
A. Mg( Al2 03) B.MgCl2( AlC13) C. Fe(Al) D.Fe2O3( Al203)
2、向Al2(SO4)3溶液中滴加下列试剂,有沉淀产生,且沉淀不会因加入试剂过量而消失的是( )
A、NaOH溶液 B、氨水 C、NaCl溶液 D、BaCl2溶液
3、往100ml 0.1mol/L 的Al2(SO4)3溶液中加入 0.5mol/L的NaOH溶液,得到1.17克沉淀,则加入的NaOH溶液的体积是( ) A.70ml B.90ml C . 130ml D.160ml
4、CO和H2的混合气体共3 g,与足量的过氧化钠置于密闭容器中,通入足量氧气用电火花点燃,则固体的质量增加了 ( ) A.3 g B.3.2 g C.4.4 g D.5.6 g
5、在一定条件下,将钠与氧气反应的生成物1.5 9溶于水,所得溶液恰好能被80 ml。浓度为0.50 mol/L的HCl溶液中和,则该生成物的成分是 ( )
A.Na2O B.Na2O2 C.Na2O和Na2O2 D.Na2O2和NaO2
6、在含有Fe3+、Fe2+、Al3+、NH4+的稀溶液中,加入足量的Na2O2固体,充分反应后,再加入过量的稀盐酸,完全反应后,离子数目几乎没有变化的是( )A.Fe3+ B. Al3+ C. NH4+ D .Fe2
五、盐
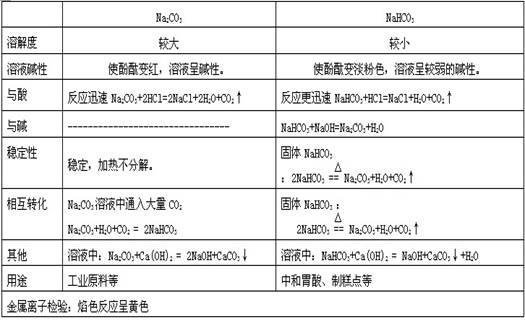
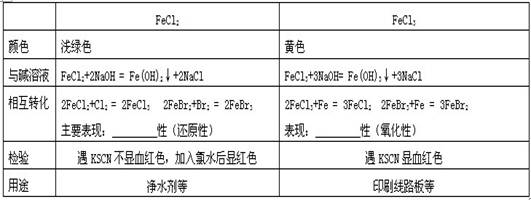
典型例题:1.下列物质中能通过化合反应制取的是( ) ①Fe3O4 ②Fe(OH)3 ③FeCl2 ④FeCl3
A.①④ B.①②④ C.①③④ D.①②③④
2.下列物质跟铁反应后的生成物与KSCN溶液作用一定会产生红色溶液的是( )
A.盐酸 B.Fe2(SO4)3溶液 C.氯气 D.CuSO4溶液
3.在电子工业中,制印刷电路时,常用氯化铁溶液作为铜的“腐蚀液”,该过程发生的反应为:2FeCl3+Cu=2FeCl2+CuCl2。该反应利用了铜的什么性质( )A .氧化性 B.还原性 C.导电性 D. 导热性
4. 在FeCl3、CuCl2的混合溶液中,加入一定量的铁屑,反应完全后将固体滤出,下列说法中正确的是( )
A .若滤出的固体中只有铜,则溶液中一定含有的阳离子是Fe2+,一定不含Cu2+ ;
B.若滤出的固体中含有铁和铜,则溶液中一定含有的阳离子是Fe2+,一定不含Cu2+和Fe3+
C.若滤出的固体中只有铜,则溶液中一定含有的阳离子是Fe2+,可能含有Cu2和Fe3+
D.若滤出的固体中只有铜,则溶液中一定含有的阳离子是Fe3+和Fe2+,一定不含Cu2

课后练习题:
1.下列实验能证明某无色气体为SO2的是( )
①能使澄清石灰水变浑浊 ②能使湿润的蓝色石蕊试纸变红③能使品红溶液褪色,加热后又显红色
④能使溴水褪色,再滴加酸化的BaCl2溶液有白色沉淀产生
A.①②③④ B.①③④ C.③④ D.②③④
2.为了加速漂白粉的漂白作用,最好的方法是( )
A.加入苛性钠溶液 B.用水湿润 C.加少量稀盐酸 D.加热干燥使用
3.下列化学反应的离子方程式正确的是( )
A.在稀氨水中通入过量CO2:NH3·H2O+CO2===NH4++HCO3-
B.少量SO2通入Ca(ClO)2溶液中:SO2+H2O+Ca2++2ClO-===CaSO3↓+2HClO
C.用稀HNO3溶解FeS固体:FeS+2H+===Fe2++H2S↑
D.氢氧化钙溶液与等物质的量的稀硫酸混合:Ca2++OH-+H++SO42-===CaSO4↓+H2O
4.在不同的化学反应里,既能表现酸性,又能表现氧化性和还原性的酸是( )
A.浓H2SO4 B.HNO3 C.HCl D.H2O
5.请用下列装置设计一个实验,证明Cl2的氧化性比I2的氧化性强。
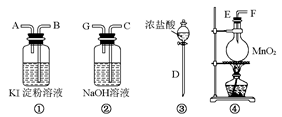
请回答下列问题:
(1)若气流从左到右,则上述仪器的连接顺序为D接E,_________接_________,_______接_______。
(2)圆底烧瓶中发生反应的化学方程式为__________________________。
(3)证明Cl2比I2的氧化性强的实验现象是______________________,反应的离子方程式是_________________。
(4)装置②的作用是__________________。
(5)若要证明Cl2的氧化性比Br2强,则需做的改动是__________________________。
5.黄铜矿(CuFeS2)是制取铜及其化合物的主要原料之一,还可制备硫及铁的化合物。
(1)冶炼铜的反应为8CuFeS2+21O28Cu+4FeO+2Fe2O3+16SO2。若CuFeS2中Fe的化合价为+2,则反应中被还原的元素是__________(填元素符号)。
(2)对上述冶炼过程中产生的大量SO2,下列处理方案中合理的是__________(填字母)。
a.高空排放 b.用于制备硫酸 c.用纯碱溶液吸收制Na2SO3
(3)利用黄铜矿冶炼铜产生的炉渣(含Fe2O3、FeO、SiO2、Al2O3)可制备Fe2O3。
炉渣NaOH溶液,过滤Ⅰ沉淀盐酸、H2O2Ⅱ溶液NaOH溶液ⅢFe(OH)3△ⅣFe2O3
①步骤Ⅰ中发生的两个反应的离子方程式分别为
____________________________________________、____________________________________________。
②步骤Ⅱ的目的是将铁的氧化物溶解并将Fe2+氧化成Fe3+,则Fe2+发生氧化反应的离子方程式为________________________________________________________________
