光的粒子性
【考纲要求】

 说明:相比10年,新考试说明中删去了康普顿效应
说明:相比10年,新考试说明中删去了康普顿效应
【知识要点】
1.光电效应
概念:在光(包括不可见光)的照射下,从物体发射 的现象叫做光电效应。
2.光电效应的实验规律
(1)存在遏止电压
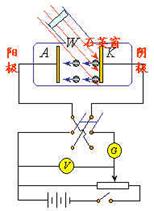 如图所示,光线经石英窗照在阴极上,便有电子逸出----光电子。
如图所示,光线经石英窗照在阴极上,便有电子逸出----光电子。
光电子在电场作用下形成光电流。
概念:遏止电压
将换向开关反接,电场反向,则光电子离开阴极后将受反向电场阻碍作用。
当 K、A 间加反向电压,光电子克服电场力作功,当电压达到某一值 Uc 时,光电流恰为0。 Uc称遏止电压。
根据动能定理,有

实验表明,无论光的强弱如何,遏止电压都是一样的。光的频率改变时,遏止电压也会改变,这表明光电子的能量只与入射光的频率有关,而与入射光的强弱无关。
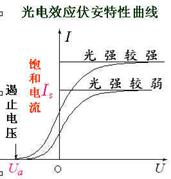
(2) 光电流与光强的关系:
饱和光电流强度与入射光强度成正比。
(3) 截止频率νc ----极限频率
对于每种金属材料,都相应的有一确定的截止频率νc 。
当入射光频率ν>νc 时,电子才能逸出金属表面;
当入射光频率ν <νc时,无论光强多大也无电子逸出金属表面。
 (4)光电效应是瞬时的。从光开始照射到光电子逸出所需时间<10-9s。
(4)光电效应是瞬时的。从光开始照射到光电子逸出所需时间<10-9s。
3.光电效应解释中的疑难
经典理论无法解释光电效应的实验结果。
经典理论认为,按照经典电磁理论,入射光的光强越大,光波的电场强度的振幅也越大,作用在金属中电子上的力也就越大,光电子逸出的能量也应该越大。也就是说,光电子的能量应该随着光强度的增加而增大,不应该与入射光的频率有关,更不应该有什么截止频率。
光电效应实验表明:饱和电流不仅与光强有关而且与频率有关,光电子初动能也与频率有关。只要频率高于极限频率,即使光强很弱也有光电流;频率低于极限频率时,无论光强再大也没有光电流。
光电效应具有瞬时性。而经典认为光能量分布在波面上,吸收能量要时间,即需能量的积累过程。
为了解释光电效应,爱因斯坦在能量子假说的基础上提出光子理论,提出了光量子假设。
4.爱因斯坦的光量子假设
(1)内容
光不仅在发射和吸收时以能量为hν的微粒形式出现,而且在空间传播时也是如此。也就是说,频率为ν的光是由大量能量为 E =hν的光子组成的粒子流,这些光子沿光的传播方向以光速 c 运动。
(2)爱因斯坦光电效应方程

在光电效应中金属中的电子吸收了光子的能量,一部分消耗在电子逸出功 W 0,另一部分变为光电子逸出后的动能 E k 。由能量守恒可得出:
W0为电子逸出金属表面所需做的功,称为逸出功
Wk为光电子的最大初动能。
(3)爱因斯坦对光电效应的解释:
①光强大,光子数多,释放的光电子也多,所以光电流也大。
②电子只要吸收一个光子就可以从金属表面逸出,所以不需时间的累积。
③从方程可以看出光电子初动能和照射光的频率成线性关系
④从光电效应方程中,当初动能为零时,可得极限频率: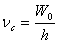
爱因斯坦光子假说圆满解释了光电效应,但当时并未被物理学家们广泛承认,因为它完全违背了光的波动理论。
5.光电效应理论的验证
美国物理学家密立根,花了十年时间做了“光电效应”实验,结果在1915年证实了爱因斯坦光电效应方程,h 的值与理论值完全一致,又一次证明了“光量子”理论的正确。
由于爱因斯坦提出的光子假说成功地说明了光电效应的实验规律,荣获1921年诺贝尔物理学奖。
 密立根由于研究基本电荷和光电效应,特别是通过著名的油滴实验,证明电荷有最小单位。获得1923年诺贝尔物理学奖。
密立根由于研究基本电荷和光电效应,特别是通过著名的油滴实验,证明电荷有最小单位。获得1923年诺贝尔物理学奖。
6.光电效应在近代技术中的应用
(1)光控继电器
可以用于自动控制,自动计数、自动报警、自动跟踪等。
(2)光电倍增管
 可对微弱光线进行放大,可使光电流放大105~108倍,灵敏度高,用在工程、天文、科研、军事等方面。
可对微弱光线进行放大,可使光电流放大105~108倍,灵敏度高,用在工程、天文、科研、军事等方面。
【巩固练习】
1.光照射到金属表面上,能使金属中的_________从表面逸出,这种现象称之为______________,逸出的电子也叫____________,使电子脱离金属表面所做的功的最小值叫____________,这种现象说明光具有____________性。
2.经典的电磁理论只能解释光是一种,它有____________、____________等波特有的现象,但它不能解释光电效应。爱因斯坦对光电效应的解释是:光本身就是由一个一个不可分割的____________组成的,每一个光的能量子被称为一个____________,这就是爱因斯坦的_________说。
3.爱因斯坦认为,在光电效应中,金属中的电子吸收一个频率为ν的光子获得的能量是_________,这些能量中的一部分用来克服金属的____________,剩下的表现为逸出的光电子的____________,用公式表示为____________________,这就是著名的爱因斯坦光电效应方程。
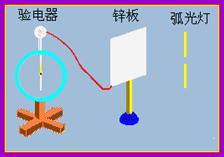
4.在演示光电效应的实验中,原来不带电的一块锌板与灵敏验电器相连,用弧光灯照射锌板时,验电器指针张开一个角度,如图所示,这时 ( )
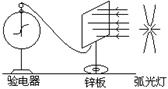 A.锌板带正电,指针带负电
A.锌板带正电,指针带负电
B.锌板带正电,指针带正电
C.锌板带负电,指针带正电
D.锌板带负电,指针带负电
5.对于任何一种金属,必须满足下列哪种条件,才能发生光电效应 ( )
A.入射光的强度大于某一极限强度
B.入射光的波长大于某一极限波长
C.入射光照射时间大于某一极限时间
D.入射光的频率大于某一极限频率
6.某种频率的光射到金属表面上时,金属表面有电子逸出,若光的频率不变而强度减弱,那么下述结论中正确的是 ( )
A.光的强度减弱到某一数值时,就没有电子逸出
B.逸出的电子数减少
C.逸出的电子数和最大初动能都减小
D.逸出的电子最大初动能不变
7.用两束频率相同,强度不同的紫外线去照射两种不同金属,都能产生光电效应,则( )
A.因入射光频率相同,产生光电子的最大初动能必相同
B.用强度大的紫外线照射时,所产生的光电子的初速度一定大
C.从极限波长较长的金属中飞出的光电子的初速度一定大
D.由强度大的紫外线所照射的金属,单位时间内产生的光电子数目一定多
8.用某一频率的绿光照射某金属时恰好能产生光电效应,则改用强度相同的蓝光和紫光分别照射该金属,下列说法正确的是 ( )
A.用蓝光照射时,光电子的最大初动能比用紫光照射时小
B.用蓝光和紫光照射时,在相同时间内逸出的电子数相同
C.用蓝光照射时,在同样时间内逸出的电子数目较多
D.用紫光照射时,在同样时间内逸出的电子数目较多
9.关于光电效应的说法中,正确的有 ( )
A.要使光电效应发生,入射光子的能量必须大于原子的电离能
B.极限频率的存在,可以表明电子对光子的吸收是一对一的
C.增大入射光子的能量,光电子的最大初动能必随着增大
D.电子对光子的吸收不存在能量的积累过程
10.已知铯的极限频率为4.55×1014Hz,钠的极限频率为6.00×1014Hz,银的极限频率为1.15×1015Hz,铂的极限频率为1.53×1015Hz,当用波长为0.375μm的光照射它们时,可发生光电效应的是 ( )
A.铯 B.钠 C.银 D.铂
11.某种金属的逸出功是1.25eV,为了使它发生光电效应,照射光的频率至少应为多少?或用可见光照射它,能否发生光电效应?
12.某金属在一束黄光照射下,刚好有电子逸出(即用频率小于黄光的光照射就没有电子逸出)。在下述情况下,电子的最大初动能及逸出的电子数目会发生什么变化?(1)增大光强而不改变光的频率;(2)用一束强度更大的红光代替黄光;(3)用强度相同的紫光代替黄光。
1、电子,光电效应,光电子,逸出功,粒子 2、干涉,衍射,能量子,光子,光子 3、hν,逸出功,初动能,hν=W+Ek 4、B 5、D 6、BD 7、CD 8、AB 9、AC 10、AB 11、3×1014Hz,可以 12、(1)最大初动能不变,光电子数目增加(2)无光电子逸出(3)最大初动能增大,光电子数目不变
第二篇:水的电离和溶液的酸碱性知识点总结
水的电离和溶液的酸碱性
一、水的电离
1. 水是一种极弱的电解质,水的电离是永恒存在的。只要是水溶液,不要忽略H+和
OH –的同时存在,注意不是大量共存。
(1)水分子能够发生电离,存在有电离平衡:
H2O+H2O  H3O++ OH – 简写为 H2O
H3O++ OH – 简写为 H2O  H++ OH –
H++ OH –
(2)水分子发生电离后产生的离子分别是H3O+ 和OH –
(3)发生电离的水分子所占比例很小
根据水的电离平衡,写出相应的平衡常数表达式
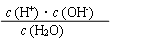 应有K电离=
应有K电离=
室温时,1L纯水中(即55.56mol/L)测得只有1×10-7molH2O发生电离,电离前后H2O的物质的量几乎不变,故c(H2O)可视为常数,上式可表示为:c(H+)·c(OH –)=K电离·c(H2O)
K电离与常数c(H2O)的积叫做水的离子积常数,用KW 表示
2.水的离子积
一定温度下,无论是稀酸、稀碱或盐溶液中
室温时KW=c(H+)·c(OH –) =1×10-14
水的电离是个吸热过程,故温度升高,水的KW增大。同样KW只与温度有关。
归纳:
①电离常数是表示弱电解质电离趋势的物理量。K值越大,电离趋势越大。
②一种弱电解质的电离常数只与温度有关,而与该弱电解质的浓度无关。
③电离常数随温度升高而增大。室温范围温度对电离常数影响较小,可忽略
④水的离子积不仅适用于纯水,也适用于酸、碱、盐稀溶液
⑤任何溶液中由水电离的c(H+)与c(OH –)总是相等的
3.影响水的电离平衡的因素:酸、碱、水解盐等。
二、溶液的酸碱性和pH
1.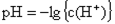
常温pH=7(中性) pH<7 (酸性) pH>7(碱性)
2.pH测定方法:pH试纸、酸碱指示剂、pH计
3.溶液pH的计算方法
(1)酸溶液: n (H+)→c(H+)→pH
(2)碱溶液:n(OH –) → c(OH –) →c(H+)=1×10-14/ c(OH –) →pH
(3)酸碱混合:
pH=7 n (H+)= n(OH –)
pH>7 n (H+)<n(OH –) c(OH –)= n(OH –) - n (H+)/V混合液→c(H+)→pH
pH<7 n (H+)> n(OH –) c(H+)= n (H+)- n(OH –) /V混合液→pH
4.特例。。。
三、溶液的pH与c(H+)变化关系
pH增大1个单位,c(H+)减小10倍;pH减小1个单位,c(H+)增大10倍;pH改变n个单位,c(H+)就改变10n倍。
