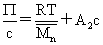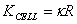 ,
,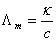 ,
,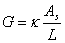 ,k=G
,k=G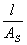 =
=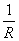
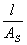
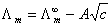 ,
, 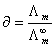 ,
,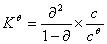
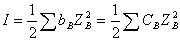

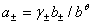 ,
,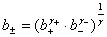 ,
, 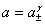 ,Q=
,Q=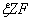
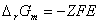 ,
, 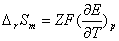 ,
,
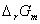 +
+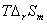
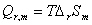 ,
, 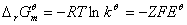
E=E
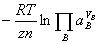 ,平衡时
,平衡时 =
=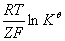
平动: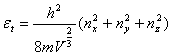 转动:
转动:
振动: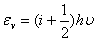
微态数:定域: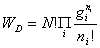 离域:
离域:
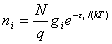 ,
, 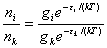
配分函数:平动: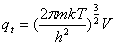 ,
,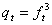
转动: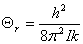 ,
, ,
,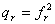
振动: ,
,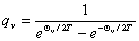 ,
,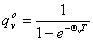
C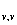 =R(
=R(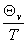 )
)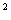
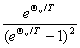 ,
,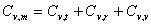
A=V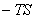 ,V=NKT
,V=NKT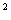
 ,S=NKln
,S=NKln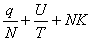
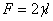


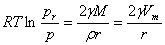
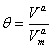

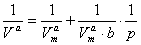
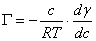 ,W
,W =
= ,
,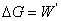 ,
,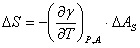
Q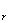 =T
=T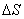 ,
,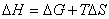 ,ln
,ln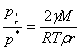
反应速率系数 k=Ae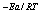 ,K=
,K=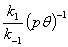 ,求活化能ln
,求活化能ln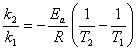
半衰期:零级 t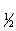 =C
=C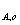
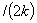 ;一级 t
;一级 t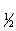 =
=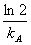 ;二级t
;二级t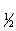 =
=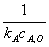
n级t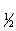 =
=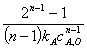
沾湿: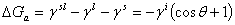
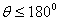
浸湿: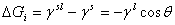


铺展: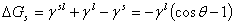
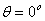 或不存在
或不存在
S=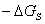 展铺的必要条件S
展铺的必要条件S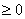
第二篇:大学物理化学必考公式总结
物理化学期末
重点复习资料
热力学第一定律
功:δW=δWe+δWf
(1)膨胀功 δWe=p外dV 膨胀功为正,压缩功为负。
(2)非膨胀功δWf=xdy
非膨胀功为广义力乘以广义位移。如δW(机械功)=fdL,δW(电功)=EdQ,δW(表面功)=rdA。
热 Q:体系吸热为正,放热为负。
热力学第一定律: △U=Q—W 焓 H=U+pV
理想气体的内能和焓只是温度的单值函数。
热容 C=δQ/dT
(1)等压热容:Cp=δQp/dT= (?H/?T)p
(2)等容热容:Cv=δQv/dT= (?U/?T)v
常温下单原子分子:Cv,m=Cv,mt=3R/2
常温下双原子分子:Cv,m=Cv,mt+Cv,mr=5R/2
等压热容与等容热容之差:
(1)任意体系 Cp —Cv=[p+(?U/?V)T](?V/?T)p
(2)理想气体 Cp —Cv=nR
理想气体绝热可逆过程方程:
pVγ=常数 TVγ-1=常数 p1-γTγ=常数 γ=Cp/ Cv
理想气体绝热功:W=Cv(T1—T2)=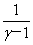 (p1V1—p2V2)
(p1V1—p2V2)
理想气体多方可逆过程:W= (T1—T2)
(T1—T2)
热机效率:η= 冷冻系数:β=-Q1/W
冷冻系数:β=-Q1/W
可逆制冷机冷冻系数:β=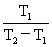
焦汤系数: μJ-T=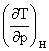 =-
=-
实际气体的ΔH和ΔU:
ΔU= +
+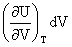 ΔH=
ΔH=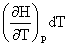 +
+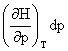
化学反应的等压热效应与等容热效应的关系:Qp=QV+ΔnRT
当反应进度 ξ=1mol时, ΔrHm=ΔrUm+ RT
RT
化学反应热效应与温度的关系: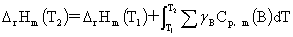
热力学第二定律
Clausius不等式: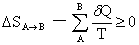
熵函数的定义:dS=δQR/T Boltzman熵定理:S=klnΩ
Helmbolz自由能定义:F=U—TS Gibbs自由能定义:G=H-TS
热力学基本公式:
(1)组成恒定、不作非膨胀功的封闭体系的热力学基本方程:
dU=TdS-pdV dH=TdS+Vdp
dF=-SdT-pdV dG=-SdT+Vdp
(2)Maxwell关系:
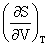 =
=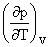
 =-
=-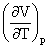
(3)热容与T、S、p、V的关系:
CV=T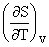 Cp=T
Cp=T
Gibbs自由能与温度的关系:Gibbs-Helmholtz公式 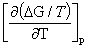 =-
=-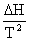
单组分体系的两相平衡:
(1)Clapeyron方程式: =
=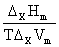 式中x代表vap,fus,sub。
式中x代表vap,fus,sub。
(2)Clausius-Clapeyron方程式(两相平衡中一相为气相):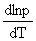 =
=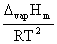
(3)外压对蒸汽压的影响: pg是在惰性气体存在总压为pe时的饱和蒸汽压。
pg是在惰性气体存在总压为pe时的饱和蒸汽压。
吉不斯-杜亥姆公式:SdT-Vdp+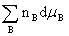 =0
=0
dU=TdS-pdV+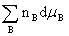 dH=TdS+Vdp+
dH=TdS+Vdp+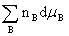
dF=-SdT-pdV+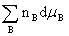 dG=-SdT+Vdp+
dG=-SdT+Vdp+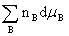
在等温过程中,一个封闭体系所能做的最大功等于其Helmbolz自由能的减少。等温等压下,一个封闭体系所能做的最大非膨胀功等于其Gibbs自由能的减少。
统计热力学
波兹曼公式:S=klnΩ
一种分布的微观状态数:定位体系:ti=N!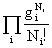 非定位体系:ti=
非定位体系:ti=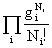 波兹曼分布:
波兹曼分布: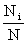 =
=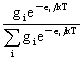
在A、B两个能级上粒子数之比: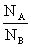 =
=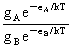
波色-爱因斯坦统计:Ni= 费米-狄拉克统计:Ni=
费米-狄拉克统计:Ni=
分子配分函数定义:q=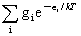 -
-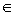 i为能级能量
i为能级能量
q=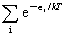 -
-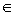 i为量子态能量
i为量子态能量
分子配分函数的分离:q=qnqeqtqrqv
能级能量公式:平动:εt=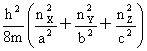
转动:εr=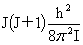 振动:εv=
振动:εv=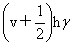
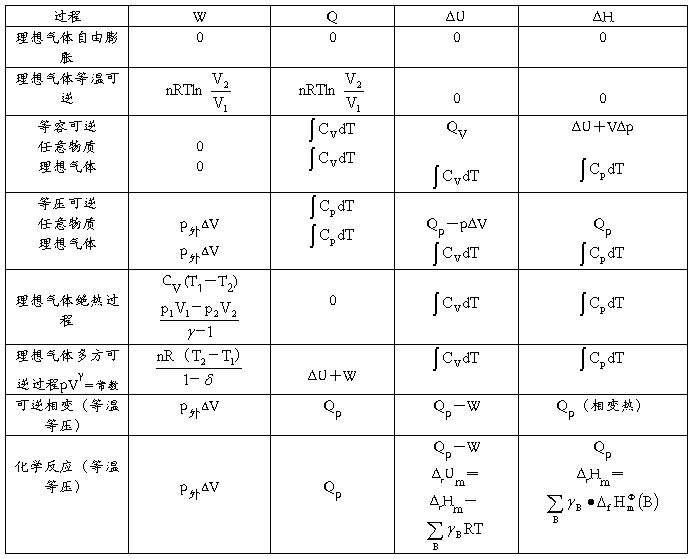
一些基本过程的ΔS、ΔG、ΔF的运算公式(Wf=0)
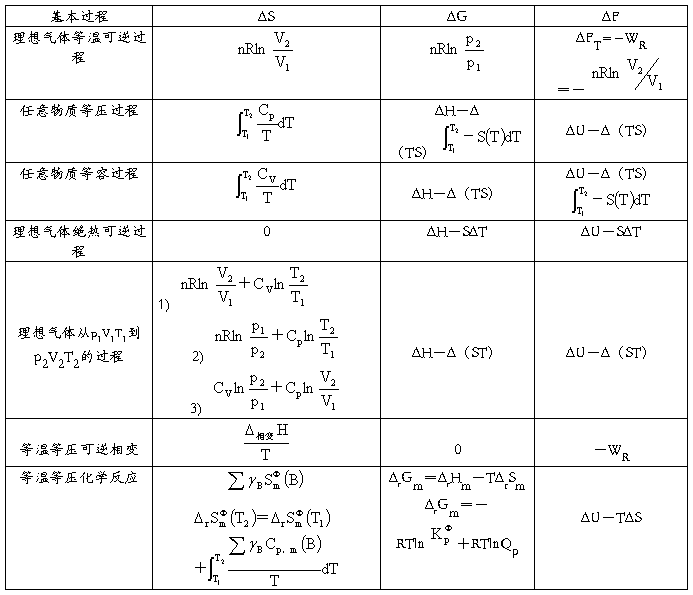
一些基本过程的W、Q、ΔU、ΔH的运算公式(Wf=0)
溶液-多组分体系体系热力学在溶液中的应用
溶液组成的表示法:(1)物质的量分数: (2)质量摩尔浓度:
(2)质量摩尔浓度: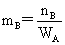 (3)物质的量浓度:
(3)物质的量浓度: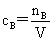 (4)质量浓度
(4)质量浓度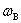
拉乌尔定律  亨利定律:
亨利定律:
化学势的各种表示式和某些符号的物理意义:
气体:
(1)纯理想气体的化学势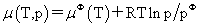 标准态:任意温度,p=pφ=101325Pa。μφ(T)为标准态时的化学势
标准态:任意温度,p=pφ=101325Pa。μφ(T)为标准态时的化学势
(2)纯实际气体的化学势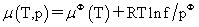 标准态:任意温度,f=pφ且复合理想气体行为的假想态(即p=pφ,γ=1),μφ(T)为标准态时的化学势。
标准态:任意温度,f=pφ且复合理想气体行为的假想态(即p=pφ,γ=1),μφ(T)为标准态时的化学势。
(3)混合理想气体中组分B的化学势 因为
因为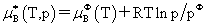 所以
所以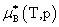 不是标准态时的化学势,是纯B气体在指定T、p时的化学势。
不是标准态时的化学势,是纯B气体在指定T、p时的化学势。
溶液:
(1) 理想溶液组分的化学势

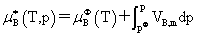
所以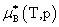 不是标准态时的化学势而是温度为T、溶液上方总压为p时,纯液体B的化学势。
不是标准态时的化学势而是温度为T、溶液上方总压为p时,纯液体B的化学势。
(2) 稀溶液中各组分的化学势
溶剂: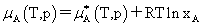
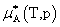 不是标准态时的化学势而是温度为T、溶液上方总压为p时,纯溶剂A的化学势。
不是标准态时的化学势而是温度为T、溶液上方总压为p时,纯溶剂A的化学势。
溶质:
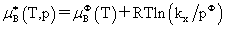
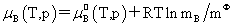
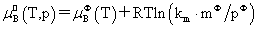
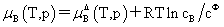
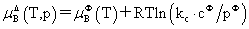
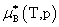 ,
,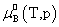 ,
,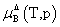 均不是标准态时的化学势,均是T,p的函数,它们分别为:当xB=1,mB=1molkg-1,cB=1moldm-3时且服从亨利定律的那个假想态的化学势。
均不是标准态时的化学势,均是T,p的函数,它们分别为:当xB=1,mB=1molkg-1,cB=1moldm-3时且服从亨利定律的那个假想态的化学势。
(4)非理想溶液中各组分的化学势
溶剂: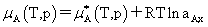
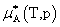 不是标准态的化学势,而是aA,x=1即xA=1,γA=1的纯组分A的化学势。
不是标准态的化学势,而是aA,x=1即xA=1,γA=1的纯组分A的化学势。
溶质:

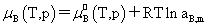
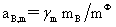
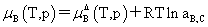

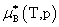 ,
,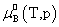 ,
,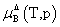 均不是标准态时的化学势,均是T,p的函数,它们分别为:当aB,x=1,aB,m=1,aB,c=1时且服从亨利定律的那个假想态的化学势。
均不是标准态时的化学势,均是T,p的函数,它们分别为:当aB,x=1,aB,m=1,aB,c=1时且服从亨利定律的那个假想态的化学势。
(4)活度a的求算公式:
ü 蒸汽压法:溶剂aA=γAxA=pA /pA * 溶质:aB=γBxB=pA /kc
ü 凝固点下降法:溶剂
ü Gibbs-Duhem公式从溶质(剂)的活度求溶剂(质)的活度。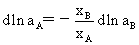
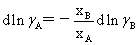
(5)理想溶液与非理想溶液性质:
理想溶液: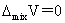

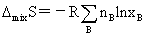

非理想溶液: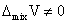

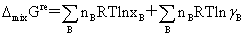
超额函数: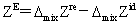
溶液热力学中的重要公式:
(1) Gibbs-Duhem公式
(2) Duhem-Margule公式: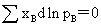 对二组分体系:
对二组分体系:
稀溶液依数性:
(1)凝固点降低:
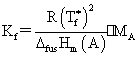
(2)沸点升高: 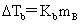
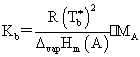
(3)渗透压: 
化平衡学
化学反应亲和势:A=-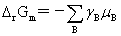
化学反应等温式: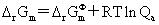
平衡常数的表达式:
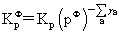
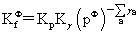


温度,压力及惰性气体对化学平衡的影响:
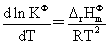
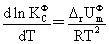
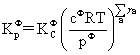
电解质溶液
法拉第定律:Q=nzF m=
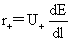
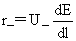
t+= =
=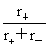 =
=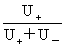 =
=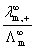 =
=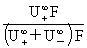
r+为离子移动速率,U+( U-)为正(负)离子的电迁移率(亦称淌度)。
近似: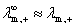
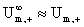
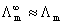 (浓度不太大的强电解质溶液)
(浓度不太大的强电解质溶液)
离子迁移数:tB=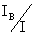 =
=
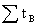 =
=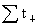 +
+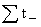 =1
=1
电导:G=1/R=I/U=kA/l
电导率:k=1/ρ 单位:S·m-1 莫尔电导率:Λm=kVm=k/c 单位S·m2·mol-1
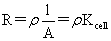

科尔劳乌施经验式:Λm=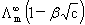
离子独立移动定律: =
=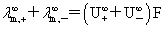
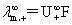
奥斯特瓦儿德稀释定律: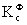 =
=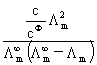
平均质量摩尔浓度: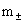 =
=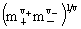
平均活度系数: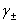 =
= 平均活度:
平均活度: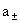 =
=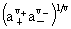 =
=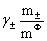
电解质B的活度:aB=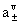 =
=
 m+=v+mB m-=v-mB
m+=v+mB m-=v-mB 
离子强度:I=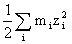
德拜-休克尔公式:lg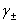 =-A|z+z--|
=-A|z+z--|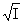
可逆电池的电动势及其应用
(ΔrG)T,p=-Wf,max (ΔrGm)T,p=zEF
Nernst Equation:若电池反应为 cC+dD=gG+hH
E=Eφ-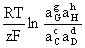
标准电动势Eφ与平衡常数Kφ的关系:Eφ=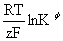
还原电极电势的计算公式: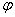 =
=
计算电池反应的有关热力学函数变化值: =
=
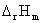 =-zEF+
=-zEF+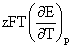 QR=T
QR=T =
=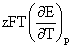
zF zF
zF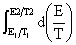 =
=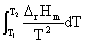
电极书面表示所采用的规则:负极写在左方,进行氧化反应(是阳极),正极写在右方,进行还原反应(是阴极)
电动势测定的应用:
(1)求热力学函数变量ΔrGm、ΔrGmΦ、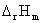 、
、 及电池的可逆热效应QR等。
及电池的可逆热效应QR等。
(2)求氧化还原反应的热力学平衡常数KΦ值:KΦ=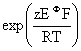 EΦ=
EΦ=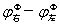 E=
E=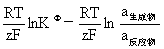
(3)求难溶盐的溶度积Ksp、水的离子积Kw及弱酸弱碱的电离常数等。
(4)求电解质溶液的平均活度系数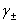 和电极的
和电极的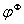 值。
值。
(5)从液接电势求离子的迁移数。Pt,H2(p)|HCl(m)|HCl(m’)| H2(p),Pt
1-1价型:Ej=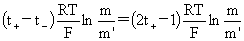 E=Ec+Ej=
E=Ec+Ej=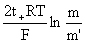
高价型:Mz+Az-(m1)|Mz+Az-(m2) Ej=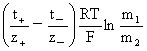
(6)利用醌氢醌电极或玻璃电极测定溶液的pH
电解与极化作用
E分解=E可逆+ΔE不可逆+IR
ΔE不可逆=η阴+η阳
η阴=(φ可逆-φ不可逆)阴 η阳=(φ不可逆-φ可逆)阳
φ阳,析出=φ阳,可逆+η阳 φ阴,析出=φ阴,可逆-η阴
η=a+blnj
E(实际分解)=E(理论分解)+η(阴)+η(阳)+IR
对电解池,由于超电势的存在,总是使外加电压增加而多消耗电能;对原电池,由于超电势的存在,使电池电动势变小而降低了对外作功的能力。
在阴极上,(还原)电势愈正者,其氧化态愈先还原而析出;同理,在阳机上,则(还原)电势愈负者其还原态愈先氧化而析出。(需外加电压小)
化学反应动力学
半衰期法计算反应级数:
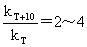

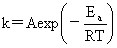

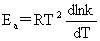
 kp=kc(RT)1-n Ea-Ea’=Q
kp=kc(RT)1-n Ea-Ea’=Q
化学反应动力学基础二:
ZAB=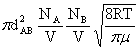 =
=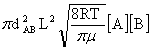 μ=
μ=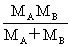
若体系只有一种分子:
ZAA=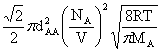 =
=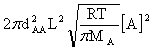
碰撞参数:b=dABsinθ
碰撞截面: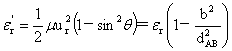
反应截面: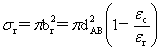
kSCT(T)=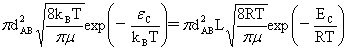
kSCT(T)=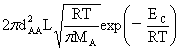
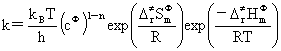 =
=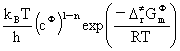
几个能量之间的关系:Ea=Ec+RT/2=E0+mRT=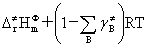
式中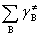 是反应物形成活化络合物时气态物质的代数和,对凝聚相反应,
是反应物形成活化络合物时气态物质的代数和,对凝聚相反应,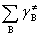 =0。对气相反应也可表示为:Ea=
=0。对气相反应也可表示为:Ea=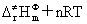 (式中n为气相反应的系数之和)
(式中n为气相反应的系数之和)
原盐效应: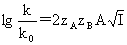
弛豫法:36.79%
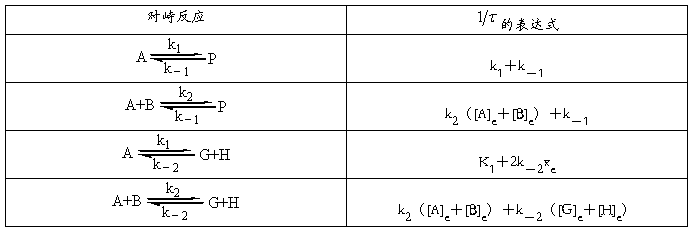
界面现象
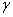 与T的关系:
与T的关系: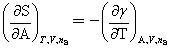
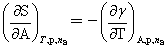
两边均乘以T,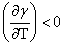 ,即
,即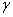 的值将随温度升高而下降,所以若以绝热方式扩大表面积,体系的温度必将下降。
的值将随温度升高而下降,所以若以绝热方式扩大表面积,体系的温度必将下降。
杨-拉普拉斯公式:ps
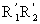 为曲率半径,若为球面
为曲率半径,若为球面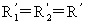
ps=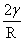 ,平面
,平面 ps
ps 。液滴愈小,所受附加压力愈大;液滴呈凹形,R‘为负值,ps为负值,即凹形面下液体所受压力比平面下要小。
。液滴愈小,所受附加压力愈大;液滴呈凹形,R‘为负值,ps为负值,即凹形面下液体所受压力比平面下要小。
毛细管:ps=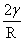 =Δρgh Δρgh=
=Δρgh Δρgh=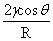 (R为毛细管半径)
(R为毛细管半径)
开尔文公式:p0和p分别为平面与小液滴时所受的压力
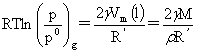
对于液滴(凸面R‘>0),半径愈小,蒸汽压愈大。
对于蒸汽泡(凹面R‘<0),半径愈小,蒸汽压愈小。
两个不同液滴的蒸汽压: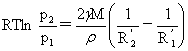
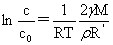 溶液越稀,颗粒越大。
溶液越稀,颗粒越大。
液体的铺展: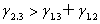
非表面活性物质使表面张力升高,表面活性物质使表面张力降低。
吉不斯吸附公式: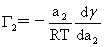
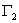 为表面超额
为表面超额
若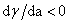 ,
,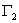 >0,正吸附;
>0,正吸附; ,
,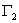 <0,负吸附。
<0,负吸附。
表面活性物质的横截面积:Am=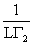
粘附功: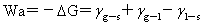 Wa值愈大,液体愈容易润湿固体,液固界面愈牢。
Wa值愈大,液体愈容易润湿固体,液固界面愈牢。
内聚功: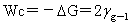 浸湿功:
浸湿功: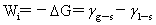
铺展系数: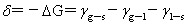
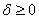 ,液体可在固体表面自动铺展。
,液体可在固体表面自动铺展。
接触角: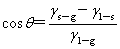
Langmuir等温式: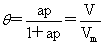 θ:表面被覆盖的百分数。
θ:表面被覆盖的百分数。
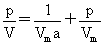 离解为两个分子:
离解为两个分子: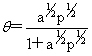
混合吸附: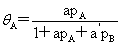
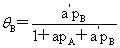 即:
即: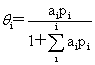
BET公式: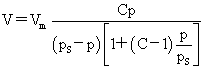
弗伦德利希等温式: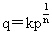 乔姆金吸附等温式:
乔姆金吸附等温式: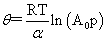
吸附剂的总表面积:S=AmLn n=Vm/22400cm3mol-1
气固相表面催化反应速率:单分子反应: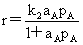 (产物吸附很弱)
(产物吸附很弱)
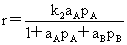 (产物也能吸附)
(产物也能吸附)
双分子反应: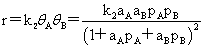 (AB都吸附)
(AB都吸附)
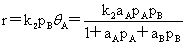 (AB均吸附,但吸附的B不与吸附的A反应)
(AB均吸附,但吸附的B不与吸附的A反应)
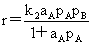 (B不吸附)
(B不吸附)
胶体分散体系和大分子溶液
布朗运动公式: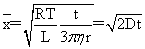 (D为扩散系数)
(D为扩散系数)
球形粒子的扩散系数: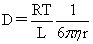
渗透压: 渗透力:F=
渗透力:F=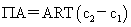 扩散力=-F
扩散力=-F
沉降平衡时粒子随高度分布公式: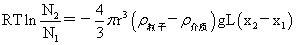
瑞利公式: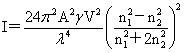
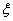 电势 表面电势
电势 表面电势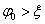 Stern电势
Stern电势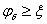 电解质浓度增加
电解质浓度增加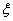 电势减小。
电势减小。
电泳速度: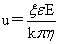 k=6时为电泳,k=4时为电渗。
k=6时为电泳,k=4时为电渗。
大分子稀溶液渗透压公式: