第一章 物质结构 元素周期律
一、原子结构
 质子(Z个)
质子(Z个)
 原子核 注意:
原子核 注意:
中子(N个) 质量数(A)=质子数(Z)+中子数(N)
 1.原子(
A X ) 原子序数=核电荷数=质子数=原子的核外电子数
1.原子(
A X ) 原子序数=核电荷数=质子数=原子的核外电子数
核外电子(Z个)
★熟背前20号元素,熟悉1~20号元素原子核外电子的排布:
H He Li Be B C N O F Ne Na Mg Al Si P S Cl Ar K Ca
2.原子核外电子的排布规律:①电子总是尽先排布在能量最低的电子层里;②各电子层最多容纳的电子数是2n2;③最外层电子数不超过8个(K层为最外层不超过2个),次外层不超过18个,倒数第三层电子数不超过32个。
电子层: 一(能量最低) 二 三 四 五 六 七
对应表示符号: K L M N O P Q
3.元素、核素、同位素
元素:具有相同核电荷数的同一类原子的总称。
核素:具有一定数目的质子和一定数目的中子的一种原子。
同位素:质子数相同而中子数不同的同一元素的不同原子互称为同位素。(对于原子来说)
二、元素周期表
1.编排原则:
①按原子序数递增的顺序从左到右排列
②将电子层数相同的各元素从左到右排成一横行。(周期序数=原子的电子层数)
③把最外层电子数相同的元素按电子层数递增的顺序从上到下排成一纵行。
主族序数=原子最外层电子数
2.结构特点:
核外电子层数 元素种类
 第一周期 1 2种元素
第一周期 1 2种元素
 短周期 第二周期 2 8种元素
短周期 第二周期 2 8种元素
 周期 第三周期 3 8种元素
周期 第三周期 3 8种元素
 元 (7个横行) 第四周期 4 18种元素
元 (7个横行) 第四周期 4 18种元素
素 (7个周期) 第五周期 5 18种元素
周 长周期 第六周期 6 32种元素
期 第七周期 7 未填满(已有26种元素)
 表 主族:ⅠA~ⅦA共7个主族
表 主族:ⅠA~ⅦA共7个主族
族 副族:ⅢB~ⅦB、ⅠB~ⅡB,共7个副族
(18个纵行) 第Ⅷ族:三个纵行,位于ⅦB和ⅠB之间
(16个族) 零族:稀有气体
三、元素周期律
1.元素周期律:元素的性质(核外电子排布、原子半径、主要化合价、金属性、非金属性)随着核电荷数的递增而呈周期性变化的规律。元素性质的周期性变化实质是元素原子核外电子排布的周期性变化的必然结果。
2.同周期元素性质递变规律

第ⅠA族碱金属元素:Li Na K Rb Cs Fr (Fr是金属性最强的元素,位于周期表左下方)
第ⅦA族卤族元素:F Cl Br I At (F是非金属性最强的元素,位于周期表右上方)
★判断元素金属性和非金属性强弱的方法:
(1)金属性强(弱)——①单质与水或酸反应生成氢气容易(难);②氢氧化物碱性强(弱);③相互置换反应(强制弱)Fe+CuSO4=FeSO4+Cu。
(2)非金属性强(弱)——①单质与氢气易(难)反应;②生成的氢化物稳定(不稳定);③最高价氧化物的水化物(含氧酸)酸性强(弱);④相互置换反应(强制弱)2NaBr+Cl2=2NaCl+Br2。
(Ⅰ)同周期比较:

(Ⅱ)同主族比较:

(Ⅲ)
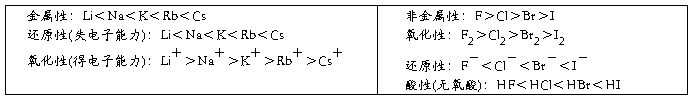
比较粒子(包括原子、离子)半径的方法:(1)先比较电子层数,电子层数多的半径大。
(2)电子层数相同时,再比较核电荷数,核电荷数多的半径反而小。
对除稀有气体元素原子以外的任何原子或离子的半径进行比较要“三看”:
① 首先看层,层少半径小;
② 同层看核,核大半径小;
③ 同核看价,价高半径小.
四、化学键
化学键是相邻两个或多个原子间强烈的相互作用。

1.离子键与共价键的比较
离子化合物:由离子键构成的化合物叫做离子化合物。(一定有离子键,可能有共价键)
共价化合物:原子间通过共用电子对形成分子的化合物叫做共价化合物。(只有共价键)
 极性共价键(简称极性键):由不同种原子形成,A-B型,如,H-Cl。
极性共价键(简称极性键):由不同种原子形成,A-B型,如,H-Cl。
共价键
非极性共价键(简称非极性键):由同种原子形成,A-A型,如,Cl-Cl。
2.电子式:
用电子式表示离子键形成的物质的结构与表示共价键形成的物质的结构的不同点:(1)电荷:用电子式表示离子键形成的物质的结构需标出阳离子和阴离子的电荷;而表示共价键形成的物质的结构不能标电荷。(2)[ ](方括号):离子键形成的物质中的阴离子需用方括号括起来,而共价键形成的物质中不能用方括号。
第二篇:高中化学必修一第一章知识点梳理
第一章知识梳理
一、化学实验安全
1、药品取用
(1)安全原则:不允许用手,鼻子,嘴
(2)节约原则:按量取;未规定用量,固体药品盖过试管底部,液体取1-2ml
(3)保纯性原则:实验剩余药品既不能放回原试剂瓶,也不能随意丢弃,要放入指定容器。(钠,钾,镁条,锌粒等可以放回原试剂瓶)
2、药品取用
(1)块状或金属颗粒:一横,二放,三慢立
(2)固体粉末:一斜,二送,三直立
(3)液体:拿下瓶塞,倒放桌面上,倾倒时瓶上标签向着手心防止瓶口残留药液留下来腐蚀标签,同时瓶口紧挨试管口缓慢倾倒
取用块状或颗粒状药品用镊子,粉末状药品用药匙或纸槽,少量液体用胶头滴管(胶头滴管应在试管口上部悬空,不能插入试管内)
3、物质加热
可直接加热的仪器:试管,坩埚,蒸发皿,燃烧匙
隔石棉网加热的仪器:烧杯,烧瓶,锥形瓶
酒精灯使用:添加酒精不超过容积三分之二,禁止向燃着酒精灯加酒精,禁止用一个酒精灯点燃另一个酒精灯,用灯帽盖灭,不许用嘴
试管加热前要预热,防止局部受热使试管炸裂。加热试管液体时,液体体积不超过试管容积三分之一,45°倾斜,管口不对人。
4、药品存放
(1)受热或见光易分解的物质存放在棕色瓶中(浓硝酸,硝酸银)
(2)金属钠保存在煤油中,易和氧气,水反应,白磷着火点低(40摄氏度)在空气中自燃,保存在冷水中。
5、实验意外事故处理方法
(1)酸沾到皮肤,立即用水冲洗,再用3%-5%碳酸氢钠冲洗,碱沾到皮肤,用水冲洗,涂上硼酸溶液
(2)眼睛被化学药品灼伤,立即用大量水冲洗,边洗边眨眼间
(3)苯酚灼伤,先乙醇洗,后用水
(4)磷灼伤,用硫酸铜溶液涂抹伤处
(5)酒精失火,用湿抹布扑盖,钠,磷失火用细沙
(6)贡洒落后,撒上硫粉,打开排气扇。
十个危险化学药品标志(书上) 有害气体处理(点燃式,直接吸收式,收集式)
二、混合物的分离和提纯
1、过滤:分离出不溶于水的固体物质,仪器,注意事项:一贴,二低,三靠
2、蒸发:从溶液中分离出固体物质方法,仪器(铁架台带铁圈),注意事项:安装仪器顺序,先酒精灯,后铁圈高度。用玻璃棒不断搅动溶液,防止局部温度过高,液滴飞溅。当蒸发皿中出现较多固体时停止加热,利用余热蒸干,防止晶体过热飞溅。
3、蒸馏:利用沸点不同分离液态混合物,仪器,注意事项:加碎瓷片或沸石,防瀑沸。温度计水银球与蒸馏烧瓶支管口相平。冷凝管水流由下而上。液体体积在三分之一和三分之二之间。齐去开始时收集到的馏份。蒸馏烧瓶加热要垫石棉网。检查气密性
4、萃取分液:利用物质在互不相容的溶剂里溶解度的不同,用一种溶剂把物质从它另一种溶剂所组成的溶液里提取出来的方法。萃取剂选取原则:与原溶剂互不相容,不与溶质溶剂反应;溶质在萃取剂中的溶解度远大于在原溶剂中的溶解度。操作:见书 注意事项:使用之前检查是否漏水,在分液漏斗中注入少量的水,塞上瓶塞,倒置看是否漏水;若不漏水,把瓶塞旋转180°,在倒置看是否漏水。分液要领:见书
常见的萃取剂:密度小于水的:苯,汽油 大于水的:四氯化碳
常见离子检验:硫酸根:氯化钡和稀硝酸
氯离子:硝酸银和稀硝酸
碳酸根:稀盐酸和澄清的石灰水
粗盐提纯:粗盐成分:不溶性泥沙,可溶性氯化钙氯化镁以及一些硫酸盐
步骤:溶解,过滤,蒸发
除去可溶性杂质:注意加的试剂和滴加的顺序
三、化学计量在实验中的应用

阿伏伽德罗定律及推论:(理想气体状态方程)
VP=nRT MP=pRT
配置一定物质的量浓度溶液:
