“化学实验报告”型试题例析
化学是一门以实验为基础的学科,化学实验不仅有利于学生理解和巩固化学知识,更重要的是可以培养学生科学的思维方式和科学的研究方法,提高分析、解决实际问题的能力。
化学的实验教学,形式多样,从认识方法上可分为验证性实验和探索性实验;从内容上可分为化学基本操作实验、物质性质和制备实验、运用“双基”进行的设计性实验等等。但不论做哪种类型的实验,要求教师让学生在平时的实验课上多亲自体验实验探究的过程,多动手实验,并做到实验前进行实验预习和认真填写实验报告的好习惯。实验报告是实验的书面表达,也是培养学生科学素养的重要技能。
例1.碘是人体必需的微量元素之一,研缺乏病是世界上发病人数最多的地方病,我国通过食盐加碘来消除碘缺乏病。请回答下列问题:
(1)人体缺乏碘可导致那些疾病?_______________ ;
(2)在碘盐里,碘以KIO3形式存在,怎样检验KIO3?(可供选择的试剂有:稀硝酸、稀盐酸、KCI、KI、淀粉溶液、石蕊试液)________________________ ;
(3)正确食用碘盐才能起到以补碘的作用,某班同学在以下两个问题上产生了分歧;
①油炸食品时是否适宜放碘盐?
②做凉拌菜时碘盐是否适宜跟醋一起使用?
请你选择其中一个问题进行研究:
你选的课题名称是:______________________ 。
你设计的研究方案是:___________________ 。
你的研究成果的最终形式是:__________________ 。
解答:(1)人体缺乏碘可导致甲状腺肿大、大脑功能障碍、智力低下、生长发育停滞、呆小病等。
(2)取少量样品溶解后,加入稀盐酸和KI溶液,再加入淀粉溶液,若显蓝色,则有KIO3存在。
(3)若选①,课题名称:油炸食品时是否适宜放碘盐?(或温度对KIO3稳定性的影响…等)
研究方案:(关于不同温度下KIO3稳定性的对比方案,凡合理的均可。)
若选②,课题名称:做凉拌菜时碘盐是否适宜跟醋一起使用?(或酸对KIO3稳定性的影响……等)
研究方案:(关于不同酸度下KIO3稳定性的对比方案,凡合理的均给分。)
研究成果的最终形式:研究报告、实验报告、论文……等。
例1.某同学做同周期元素性质递变规律实验时,自己设计了一套实验方案,并记录了有关实验现象如下表。
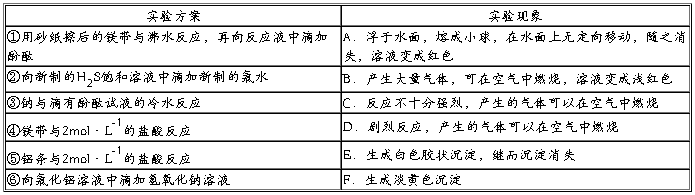
请你帮助该同学整理并完成实验报告。
(1)实验目的:________________________________________________________。
(2)实验用品。仪器___________________;药品___________________________。
(3)实验内容:(*填写题给信息表中的序号)

(4)实验结论:__________________________________________________________。
(5)请从结构理论上简单说明具有上述结论的原因。
(6)请你补充一组实验方案(简单易行),证明此周期中另外两种元素的性质递变规律。
解析:(1)先分析每个实验可得出的结论:通过实验①可得出镁跟水反应的难易、氢氧化镁的碱性强弱;通过实验②可得出Cl2能从H2S中置换出S;实验③钠跟水反应的难易、氢氧化钠的碱性强弱;实验④、⑤分别可得出镁、铝跟盐酸置换反应的难易;实验⑥可得出氢氧化铝是一种两性氢氧化物。把上述分析结果联成一个整体来看,可发现这6个实验都是研究第三周期元素的单质和化合物的性质,从中可定性地比较出钠、镁、铝三种元素的金属性强弱,氯、硫两种元素的非金属性强弱。所以,这一套实验的目的是"验证第三周期元素从左至右金属性递减、非金属性递增的规律。"
(2)联想每个实验的过程可知,这些实验中要用的仪器有:试管,酒精灯,砂纸,镊子,小刀,胶头滴管等。要用到的药品有:镁条,钠,铝条,新制氯水,新制饱和硫化氢溶液,2mol·L-1的盐酸,2mol·L-1的NaOH溶液,蒸馏水,酚酞,2mol·L-1的AlCl3溶液。
(3)根据元素周期表第三周期元素的排列顺序,作了有序地研究,可确定实验操作顺序和相关的实验现象等(如下表)。

(4)金属性:Na>Mg>Al;非金属性:S<Cl。
(5)从Na、Mg、Al、S、Cl,原子核外都有三个电子层,但最外层电子数依次为1、2、3、6、7,原子半径随电子数增多而减小,所以核对最外层电子的吸引力依次增强,原子失电子能力减弱,得电子能力增强。
(6)第三周期还有硫、硅两种元素,要完整的比较出这些元素的金属性和非金属性,必须要补充实验。联系到元素最高价含氧酸的酸性与元素非金属性的关系,可以比较硅酸、磷酸、硫酸的酸性强弱来比较Si、P、S元素的非金属性强弱。在中学化学知识范围内可设计出下列三种方案:
方案一:测定0.1mol·L-1的Na2SiO3、Na3PO4、Na2SO4的pH,由此判断三种盐溶液的水解能力,得出硅酸、磷酸、硫酸三种最高价含氧酸的酸性强弱顺序,进而得出硅、磷、氮三元素非金属强弱顺序。
方案二:测定相同浓度的硅酸、硫酸、磷酸溶液的pH。
方案三:在硅酸钠溶液中滴加磷酸溶液,可发生反应:SiO32-+H3PO4=H2SiO3↓+HPO4-。
在磷酸镁沉淀中滴加稀硫酸溶液,沉淀可溶解:Mg3(PO4)2+4H+=3Mg2++2H2PO4-。
例3.高中教材中钠的化合物一节中有这样一个实验:在两支试管中分别加入3mL稀盐酸(设此稀盐酸的浓度为4mol/L),将分别装有0.3gNaHCO3和0.3gNa2CO3粉末的小气球分别套在两支试管口。将气球内的NaHCO3和Na2CO3同时倒人试管中,观察到的现象及分析如下:
(1)比较两只试管中的现象:_______________________ 。
(2)若两气球内的压强相同.原试管大小相同,且试管中的液体体积相同,则大小气球体积之比约为________________________(填最简整数比)
(3)甲同学用:手触摸试管,发现盛NaHCO3粉末的试管变冷,而盛Na2CO3的试管温度升高。由此他得出:不管其状态如何? NaHCO3和HCl反应为吸热反应,而Na2CO3和HCl反应为放热反应。甲同学写出了下列热化学方程式(其中“aq”代表水合或无限稀释的含义):
HCO3-(aq)+H+(aq)=H2O(1)+CO2(g);△H>O;
CO32-(aq)+2H+(aq)=H2O(1)+CO2(g);△H<O;
甲分析结论的方法是否科学? _____。(填“是”或“否”)
(4)为研究反应是吸热还是放热,继续讲行下列实验验。(每个实验平行做三次,取平均值)

请填写相关内容:
①该研究报告的题目是《 》
②该实验中所用的仪器除托盘天平、试管、药匙(或V型纸槽)、气球、玻璃棒、烧杯、量筒、保温瓶外还需要的主要仪器是____________;③通过上述实验可得出五条结沦:
a.NaHCO3的溶解是——————(“吸热”或“放热”)过程;
b.Na2CO3的溶解是————(“吸热”或“放热”)过程;
c.NaHCO3的饱和溶液和盐酸的反应是_______(”吸热”或“放热”)反应;
d.Na2CO3的饱和溶液和盐酸的反应是______(“吸热”或“放热”)反应;
e.NaHCO3固体与稀盐酸反应的反应热是______(填a→d的字母)的热效应之和。
解析:试题取材于课本实验,第(1)问考查了对实验现象的观察,现象应是:两支试管中都产生大量气泡,但盛NaHCO3的试管中反应速率要快得多。第(2)问计算得53/42;第(3)问:手触摸试管显然不科学,因为反应放、吸热受量及浓度的相对多少,反应时间长短,晶体溶于水还有溶解热效应;实验报告题目应是对实验目的的概括,是实验的中心思想,体现了实验操作的目的,该实验报告题目应是:NaHCO3,Na2CO3 和盐酸反应过程中热效应的研究。认真阅读实验数据,分析前后温度变化,可得出相关五条结论。
答案:(1)两支试管中都产生大量气泡,但盛NaHCO3的试管中反应速率要快得多(2)53/42 (3)不正确(4)①《NaHCO3,Na2CO3 和盐酸反应过程中热效应的研究》(或相关内容) ②托盘天平、温度计 a .吸热 b.放热 c吸热 d.放热 e.a c。
第二篇:化学实验报告格式
化学实验报告格式
例一 定量分析实验报告格式
(以草酸中h2c2o4含量的测定为例)
实验题目:草酸中h2c2o4含量的测定
实验目的:
学习naoh标准溶液的配制、标定及有关仪器的使用;
学习碱式滴定管的使用,练习滴定操作。
实验原理:
h2c2o4为有机弱酸,其ka1=5.9×10-2,ka2=6.4×10-5。常量组分分析时cka1>10-8,cka2>10-8,ka1/ka2<105,可在水溶液中一次性滴定其两步离解的h+:
h2c2o4+2naoh===na2c2o4+2h2o
计量点ph值8.4左右,可用酚酞为指示剂。
naoh标准溶液采用间接配制法获得,以邻苯二甲酸氢钾标定:
-cook
-cooh
+naoh===
-cook
-coona
+h2o
此反应计量点ph值9.1左右,同样可用酚酞为指示剂。
实验方法:
一、naoh标准溶液的配制与标定
用台式天平称取naoh1g于100ml烧杯中,加50ml蒸馏水,搅拌使其溶解。移入500ml试剂瓶中,再加200ml蒸馏水,摇匀。
准确称取0.4~0.5g邻苯二甲酸氢钾三份,分别置于250ml锥形瓶中,加20~30ml蒸馏水溶解,再加1~2滴0.2%酚酞指示剂,用naoh标准溶液滴定至溶液呈微红色,半分钟不褪色即为终点。
二、h2c2o4含量测定
准确称取0.5g左右草酸试样,置于小烧杯中,加20ml蒸馏水溶解,然后定量地转入100ml容量瓶中,用蒸馏水稀释至刻度,摇匀。
用20ml移液管移取试样溶液于锥形瓶中,加酚酞指示剂1~2滴,用naoh标准溶液滴定至溶液呈微红色,半分钟不褪色即为终点。平行做三次。
实验数据记录与处理:
一、naoh标准溶液的标定
实验编号123备注
mkhc8h4o4 /g始读数
终读数
结 果
vnaoh /ml始读数
终读数
结 果
cnaoh /mol·l-1
naoh /mol·l-1
结果的相对平均偏差
二、h2c2o4含量测定
实验编号123备注
cnaoh /mol·l-1
m样 /g
v样 /ml20.0020.0020.00
vnaoh /ml始读数
终读数
结 果
ωh2c2o4
h2c2o4
结果的相对平均偏差
实验结果与讨论:
(1)(2)(3)……
结论:
例二 合成实验报告格式
实验题目:溴乙烷的合成
实验目的:1. 学习从醇制备溴乙烷的原理和方法
2. 巩固蒸馏的操作技术和学习分液漏斗的使用。
实验原理:
主要的副反应:
反应装置示意图:
(注:在此画上合成的装置图)
实验步骤及现象记录:
实 验 步 骤现 象 记 录
1. 加料:
将9.0ml水加入100ml圆底烧瓶, 在冷却和不断振荡下,慢慢地加入19.0ml浓硫酸。冷至室温后,再加入10ml95%乙醇,然后在搅拌下加入13.0g研细的溴化钠,再投入2-3粒沸石。
放热,烧瓶烫手。
2. 装配装置,反应:
装配好蒸馏装置。为防止产品挥发损失,在接受器中加入5ml 40%nahso3溶液,放在冰水浴中冷却,并使接受管(具小咀)的末端刚好浸没在接受器的水溶液中。用小火加热石棉网上的烧瓶,瓶中物质开始冒泡,控制火焰大小,使油状物质逐渐蒸馏出去,约30分钟后慢慢加大火焰,直到无油滴蒸出为止。
加热开始,瓶中出现白雾状hbr。稍后,瓶中白雾状hbr增多。瓶中原来不溶的固体逐渐溶解,因溴的生成,溶液呈橙黄色。
3. 产物粗分:
将接受器中的液体倒入分液漏斗中。静置分层后,将下层的粗制溴乙烷放入干燥的小锥形瓶中。将锥形瓶浸于冰水浴中冷却,逐滴往瓶中加入浓硫酸,同时振荡,直到溴乙烷变得澄清透明,而且瓶底有液层分出(约需4ml浓硫酸)。用干燥的分液漏斗仔细地分去下面的硫酸层,将溴乙烷层从分液漏斗的上口倒入30ml蒸馏瓶中。
接受器中液体为浑浊液。分离后的溴乙烷层为澄清液。
4. 溴乙烷的精制
配蒸馏装置,加2-3粒沸石,用水浴加热,蒸馏溴乙烷。收集37-40℃的馏分。收集产品的接受器要用冰水浴冷却。无色液体,样品+瓶重=30.3g,其中,瓶重20.5g,样品重9.8g。
5.计算产率。
理论产量:0.126×109=13.7g
产 率:9.8/13.7=71.5%
结果与讨论:
(1)溶液中的橙黄色可能为副产物中的溴引起。
(2)最后一步蒸馏溴乙烷时,温度偏高,致使溴乙烷逸失,产量因而偏低,以后实验应严格操作。
例三 性质实验报告格式
实验题目:
实验目的:
实验方法:
实验方法和步骤 现 象 解释和化学反应式
结论:
(1)(2)……
