QA检查标准
根据公司领导要求,结合本公司目前生产剂型和生产实际状况,特制定QA人员下车间检查工作标准如下:
一、按照生产计划,QA指派人员到生产车间进行质量监控、现场跟踪、产品抽查、抽检。QA人员工作重点是管理好车间人员(即操作工)和关键工段(配料、制粒、烘干、充填、压片、颗粒分装)的监管和检测,确保各关键工段产品质量检测指标达到中间产品内控标准。
二、去中药提取车间检查标准:查生产状态标志,看其内容是否齐全(生产品名、产品批号、生产日期、投料数量),批生产记录是否在操作岗位现场,记录是否及时、真实、完整地填写。
前处理工段:按生产指令进行领用经检验合格的物料,中药材挑选、清洗,浸泡、烘干或处理后,检查应无杂质、无异物、无不可药用部位,无本次生产处方中规定外药材。查药材是否按工艺规定切药,片:极薄片0.5mm以下,薄片1~2mm,厚片2~4mm,段:长10~15mm,块:8~12mm的方块。投料称量时,检查称量是否准确,计量器具是否有效、是否在有效期内,是否有人复核。
提取工段:在生产现场检查以下几点:
1.醇提-配制乙醇浓度是否正确,投放量是否准确。
2.水提-投放量是否按工艺规定量投放,投放量是否准确。
查煎煮次数、加多少倍量的水,检查生产与批准的工艺规定是否吻合。
生产品种煎煮工艺规定见下表:
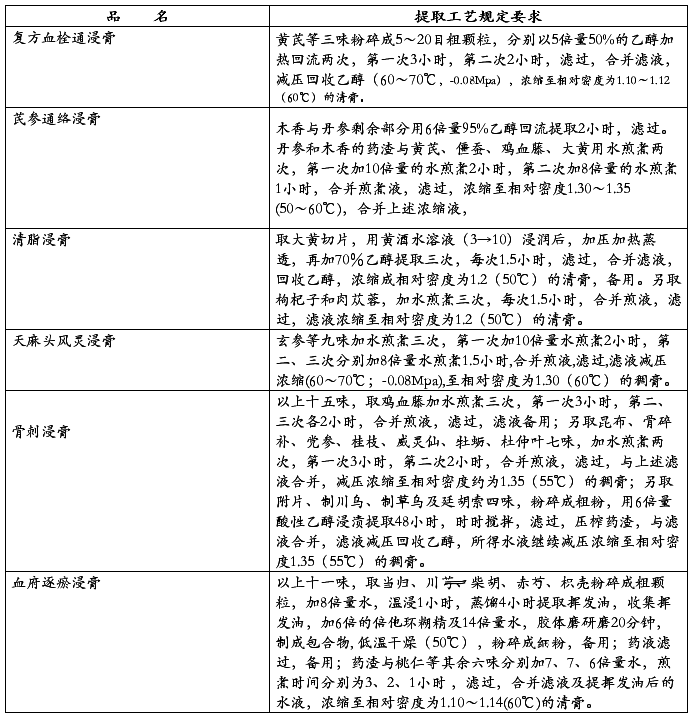
3.浓缩-减压浓缩一般温度60~70℃,真空度-0.08MPa。
4.乙醇回收-一般温度60℃,真空度-0.06至-0.08MPa。
5.收膏-例如复方血栓通,浓缩至相对密度为1.10~1.12(60℃)的清膏。(具体品种工艺规定的指标见下表)
本公司常年生产品种工艺规定如下:
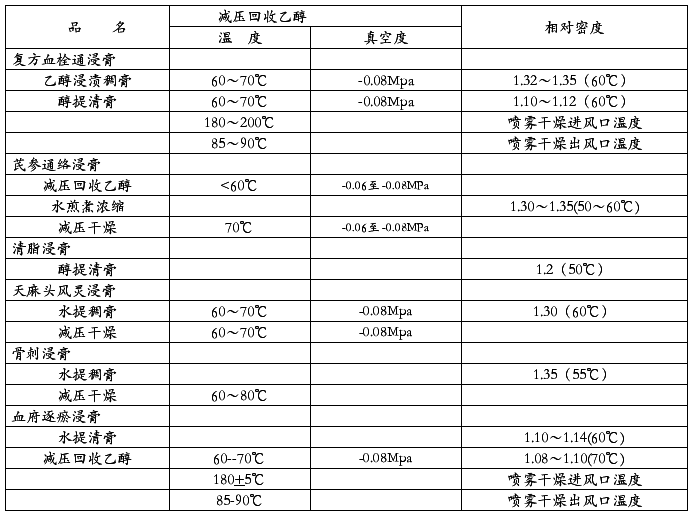
干燥制粒工段:本工段检查三个项目:鉴别、水分、含量测定。生产现场检查温度、压力、真空度、干燥时间,一步制粒检查进风口温度、出风口温度、干燥时间,粒度大小适宜。
胶囊剂颗粒如在沸腾制粒机内干燥,干燥时间应充分保证,最终确保中药胶囊剂中间产品水分控制在5.0%以内。血府逐瘀颗粒中间产品粒度控制在13.0%以内,水分控制在4.8%以内。
中药浸膏粉(中间产品)入库后,凭请检单,取样,由中心化验室检查:鉴别试验、水分检查、含量测定.并出具检验报告书。
三、去固体制剂车间检查标准:查生产状态标志,看其内容是否齐全(生产品名、产品批号、生产日期、投料数量),批生产记录是否在操作岗位现场,记录是否及时、真实、完整地填写。
胶囊充填工段:本工段检查三个项目:崩解时限、装量差异、水分。看其三个控制指标是否在中间产品规定的范围内。
1.崩解时限在充填刚开始,由QA人员取样送中心化验室检查,合格后开始正式充填。
崩解检验使用仪器为:崩解仪。仪器装置:将吊篮通过上端的不锈钢轴悬挂于金属支架上,浸入1000ml烧杯中,并调节吊篮位置使其下降时筛网距烧杯底部25mm,烧杯内盛有温度为37°C±1°C的水,调节水位高度使吊篮上升时筛网在水面下15mm处。
检查方法:取胶囊6粒,分别置上述吊篮的玻璃管中,加挡
板,启动崩解仪进行检查,崩解时限应符合规定。
2.装量差异检查:充填刚开始,胶囊充填工检查装量(胶囊毛重),检查频率2~3次,自检合格后,由 QA人员在生产现场,检查(胶囊毛重)1~2次,在车间检查合格后,取样送中心化验室检查(内容物净重),检验合格后,出具中间产品检验报告书。使用仪器为:电子分析天平。检查方法:抽取充填好胶囊(中药)10粒或(西药)20粒,分别精密称定重量,看其装量是否在规定的范围内。
3.待机器稳定后,装量差异在正常情况下,胶囊充填工每15分钟自检(胶囊毛重)一次,QA人员在生产现场中途要随机抽查(胶囊毛重)1~2次,必要时,再取样送中心化验室检查(内容物净重)2~3次。
4.在充填刚开始和快要结束时,QA人员在生产现场要加强抽查2~3次。以防止刚开始不稳定和快要结束时料少压力小造成装量偏移。
5.胶囊抛光前应剔除毛刺等次品,胶囊抛光时应缓慢地将胶囊放入抛光机内,保证抛光质量。
胶囊剂装量差异、崩解时限中间产品规定的范围见下表:
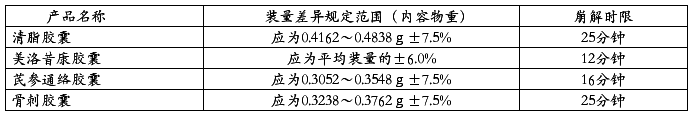
6.胶囊内容物水分,由中心化验室检查,水分控制在5%以内。
水分检验使用仪器为:电子分析天平(万分之一)、电热恒温干燥
箱、干燥器(内装硅胶)、扁形称量瓶。
检查方法:取供试品,混合均匀,取2~5g的重量,平铺于与供试品同样条件下干燥至恒重的扁形称量瓶中,精密称定,除另有规定外,照各品种项下规定的条件(105℃)干燥至恒重,由减失的重量和取样量计算供试品的水分。
压片工段:本工段检查三个项目:崩解时限、重量差异、外观。看其二个控制指标是否在中间产品规定的范围内,现场检查片子的外观,是否光洁,有无麻面、黑斑(点)等缺陷。
1.崩解时限检查:在压片刚开始,由QA人员取样送中心化验室检查,合格后开始正式压片。
2.重量差异检查:压片刚开始,压片工检查重量差异(素片),检查频率2~3次,自检合格后,由 QA人员在生产现场,检查(素片)1~2次,在车间检查合格后,取样送中心化验室检查(素片),检验合格后,出具中间产品检验报告书。使用仪器为:电子分析天平。检查方法:抽取压好的素片20片,分别精密称定重量,看其重量差异是否在规定的范围内。
3.待压片机稳定后,在正常情况下,压片工每15分钟自检(素片)一次,QA人员在生产现场中途要随机抽查(素片)1~2次,必要时,再取样送中心化验室检查(素片)2~3次。
片剂重量差异、崩解时限中间产品规定的范围见下表:

包薄膜衣工段:本工段检查三个项目:重量差异、崩解时限、外观。
看其二个控制指标是否在中间产品规定的范围内,现场检查片子的外观,是否光洁、色泽是否均匀、有无麻面、黑斑(点)等缺陷;检查各品种规定的包衣料颜色。
1.重量差异检查:包薄膜衣快要结束时,包衣工检查重量差异(薄膜衣片)2~3次,自检合格后,由 QA人员在生产现场,检查(薄膜衣片)1~2次,在车间检查合格后,取样送中心化验室检查(薄膜衣片)重量差异,检验后,出具中间产品检验报告书。合格后,用塑料袋装好,口扎紧,贴上标签(注明品名、编号、批号,净重),转入下道工序或存放中转站,备用。
检验使用仪器为:电子分析天平。检查方法:抽取薄膜衣片20片,分别精密称定重量,看其重量差异是否在规定的范围内。
2. 崩解时限检查:薄膜衣包完后,由QA人员取样,送中心化验室检查崩解时限,检验后,出具中间产品检验报告书。
检验使用仪器为:崩解仪。仪器装置:将吊篮通过上端的不锈钢轴悬挂于金属支架上,浸入1000ml烧杯中,并调节吊篮位置使其下降时筛网距烧杯底部25mm,烧杯内盛有温度为37°C±1°C的0.1mol/L盐酸溶液,调节液位高度使吊篮上升时筛网在水面下15mm处。
检查方法:取薄膜衣片6片,分别置上述吊篮的玻璃管中,加挡
板,启动崩解仪进行检查,崩解时限应符合规定。
片剂重量差异、崩解时限中间产品规定的范围见下表:

铝塑包装工段:检查铝塑板是否密封,产品批号、有效期是否正确,是否清晰,外观是否美观等。
密封检查法:一看铝塑板网纹是否压合清晰,二查铝箔与PVC压合是否牢固,用手用力搓二下,将铝箔与PVC不能撕开,证明压合密封,如能撕开说明密封不好,要查看、调节热封温度或调整机器。
要认真检查、校对产品批号、有效期,确保万无一失。
颗粒分装工段:本工段检查五个项目:粒度、溶化性、水分、装量差异、外观。
颗粒分装在分装前,由QA人员将待分装物料,取样送中心化验室检查:粒度、水分、溶化性。(检查粒度应在13%范围内、水分应在4.8%范围内,溶化性应在加热水70~80℃,200ml,搅拌5分钟,应全部溶化)。合格后开始颗粒分装。分装后操作工立即自检装量差异、外观,自查合格后,由 QA人员在生产现场检查装量差异、外观,符合规定要求后,取样,再送中心化验室检查装量差异。合格后,开机分装。操作工并不断(检查频率5~10分钟一次)自检装量差异、外观。QA人员在生产现场抽查2~3次。必要时,再取样送中心化验室检查装量差异。
1.装量差异检查方法:取供试品10袋,分别精密称定每袋内容物的重量,每袋装量与标示装量相比较,超出限度的不得多于2袋,并不得有1袋超出限度1倍。血府逐瘀颗粒,规格为:5g/袋,中间产品装量差异限度为±5%,合格范围应在4.75~5.25g。
检验使用仪器为:电子分析天平。
2.外观检查:A.血府逐瘀颗粒铝塑复合袋是否严密。检查方法:一看复合袋边缘网纹是否压合清晰,二查铝塑复合袋边缘压合是否牢固,用手用力搓几下,将复合袋边缘不能撕开,证明压合密封。
B. 检查产品批号、有效期是否正确,是否清晰,外观是否美观。
四、日常监管工作标准:
督促操作工进入洁净区,按规定两次更鞋、更衣、戴好工作帽、口罩,进行手清洗(查洗手池是否清洁)、手消毒(查75%酒精是否有),烘手机烘干后,方能进行生产操作。
生产过程中,各工段的门应随手关好,不得开着门进行操作,不得裸手接触药品。操作工要集中思想,按岗位操作规程操作,不随便讲话,不随便走动,不干违章的事情。加强中间产品的自检,在必要时,增加检测频率,对检测不符合内控标准的片子或胶囊或颗粒,要给予剔除,不得流入下道工序(查生产现场)。
生产前应充分做好准备工作,调整好机器、设备,进入洁净区后,尽量不要外出。如非要外出,重新进入时,按规定做好更鞋、更衣、手清洗、消毒等工作。上过卫生间的手或维修过机器的手,应及时清洗、消毒,以杜绝微生物的混入,影响卫生指标。杜绝污染源,确保产品微生物限度检查批批合格(查生产现场)。
领用合格的物料进行生产(查合格证),物料进入洁净区物流通道后,要进行脱包,外袋、大纸箱不得进入洁净区,脱包后的物料,应及时贴上标签,标明品名、批号、有效期、数量、生产厂家。(使用后应及时将袋口扎好、扎紧,并及时退库)。贴上标签后,方可进入生产区域(查现场、查标签)。用时要检查,看其包装是否破损、物料是否潮解,是否有异物混入,要校对品名、批号、数量、有效期、生产厂家等内容,称量要准确,不得出现差错,无误后再由另一人进行复核,品名、批号、重量、生产厂家等内容,数据及时记录在批生产记录上,两个人要亲笔签名(查批生产记录)。
生产结束后,认真做好清场工作,将本批次生产的物料全部清走,对机器、设备,地面、地漏、台面、墙面、用具、容器进行彻底清扫,擦洗、保养、润滑,不得留有残留物,清洁工作完毕后,及时挂好设备、容器清洁牌,并注明有效期,有效期一般不超过十天(查生产现场;查机器、设备、地面、地漏、台面、墙面、用具、容器;查清场记录)。
五、QA工作人员自身管理要求:
QA工作人员要严要求自己,处处以GMP标准衡量自己,各种工艺纪律首先要带头执行好,在员工面前做好表率,事事以预防为主,把质量隐患和苗头消灭在荫芽状态。平时加强业务学习,掌握法定标准,熟悉产品工艺规程,过细地工作,踏实地工作,加强巡检、抽检,认真做好每次的检查记录,对质量有波动的中间产品或边缘产品,要及时汇报、沟通,要扩大抽样量,提供有价值的检验数据,釆取纠正性的措施,最终确保产品合格,杜绝把错误!链接无效。有波动的中间产品或边缘产品,流入下道工序。 20##年9月22日
第二篇:品质QA检验标准
深圳市亮典电子有限公司
手机检验标准及范围
1、 目的:
在检验手机系列半成品时程序规范化、检验所有依据。
2、适用范围:
所有生产的手机半成品。
3、检验条件:
(1).在正常环境下(25正负3度),与被测物呈45角度。
(2)照明环境:40W日光灯,光源距离检查目标1M远,偏离光源中心方向±15度内 (或同等亮度条件);
(3)目视检验距离:30cm远;时间:观察整个检测面5秒钟为准。
(4)目视检验方向:任意方向
(5)视力:0.8~1.2以上(含矫正视力);
(6)检查方法:a.目视检查,b.卡尺测量,c.标准点线卡比较,d.与标准样品对比。
4、抽样标准:MIL-STD 105E SINGLE NORMAL LEVEL Ⅱ
严重缺陷(CRI):AQL=O
重缺陷(MAJ):AQL=O.4
轻缺陷(MIN):AQL=1.0
5、缺陷等级:
(1)严重缺陷(Critical Defect):产品存在对使用者的人身及财产安全构成威胁的缺陷。
(2)重缺陷(Major Defect):产品存在下列缺陷,为主要缺陷。
(3)功能缺陷影响正常使用;
(4)性能参数超出规格标准;
(5)漏元件、配件或主要标识,多出无关标识及其他可能影响产品性能的物品;导致最终客户拒绝购买的结构及外观缺陷。
6、次要缺陷(Minor Defect):不影响产品使用,最终客户有可能愿意让步接受的缺陷.有些外观检查中发现的问题会影响到产品的功能,则按照功能缺陷的标准来确定
限等级;如按键脱落会导致按键无功能,为主要缺陷。有些功能检查中发现的问题影响到产品观感,泽按照外观缺陷的标准来确定缺陷等级;如按键漏光。

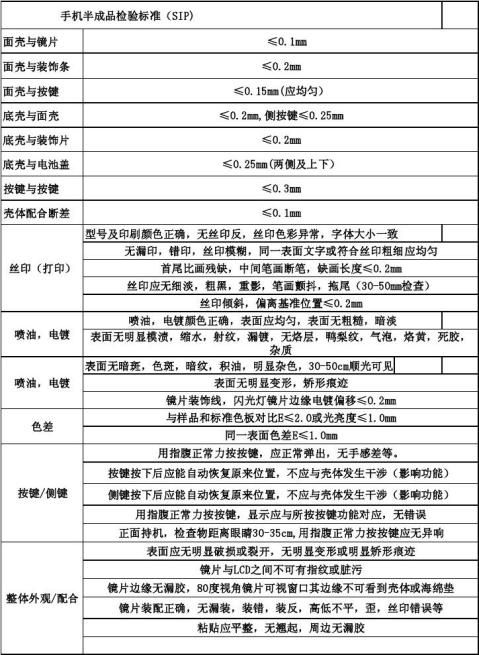
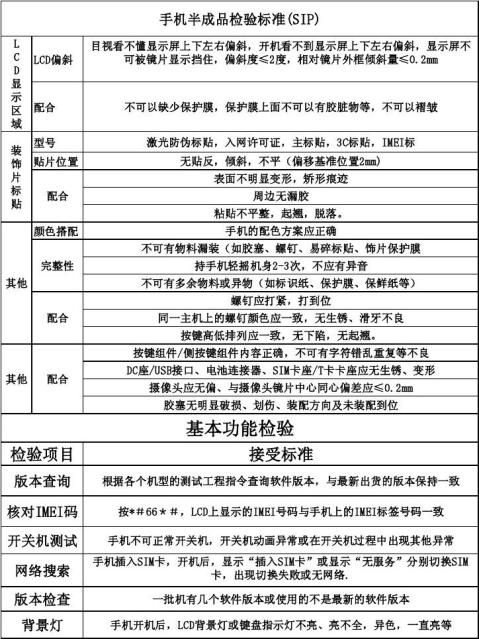
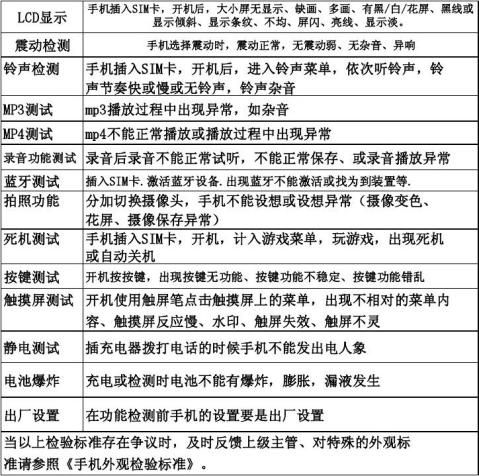
手机半成品检验标准