验证某未知混合试液含有Fe3+、Cu2+、Ni2+、Pb2+离子并测量各离子含量
一、实验目的
通过用配位滴定方法定性与定量分析混合溶液中各金属离子的浓度;熟悉配位滴定的原理和操作,以及各金属离子的性质和配位滴定中需要注意的问题(包括PH的控制以及副反应,掩蔽剂的选择,直接滴定法和返滴定法以及置换滴定的条件)。
二、目前有关本次实验中所测元素常量测定方法的概述
1.络合滴定法
实验室常用的方法之一,采用有机络合剂与所需要检验的金属离子发生络合反应,生成稳定的络合物或络合离子,借用合适的指示剂指示反应的终止。而常采用的络合剂是EDTA溶液,在使用EDTA之前要利用Zn2+ 标准溶液进行标定再使用。通过EDTA滴定消耗的体积量,间接求得所求金属离子含量。
2.ICP-AES法测量重金属,即电感耦合等离子体原子发射光谱法
目前,金属元素测定方法主要有原子吸收分光光度法和电感耦合等离子体原子发射光谱法(ICP-AES)。原子吸收分光光度法虽是一种成熟方法,但测定速度较慢、干扰物质复杂。电感耦合等离子体原子发射光谱法是以电感耦合等离子矩为激发光源的一类光谱分析方法。
其原理为等离子体发射光谱法可以同时测定样品中多元素的含量。当氩气通过等离子体火炬时,经射频发生器所产生的交变电磁场使其电离、加速并与其他氩原子碰撞。这种链锁反应使更多的氩原子电离,形成原子、离子、电子的粒子混合气体,即等离子体。等离子体火炬可达6000~8000K的高温。过滤或消解处理过的样品经进样器中的雾化器被雾化并由氩载气带入等离子体火炬中,气化的样品分子在等离子体火炬的高温下被原子化、电离、激发。不同元素的原子在激发或电离时刻发射出特征光谱,所以等离子体发射光谱可用来定性样品中存在的元素。特征光谱的强弱与样品中原子浓度有关,与标溶液进行比较,即可定量测定样品中各元素的含量。
3.原子吸收分光度法
原子吸收分光光度法的测量对象是呈原子状态的金属元素和部分非金属元素,是由待测元素灯发出的特征谱线通过供试品经原子化产生的原子蒸气时,被蒸气中待测元素的基态原子所吸收,通过测定辐射光强度减弱的程度,求出供试品中待测元素的含量。
原子吸收一般遵循分光光度法的吸收定律,通常借比较对照品溶液和供试品溶液的吸光度,求得供试品中待测元素的含量。本方法适用于地表水和污水中Al、As、Ba、Be、Ca、Cd、Co、Cr、Cu、Fe、K、Mn、Na、Ni、Pb、Sr、Ti、V和Zn等20种元素总量的测定。(1)溶解态元素:未经酸化的样品中,能通过0.45um滤膜的元素成分。(2)元素总量:未经过滤的样品,经消解后测得的元素浓度。即样品中溶解态和悬浮态两部分元素浓度的总和。
三、实验原理
1 定性分析
采用K4[Fe(CN)6],鉴定Fe3+。
利用HCl沉淀Pb2+,根据PbCl2易溶于热水,在弱酸介质中,Pb2+与CrO42-反应生成黄色PbCrO4沉定来鉴定Pb2+,必要时加入NaOH溶液,将沉淀溶解,以确证Pb2+的存在。
利用NH3·H2O将Fe3+、Pb2+与Cu2+、Ni2+分离为:Fe(OH)3、Pb(OH)2 和Cu(NH3)42+、Ni(NH3)42+。滤液在弱酸(HAc)介质中,K4[Fe(CN)6]溶液与Cu2+生成红棕色沉淀鉴定Cu2+;在氨性介质中,Ni2+与丁二酮肟生成鲜红色丁二肟镍沉淀鉴定Ni2+。
2 定量分析
根据Fe3+与Pb2+、Cu2+和Ni2+的稳定常数的差别( ),采用控制酸度的方法,测定Fe3+。选用磺基水杨酸作为指示剂,指示终点为溶液由紫红色变成黄绿色。
),采用控制酸度的方法,测定Fe3+。选用磺基水杨酸作为指示剂,指示终点为溶液由紫红色变成黄绿色。
利用NH3·H2O将Fe3+、Pb2+与Cu2+、Ni2+分离为:Fe(OH)3、Pb(OH)2 和Cu(NH3)42+、Ni(NH3)42+。过滤后的Cu(NH3)42+、Ni(NH3)42+滤液用酸中和,Na2S2O3掩蔽Cu2+,采用返滴定法测定Ni2+,以二甲酚橙为指示剂,亮黄色变成酒红色为终点,再利用返滴定法测定Cu2+、Ni2+总量,其中铜的指示剂采用二甲酚橙,终点为溶液由红色变为黄绿色。滴定终点后,采用差减法,确定Cu2+的含量。
利用返滴定法测定Fe3+、Ni2+、Cu2+、Pb2+总量,采用差减法,确定 Pb2+ 的含量。
分步滴定判断所需数据
logKFe(III)Y=25.10,logKCuY=18.80,logKNiY=18.62,logKPbY=18.04。
Ksp[Fe(OH)3] =4.0×10-38,Ksp[Cu(OH)2] =2.2×10-20;
Ksp[Ni(OH)2] =2.0×10-15,Ksp[Pb(OH)2] =1.2×10-15。
四、试剂、材料和仪器
药品
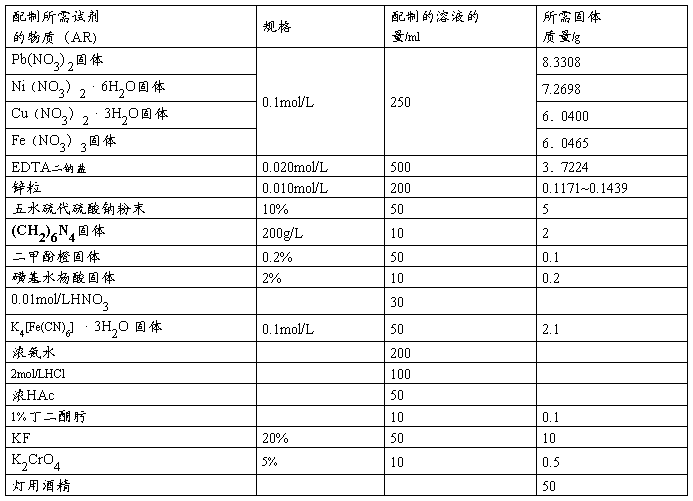
溶液的配制
0.01 mol·L-1Zn2+标准溶液的配制
用干净的小烧杯(或称量纸)准确称取0.1171~0.1439g配制200 mL 0.01mol·L-1 的锌溶液所需的纯锌粒于150 mL烧杯中,加入5 mL 6 mol·L-1的HCl 溶液,立即盖上表面皿,微热,待锌完全溶解后,以少量水冲洗表面皿和烧杯内壁,冷却后,定量转移至200.00 mL的容量瓶中,以水稀释至刻度,摇匀。计算其准确浓度。
0.01mol·L-1 EDTA标准溶液的配制及标定
用洁净的1000 mL容量瓶称取配制1000 mL 0.01 mol·L-1 EDTA溶液所需的EDTA二钠盐(Na2H2Y·2H2O)固体3.8g,在烧杯中加水、温热溶解、冷却后转移入试剂瓶中,摇匀。
吸取20.00 mL 0.01 mol·L-1 的Zn2+ 标准溶液于锥形瓶中。加入 2滴二甲酚橙指示剂,滴加200g/L六亚甲基四胺溶液至溶液呈现稳定的紫红色,再过量5 mL。用0.01 mol·L-1 EDTA溶液滴定至溶液由紫红色变为亮黄色即为终点。平行标定三份,计算EDTA溶液的准确浓度。数据记录和结果表达如表1所示。
约0.01mol·L-1 未知混合溶液的配制
称取配制各离子浓度约0.01mol·L-1 的固体于100ml小烧杯当中,用20ml去离子水溶解,转移至250.00ml的容量瓶中,洗涤烧杯,玻棒3~4次,将洗液移至容量瓶中,定容,摇匀。备用。
200g/L的六亚甲基四胺溶液的配制
称取所需的六亚甲基四胺固体,溶于小烧杯中,加入少量水溶解后,移至50.00ml容量瓶中,洗涤,移液,3~4次,最后,定容,摇匀,备用。
10%Na2S2O3 ,%的磺基水杨酸,0.2%的二甲酚橙溶液等配制操作如上。
除实验柜中以外仍需的仪器
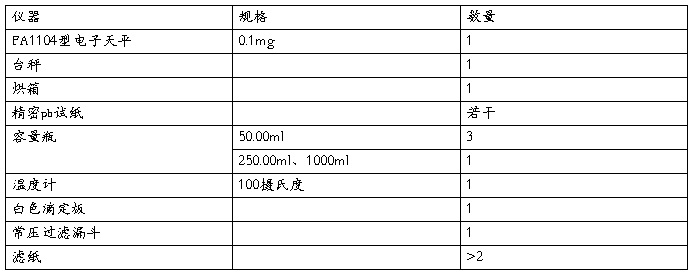
五、实验内容和步骤
混合溶液中各离子的测定
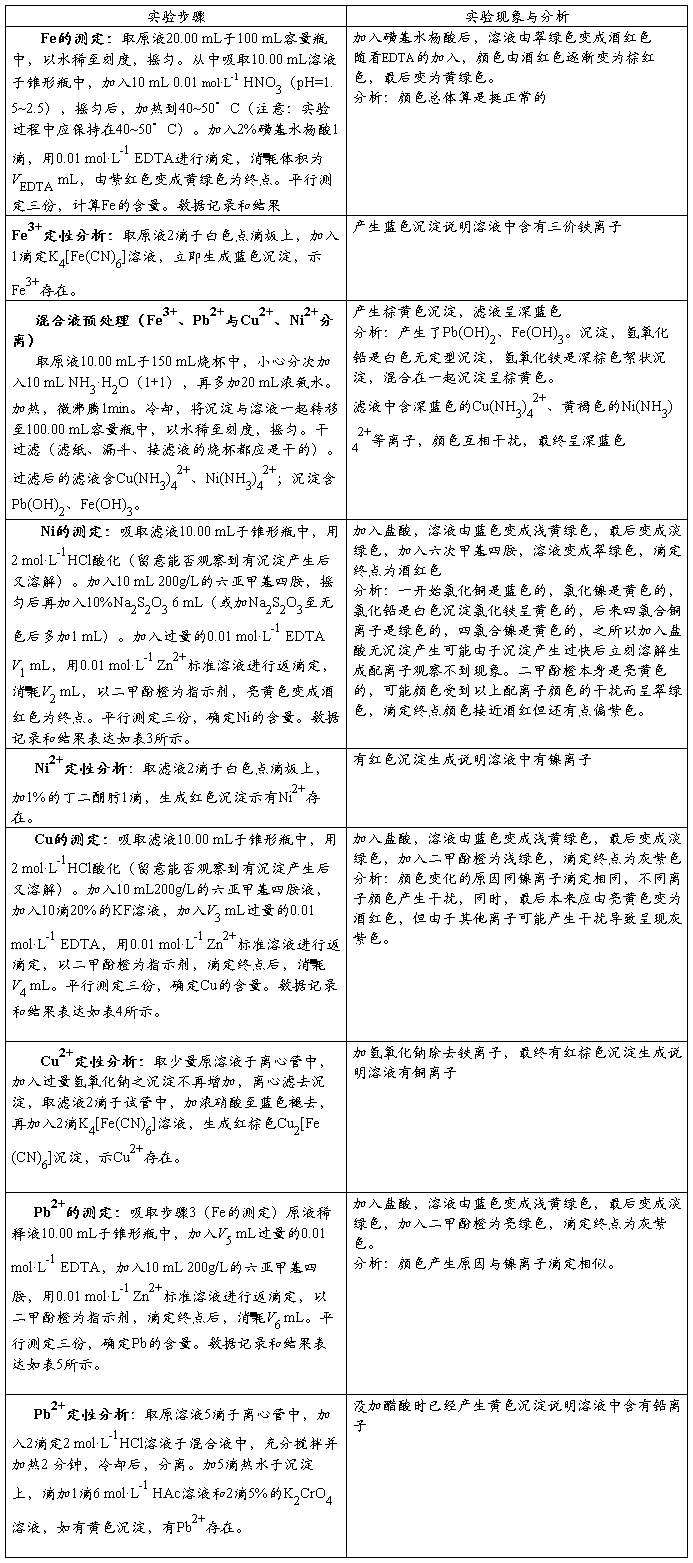
六、实验数据与结果
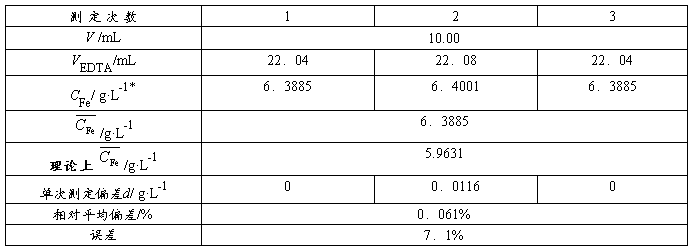
表1 0.01mol·L-1 EDTA溶液的标定
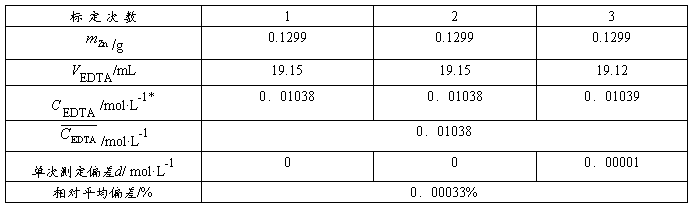
* mol·L-1
mol·L-1
表2 Fe含量的测定
*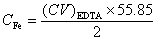 g·L-1,
g·L-1,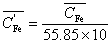 mol·L-1
mol·L-1
表3 Ni含量的测定
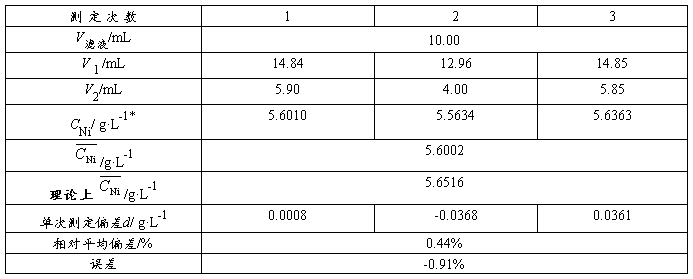
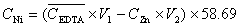 g·L-1,
g·L-1, mol·L-1
mol·L-1
表4 Cu含量的测定
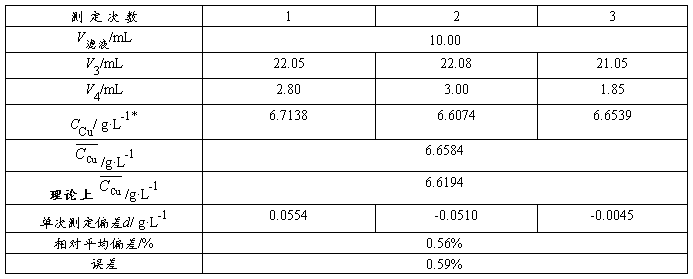
 g·L-1,
g·L-1, mol·L-1
mol·L-1
表5 Pb含量的测定
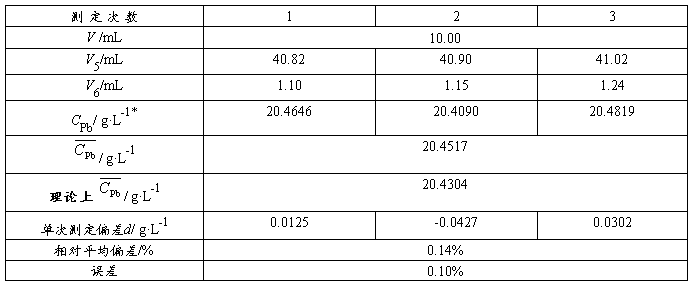
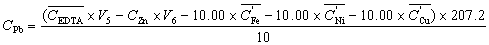 g·L-1
g·L-1
七、结果与讨论
通过处理比较滴定的数据,发现在铁含量的滴定与实验理论结果有较大偏差。可能原因:
1、铁与EDTA在PH=2时并不是严格按1:1反应,可能是1:2甚至是1:3反应。为了验证假设,配了含铁的纯溶液,在采用相同处理条件的情况下,用EDTA滴定时消耗的体积与铁几乎1:1.也就是说在PH=2的情况下,铁与EDTA也应是1:1.
2、在PH=2的情况下,混合样液中的其他离子会影响铁与EDTA的反应,即在滴定铁的同时可能会有部分其他离子被同时滴定。但是在查看林邦曲线时发现,lgKFe(III)Y=25.10,lgKCuY=18.80,lgKNiY=18.62,lgKPbY=18.04。?lgK(Fe-Cu)=6.30,只是略大于6.虽然?lgK≥6是在允许滴定终点误差为0.1%时准确滴定的条件。所以,应该配制3种分别含有铁和铜,铁和镍,铁和铅混合溶液,进行EDTA的滴定,验证是否其他离子会影响滴定结果的猜想。
3、可能原样在存放过程中可能因为是由于原液储存在玻璃瓶中置换出部分Al和Ca,从未影响了在后来滴定以及铁含量的测定。
.对于镍的定性检测,在加入丁二酮肟后,溶液并不是生成理论上丁二酮肟与镍的桃红色沉淀,而是红棕色的浑浊溶液。原因可能是丁二酮肟还会与Pb 生成沉淀,还可以跟Cu2+ 、Fe3+ 生成水溶性的络合物。这也可以解释为什么定性分析中出现的是红棕色的浑浊溶液而不是鲜红色的沉淀。
八、参考文献
[1] 第一届广东省大学生化学实验竞赛_实验操作试题
[2]华南师范大学,华中师范大学.分析化学.高等教育出版社.2011,4,第四版
[3]汤又文,分析化学实验,化学工业出版社,2008,2
[4]《 Pb2、Co2、CU2、Ni2混合液中Pb2的分离和测定》,新疆医科大学学,20##年,12,,24
[5]南京同普分析仪器制造有限公司,《铜合金中铜锌铅铁镍锰元素测定法》,2012,10,09
第二篇:实验报告9 典型相关分析
实验九 典型相关分析
实验目的和要求
能利用原始数据与相关矩阵、协主差矩阵作相关分析,能根据SAS输出结果选出满足要求的几个典型变量.
实验要求:编写程序,结果分析.
实验内容:4.9
方法一:SAS
data examp4_9;
input x1-x2 y1-y2;
cards;
191 155 179 145
195 149 201 152
181 148 185 149
183 153 188 149
176 144 171 142
208 157 192 152
189 150 190 149
197 159 189 152
188 152 197 159
192 150 187 151
179 158 186 148
183 147 174 147
174 150 185 152
190 159 195 157
188 151 187 158
163 137 161 130
195 155 183 158
186 153 173 148
181 145 182 146
175 140 165 137
192 154 185 152
174 143 178 147
176 139 176 143
197 167 200 158
190163187150;
run;
proccancorr data=examp4_9 corr;
var x1-x2;
with y1-y2;
run;
The SAS System 16:48 Sunday, October 31, 2012 1
The CANCORR Procedure
Correlations Among the Original Variables
Correlations Among the VAR Variables(变量x1-x2的相关系数矩阵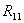 )
)
x1 x2
x1 1.0000 0.7504
x2 0.7504 1.0000
Correlations Among the WITH Variables(变量y1-y2的相关系数矩阵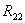 )
)
y1 y2
y1 1.0000 0.8397
y2 0.8397 1.0000
Correlations Between the VAR Variables and the WITH Variables
变量x1-x3与y1-y3的相关系数矩阵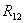
y1 y2
x1 0.7092 0.7050
x2 0.7140 0.7440
The SAS System 16:48 Sunday, October 31, 2012 2
The CANCORR Procedure
Canonical Correlation Analysis
Adjusted Approximate Squared
Canonical Canonical Standard Canonical
Correlation Correlation Error Correlation
1 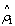 0.801420 0.788167 0.074591
0.801420 0.788167 0.074591 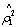 0.642274
0.642274
2 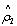 0.084522 . 0.207025
0.084522 . 0.207025 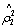 0.007144
0.007144
Test of H0: The canonical correlations in the
Eigenvalues of Inv(E)*H current row and all that follow are zero
= CanRsq/(1-CanRsq)
Likelihood Approximate
Eigenvalue Difference Proportion Cumulative Ratio F Value Num DF Den DF Pr > F
1 1.7954 1.7882 0.9960 0.9960 0.35517013 6.78 4 40 0.0003
2 0.0072 0.0040 1.0000 0.99285597 0.15 1 21 0.7014
检验假设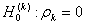
检验统计量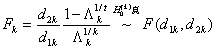 ,
, 为第一、第二自由度.由检验结果可知,
为第一、第二自由度.由检验结果可知, ,.故只有第一对典型变量显著相关.取第一对进行分析即可.
,.故只有第一对典型变量显著相关.取第一对进行分析即可.
Multivariate Statistics and F Approximations
S=2 M=-0.5 N=9
Statistic Value F Value Num DF Den DF Pr > F
Wilks' Lambda 0.35517013 6.78 4 40 0.0003
Pillai's Trace 0.64941830 5.05 4 42 0.0021
Hotelling-Lawley Trace 1.80263313 8.88 4 23 0.0002
Roy's Greatest Root 1.79543769 18.85 2 21 <.0001
NOTE: F Statistic for Roy's Greatest Root is an upper bound.
NOTE: F Statistic for Wilks' Lambda is exact.
The SAS System 16:48 Sunday, October 31, 2012 3
The CANCORR Procedure
Canonical Correlation Analysis
Raw Canonical Coefficients for the VAR Variables
V1 V2
x1 0.0474933802 -0.144760311
x2 0.0840477791 0.1959848929
Raw Canonical Coefficients for the WITH Variables
W1 W2
y1 0.0448783575 -0.174269545
y2 0.0850389917 0.2549589923
数据未标准化结果,即利用协方差矩阵分析的结果
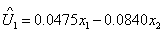
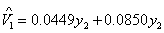
The SAS System 16:48 Sunday, October 31, 2012 4
The CANCORR Procedure
Canonical Correlation Analysis
Standardized Canonical Coefficients for the VAR Variables
V1 V2
x1 0.4716 -1.4375
x2 0.5963 1.3904
Standardized Canonical Coefficients for the WITH Variables
W1 W2
y1 0.4593 -1.7835
y2 0.5827 1.7471
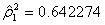 ,
,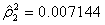 .
.
第一对典型变量
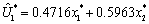
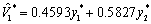
The SAS System 16:48 Sunday, October 31, 2012 5
The CANCORR Procedure
Canonical Structure
Correlations Between the VAR Variables and Their Canonical Variables
V1 V2
x1 0.9191 -0.3941
x2 0.9502 0.3117
Correlations Between the WITH Variables and Their Canonical Variables
W1 W2
y1 0.9486 -0.3164
y2 0.9684 0.2494
Correlations Between the VAR Variables and the Canonical Variables of the WITH Variables
W1 W2
x1 0.7365 -0.0333
x2 0.7615 0.0263
Correlations Between the WITH Variables and the Canonical Variables of the VAR Variables
V1 V2
y1 0.7602 -0.0267
y2 0.7761 0.0211
原变量和第一对变量相关程度高,后一组提取的信息很少,与典型对系数一致。
方法二:MATLAB
>> a=[data];
[n,m]=size(a);
b=a./(ones(n,1)*std(a));
R=cov(b);
X=b(:,1:2);
Y=b(:,3:4);
[A,B,r,U,V,ststs]=canoncorr(X,Y)
A =
0.5522 -1.3664
0.5215 1.3784
B =
0.5044 -1.7686
0.5383 1.7586
r =
0.7885 0.0537
U =
0.5731 -0.0137
0.3750 -1.6953
-0.4877 0.0774
-0.0209 0.7322
-1.0535 0.0294
1.6762 -2.0193
0.1063 -0.6685
1.1955 -0.1057
0.1912 -0.1546
0.2760 -1.0884
0.1065 2.2268
-0.4453 -0.3895
-0.7422 1.4311
0.7995 0.8741
0.1205 -0.3416
-2.2840 0.5404
0.7994 -0.5736
0.1488 0.3123
-0.6999 -0.4835
-1.3930 -0.5784
0.5590 -0.3406
-1.2373 0.1224
-1.4072 -0.9053
1.7614 1.3899
1.0825 1.6219
V =
-0.5833 -0.2587
1.0836 -2.2993
0.0390 -0.2672
0.1898 -0.7957
-1.2259 0.3643
0.6314 -0.7140
0.2902 -1.1480
0.4807 -0.1856
1.4442 0.2398
0.3000 -0.0954
0.0090 -0.7055
-0.6741 1.1462
0.2797 0.5190
1.1832 0.0680
0.8615 1.7392
-2.6910 -1.0193
0.6605 2.4438
-0.6441 1.5845
-0.3524 -0.5250
-1.9285 0.1107
0.2797 0.5190
-0.4731 0.4416
-0.8945 -0.2544
1.5147 -0.5507
0.2197 -0.3574
ststs =
Wilks: [0.3772 0.9971]
df1: [4 1]
df2: [42 22]
F: [6.5972 0.0637]
pF: [3.2565e-004 0.8031]
chisq: [20.9642 0.0639]
pChisq: [3.2189e-004 0.8004]
dfe: [4 1]
p: [3.2189e-004 0.8004]
