医疗器械临床使用安全事件监测管理制度
为加强医院医疗器械不良反应监测管理工作,依据国家《医疗器械监督管理 条例》、《医疗器械不良反应事件监测和再评价管理办法(试行)》结合我院印发《九师医院医疗安全(不良)事件报告制度》制定本制度。
一、 建立健全组织机构,明确岗位职责
(一)、成立医疗器械不良反应监测管理小组 ,协助医院医疗安全(不良)事件报告领导小组负责全院医疗器械不良事件监测管理相关工作,规范医院医疗器械不良事件的管理与监控工作。
组长:石坚 职务:设备科长
联络员成员:封帅 设备科维修员
管理小组在医院医疗安全(不良)事件报告领导小组领导下履行职责:
(1) 负责医院医疗器械不良事件监测管理工作的规划和相关制度的制定、 修改、监督和落实:
(2) 负责医院医疗器械不良事件监测管理的宣教工作及培训,
(3) 研究分析医疗器械不良事件监测管理工作的动态和存在的问题,负责定期组织召开日常监测工作总结会议,传达及记录会议内容,讨论并提出改进意见和建议。
(4) 制定和完善高风险医疗器械使用的操作规程,组织培训员工在使用高风险医疗器械时规范操作。
(5) 制定突发、群发的医疗器械不良反应事件,尤其导致死亡或者严重伤害不良事件的应急预案。
(6) 对于上报的不良事件,于一周内协同领导小组组织讨论,制定应对措施。
(7) 通报传达上级医疗器械不良反应检测技术机构的反馈信息。
(二)、明晰职能部门分工
(1)、设备科负责医疗器械不良事件的日常监测工作。负责临床科室对上报的医疗器械不良事件的日常监测信息的汇总分析及评价工作。
(2)、设备科定期总结。每年1月5日前将上一年度的医疗器械不良事件监测工作的总结报告提交给九师医院医疗安全(不良)事件报告。并保存监测的原始资料备查。
(3)、相关科室设立医疗器械不良事件兼职联络员,了解本科室医疗器械使用情况,指导临床使用科室完成填写《医疗器械不良事件报告单》。按规定时间内上报。并在医院医疗安全(不良)事件报告领导小组的领导下开展工作。
二、建立医疗器械使用不良事件报告制度
1、临床使用科室发现或可疑发生医疗器械不良事件,立即填写《可疑医疗器械不良事件报告表》,报设备科。
2、设备科经调查核实后,将上报表转达医疗安全(不良)事件报告领导小组,经过分析、评价后,由设备科上报医疗器械不良事件监测部门。
3、设备科在科室上报发生医疗器械不良事件后,对导致死亡的事件于发现或者知悉之日起5个工作日内,导致严重伤害、可能导致严重伤害或死亡的事件于15个工作日内向上级医疗器械不良事件监测技术机构报告,对突发、群发的医疗器械不良事件,立即向上级医疗器械不良事件监测技术机构报告,并在24小时内报送《可疑医疗器械不良事件报告表》
4、设备科联系告知相关生产企业。保存医疗器械不良事件监测记录,对于引起不良事件的医疗器械的监测记录保存至医疗器械上标明的使用期限后2年,并且记录保存期不少于5年。
三、制定医院医疗器械(疑是)不良事件报告流程
医院医疗器械不良事件报告流程




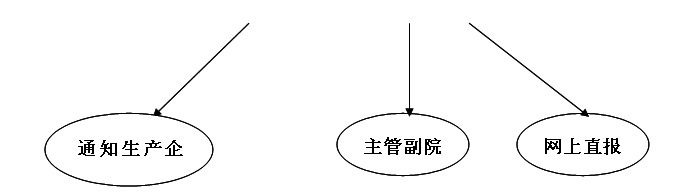
附件:使用科室《可疑医疗器械不良事件报告表》
附件1:
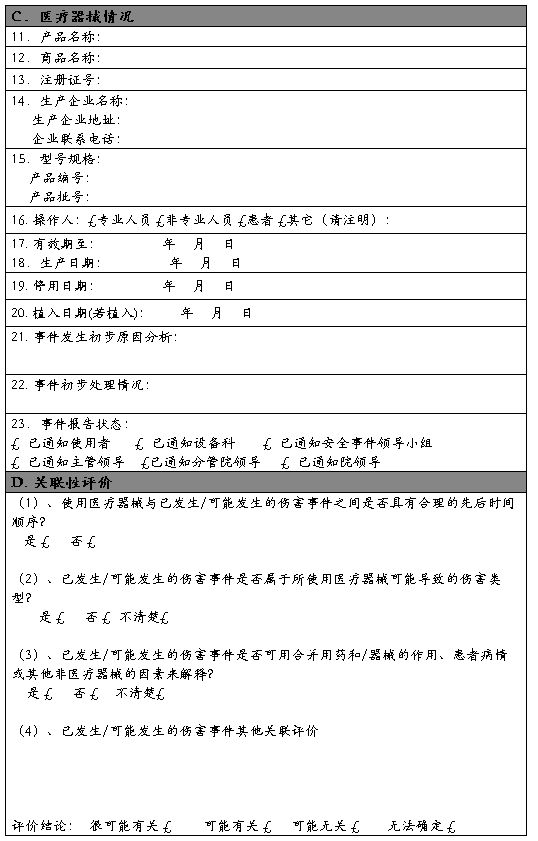
可疑医疗器械不良事件报告表
报告日期: 年 月 日 编 码:
报告来源:第九师医院 科室名称:
报告人签名:

第二篇:医疗器械不良事件监测管理制度(11)
医疗器械不良事件监测管理制度
为加强医疗器械不良事件监测管理工作,依据国家《医疗器械监督管理条例》、
《医疗医械不良事件监测和再评价管理办法(试行)》制定本制度。
一、建立健全组织结构,明确岗位职责
1、成立医疗器械不良事件监测领导小组
组长:
成员:
日常工作及会议召集、会议记录由质量保证部负责。
领导小组全面负责医疗器械不良事件监测管理相关工作,并履行以下主要职责:(1)负责医疗器械不良事件监测管理工作的规划和相关制度的制定、修改、监督和落实;(2)负责医疗器械不良事件监测管理的宣教工作;(3)研究分析医疗器械不良事件监测管理工作的动态和存在问题,定期组织召开日常监测工作总结会议,讨论并提出改进意见和建议;(4)制定与完善高风险医疗器械使用的操作规程,组织培训员工在使用高风险
医疗器械时规范操作;(5)制定突发、群发的医疗器械不良事件,尤其导致死亡或者严重伤害不良事
件的应急预案;(6)对于上报的不良事件,于一周内组织讨论,制定应对措施;(7)通报传达上级医疗器械不良事件监测技术机构的反馈
信息。
2、明晰职能部门分工
日常监测
采购员和验收员共同负责医疗器械不良事件的日常监测工作。 定期总结:每年1月5
日前将上一年度的医疗器械不良事件监测工作的总结报
告提交给质量保证部。并保存监测的原始资料备查。
监督管理:质量验收员通过每季度对后勤服务质量评价来监督采购员对医疗器
械不良事件监测实施情况。
二、建立医疗器械使用不良事件报告制
1、发现或可疑发生医疗器械不良事件,立即填写《可疑医疗器械不良事件报告
表》一式三份,报药监局
2、质量验收员保存医疗器械不良事件监测记录,对于引起不良事件的医疗器械
的监测记录保存至医疗器械上标明的使用期限后2年,
并且记录保存期不少于5年
三、建立医疗器械产品使用追溯制度
1、对于植入性医疗器械实施追溯跟踪管理。
2、植入性医疗器械要及时登记备案,严格执行国家有关规定。植入性医疗器械
包括骨科内固定植入器材、人工关节、人工晶体、人工乳房、植入式心脏起搏
器、人工心脏瓣膜、血管或腔道内导管支架,以及其它金属或高分子植入器材
等。
3、对产品的追溯登记信息主要涵盖生产企业名称、生产地、产品规格型号、
有效期、批号、医疗器械注册证编号、产品质量保证书等。
4、质量验收员定期监督检查登记情况。
