福州大学实验报告
课程名称: 化学制药实验
实验类型:_____ 综合型________
实验项目名称: 苯妥英钠的合成
学生姓名:_____ 王越________
年级专业: 2008级制药工程
学 号:____ S040803123 ___ _
同组学生姓名: 童林足 苏晓珊 严炜 许春萍
指导老师: 唐凤翔 薛蓬春
实验地点: 化学化工学院实验南楼210
实验日期: 2011年6月13日~6月15日
化学化工学院
实验五 苯妥英钠(PHenytoin Sodium)的合成
一、 实验目的
1、学习安息香缩合反应的原理和应用维生素B1为催化剂进行反应的机理和实验方法。
2、了解稀硝酸作为氧化剂的实验方法。
二、 实验原理
苯妥英钠为抗癫痫药,适于治疗癫痫大发作,也可用于三叉神经痛,及某些类型的心律不齐。苯妥英钠化学名为5,5-二苯基乙内酰脲,化学结构式为:
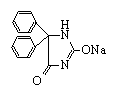
苯妥英钠为白色粉末,无臭、味苦。微有吸湿性,易溶于水,能溶于乙醇,几乎不溶于乙醚和氯仿。
合成路线如下:
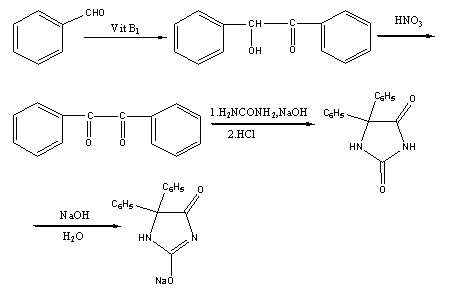
三、 实验材料与设备
表1 所用的玻璃仪器及规格
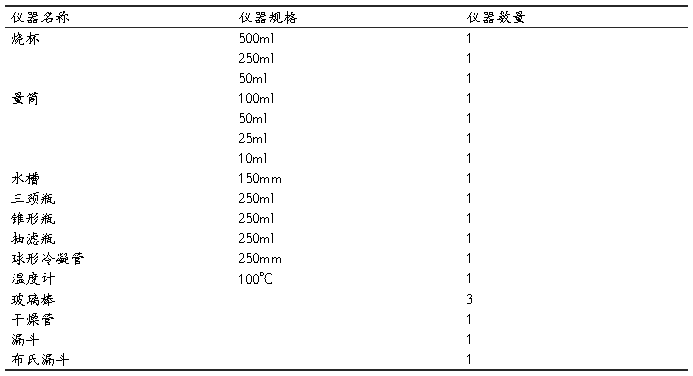
表2 所用的试剂及规格

表3 所用的设备型号及规格

四、 实验操作步骤
(一)安息香的制备
1、于250ml锥形瓶内加入VB1 6.0g(白色结晶性粉末。有微弱特臭、味苦,有潮解性。熔点248℃,易溶于水,微溶于乙醇,不溶于醚和苯中,相对分子量300.81,计算可知加入的VB1为19.946mmol)、蒸馏水30 mL、无水乙醇60 mL(水和无水乙醇提前冰水冷却)。不时摇动,待VB1溶解;
2、加入2mol/L的(冰浴冷透)NaOH 22.5 mL(VB1在碱性条件下会分解,所以NaOH溶液在反应前必须用冰水充分冷却),充分摇动;
3、快速加入新蒸馏的苯甲醛(因为蒸馏的过程耗时太长,我们直接用瓶装的苯甲醛代替)22.5 mL(无色液体,具有类似苦杏仁的香味,熔点为-26℃。 沸点为178℃,相对密度为1.0415(10/4℃),能与乙醇、乙醚、氯仿等混溶,微溶于水,能进行水蒸气蒸馏,相对分子质量为106.12,计算可知加入的苯甲醛为220.8mmol),置于装有适量冰水的水槽中,冰水浴下搅拌40min,放置两天;
4、两天后瓶中析出大量淡黄色针状晶体,抽滤,用100ml冰水分多次洗涤,得安息香粗品。
5、粗品用95% 的乙醇溶液精制,晶体转移至500ml烧杯中,水浴70℃下少量多次加入95%乙醇,搅拌至固体恰好全部溶解(用去乙醇溶液410ml),室温冷却,晶体重新析出,抽滤,用少量冰水洗涤,置于真空干燥箱中干燥,得到乳白色安息香晶体。烘干称重(因为第一次A抽滤得到的滤液又析出很多晶体,故进行第二次抽滤B,两次得到的晶体质量分别为 A:14.013g、B:1.119g),测熔点(两次测得的熔点分别为A:138~140℃,B:135~137℃,二者的熔点很接近,可认为是同一种物质)。纯安息香为白色针状结晶,熔点132~137℃,参考熔点:133℃(理论与实际熔点的差异可能是由制得的安息香中所含的杂质导致的)
(二)二苯乙二酮的制备
1、搭建油浴装置,在装有转子、温度计、球型冷凝器的250 mL三颈瓶中,投入二苯乙醇酮8 g(相对分子量为212.24,计算可知加入的二苯乙醇酮为37.69mmol),稀硝酸(HNO3:H2O=1:0.6)20 mL。开动搅拌,用油浴加热,逐渐升温至沸(110℃左右),反应 2 h(反应中硝酸被还原,产生棕红色一氧化氮、二氧化氮气体,溶液颜色加深,后期变为棕色,可从冷凝器顶端装一导管,将其导入0.25mol/L NaOH溶液(取氢氧化钠2.5g配制成250ml溶液)中吸收)。
2、反应结束( 此时体系成上下两层澄清溶液上层棕红色,下层棕黄色),在搅拌下,将反应液慢慢倾入150 mL室温蒸馏水中,搅拌,很快有黄色晶体析出。
3、待析晶完全后抽滤,滤渣用少量冰水洗涤,真空干燥,得到黄绿色块状二苯乙二酮粗品6.197g,测得熔点为88~93℃。(二苯乙二酮:纯品为黄色棱状晶体。 熔点95~96℃。沸点346~348℃(分解),相对密度1.064 ,溶于乙醇、乙醚、丙酮、苯、氯仿等有机溶剂,不溶于水。)

图1 二苯乙二酮的制备装置(油浴,带有干燥管)
(三)苯妥英的制备
1、在装有搅拌、温度计、球型冷凝器的250 mL三颈瓶中,投入二苯乙二酮4 g(相对分子量为210.228,计算可知加入的二苯乙二酮为19.03mmol),脲素1.5 g(无色或白色无臭小片或结晶性粉末,具吸湿性,相对分子量为60.06 ,计算可知加入的脲素为24.975mmol),20% NaOH 12 mL,50% 乙醇20 mL(作溶剂用),开动搅拌,加热至沸(内温100℃左右),回流反应50 min。
2、反应完毕,得到棕色溶液。取下三颈瓶,稍冷,擦干瓶底上残留的油渍,搅拌下将反应液倾入120 mL冷水中(250ml烧杯),得乳黄色悬浊液;
3、加入适量活性炭,水浴(70℃)搅拌脱色15min,然后冷却至室温,有灰色絮状沉淀析出,抽滤,除去副产物。
4、滤液用10% 盐酸(10ml的36%盐酸加入蒸馏水配置成36ml)调至pH 5~6(用去盐酸19ml,溶液中出现乳白色沉淀,),放置一夜后(沉淀变成橘黄色),抽滤,滤渣用少量水洗,干燥,得到橘黄色苯妥英粗品5,145g。(纯净的苯妥英为白色粉末)

图2 苯妥英的制备装置(油浴)
(四)成盐与精制
1、将苯妥英粗品置250 mL烧杯中,按粗品与水为1:4之比例加入20ml水,40℃水浴加热,搅拌下滴加20% NaOH(取氢氧化钠10g配制成50ml溶液)至固体全溶,用去氢氧化钠7ml;
2、加适量活性炭,在搅拌下加热脱色5 min,趁热抽滤(布氏漏斗和抽滤瓶应预热);
3、滤液转移至50ml烧杯中,室温放冷,后冰水冷却,析出大量橘红色结晶,抽滤,滤渣用少量冰水洗涤,真空干燥,得到苯妥英钠1.365g,计算收率。(苯妥英钠:易溶于水,溶于乙醇,几乎不溶于乙醚和氯仿。水溶液显碱性反应,因水解而显浑浊。)
五、实验注意事项
1、VB1在酸性条件下稳定,但易吸水,在水溶液中易被空气氧化失效。遇光和Fe、Cu、Mn等金属离子可加速氧化。在NaOH溶液中嘧唑环易开环失效。因此NaOH溶液在反应前必须用冰水充分冷却,否则,VB1在碱性条件下会分解,这是本实验成败的关键。
2、硝酸为强氧化剂,使用时应避免与皮肤,衣服等接触,氧化过程中,硝酸被还原产生氧化氮气体,该气体具有一定刺激性,故须控制反应温度,以防止反应激烈,大量氧化氮气体逸出。
3、 制备钠盐时,水量稍多,可使收率受到明显影响,要严格按比例加水。
六、 实验现象记录
表四 实验现象记录和现象分析
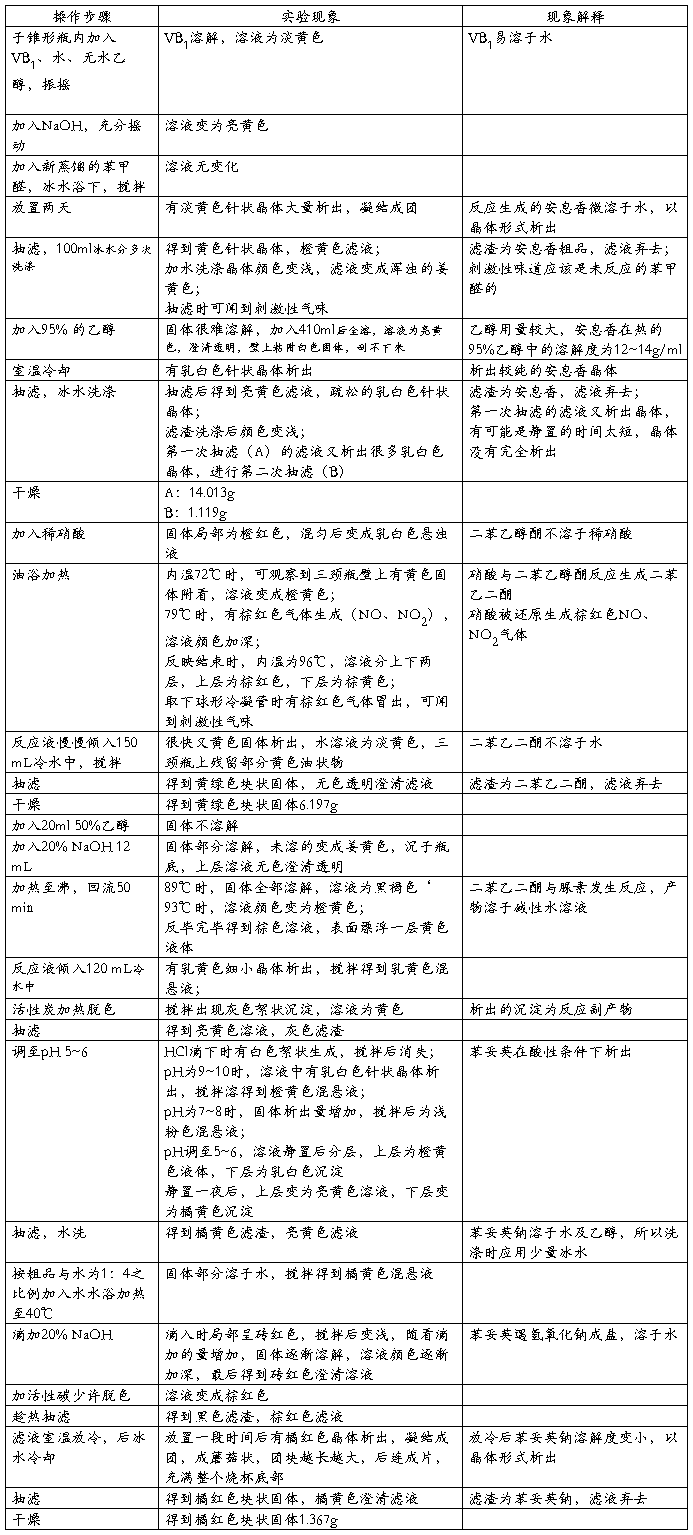
七、 实验结果与分析
根据下述反应方程式计算各步产物的产率
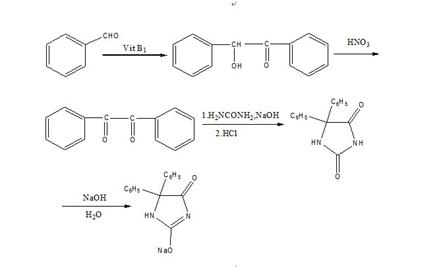
(1)安息香的制备
苯甲醛的相对分子质量 M1=106.12g/mol
相对密度 ρ1=1.0415g/ml
加入的体积 V1=22.5ml
则苯甲醛的摩尔质量 n1=220.8mmol
二苯乙醇酮的相对分子质量 M2=212.24 g/mol
二苯乙醇酮的理论产量 m2=220.8*212.24/1000=46.86g
实际产量 m2,=14.013+1.119=15.132g
产率 15.132/46.86*100%=32.29%
(2)二苯乙二酮的制备
加入的二苯乙醇酮的质量 m3=8g
二苯乙二酮的相对分子质量 M4=210.228g/mol
二苯乙二酮的理论产量 m4=8/212.24*210.228=7.92g
实际产量 m4,=6.197g
产率 6.197/7.92*100%=78.24%
(3)苯妥英的制备
加入的二苯乙二酮的质量 m5=4g
苯妥英钠的相对分子质量 M6= 274.25g/mol
苯妥英钠的理论产量 m6= 4/210.228* 274.25=5.22g
实际产量 m6‘= 1.367g
产率 1.367/5.22*100%=26.19%
表五 实验结果汇总

结果分析
(1) 反应的成功与否跟原料的质量有很大关系,首先苯甲醛不能含有苯甲酸,长期放置的苯甲醛使用前最好用5%碳酸氢钠洗涤后蒸馏,此外,噻胺易潮解,潮解后易被空气氧化而失效,因此,最好采用新鲜的噻胺,但是本实验所用的原料都是直接从瓶子里取的,可能已经放置了很久,不纯了;
(2) 各步反应中反应物部分参加反应;
(3) 安息香缩合反应结束把制得的安息香粗品拿去抽滤时,用滤液洗涤了滤渣一次,以至于得到的滤渣为黄色,再用冰水洗涤多次,仍为黄色,可能滤液中的杂质吸附在了滤渣上,后面的精制过程也没能把它完全除去,制得的安息香纯度下降;
(4) 制得的苯妥英钠刚开始放在鼓风干燥箱中60℃干燥,后来观察到晶体熔化,赶紧取出置于真空干燥箱中。苯妥英钠的实际熔程应295-598℃,但实际测得的熔程为92~100℃,与查到的文献值完全不符。可能在鼓风干燥时苯妥英钠被分解了。
八、 讨论与心得
苯妥英钠的合成过程一般是以苯甲醛为原料经安息香缩合,氧化和环化三步反应制得。在传统制备中,第l步安息香缩合反应中常用氰化物作为催化剂进行,但因为氰化物及氰化酸的致毒性极强,致毒作用极快,空气中氰化氢含量达3/100000,即可在数分钟内致人死亡,大大增加了危险性,目前普遍采用噻胺替代氰化钠催化此缩合反应,条件温和、无毒且产率较高。噻胺是一种具有生物活胜的辅酶,也是一种生物化学反应的催化剂,在生命过程中起重要作用。
催化剂是一种亲核试剂,其吸电子作用是醛基上的H活泼,从而能发生质子交换生成负碳离子是醛基成为亲核试剂,同时催化剂有事很好的离去基,可以脱去。除了氰化物和噻胺,噻唑啉离子、三乙氧基膦、和氯化三甲基硅在LDA存在下、烷基或芳基取代的咪唑啉定也可催化安息香缩合。
反应温度要严加控制,特别是安息香合成开始前期加热不必太快,后期可适当升高温度至沸腾。
附录:维生素B1催化合成安息香机理
1、本次实验使用维生素B1催化安息香缩合反应。维生素B1又称为硫胺素,其结构如下:
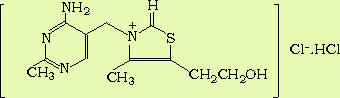
VB1是一个噻唑生成的季铵盐,也可对安息香缩合起催化作用,因此,可以用具有生物活性的VB1的盐酸盐代替氰化物催化安息香缩合反应。
反应时,VB1分子中的噻唑环上的氮原子和硫原子邻位的氢,在碱作用下可生成负碳离子:

硫胺素分子中最主要的部分是噻唑环,噻唑环C2上的氢原子由于受到氮原子核硫原子的影响,具有明显的酸性,在碱的作用下,质子容易被除去,产生的负碳离子作为活性中心。然后与苯甲醛作用生成中间体(形成烯醇中间体):
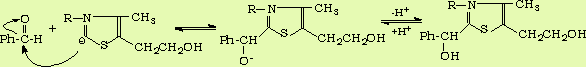
上述中间体可以被分离得到。中间体又经过脱H+得到另一个中间体烯醇,烯醇与另一分子苯甲醛作用就得到了缩合中间体,再经过水解得到产物。

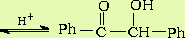
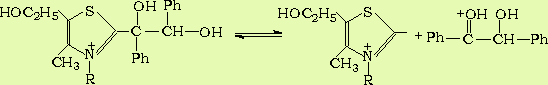
第二篇:苯妥英钠合成实验的改进
2010年38卷第7期广州化工
?97?
苯妥英钠合成实验的改进
陈新
(皖西学院化生系;安徽仿生传感与检测技术省级实验室,安徽六安237012)
摘
要:以苯甲醛为原料,通过安息香缩合,氧化和环合三步合成苯妥英钠,用维生素B。为催化剂,控制pH值为8~9,温度
60℃~70℃,并且在新蒸的苯甲醛中加入适量锌粉制备安息香;氧化步骤中用FeCl,?6H:O代替硝酸,可以使反应在较温和的条件下进行,而且产品收率有所提高。本实验苯妥英钠收率为37.57%。
关键词:苯甲醛;安息香;苯妥英钠;VBl;FeCl3?6心o
Modification
ofSynthesisofPhenytoin
CHENXin
Sodium
(DepartmentofChemistryandLifeScience,WestAnhuiUniversity;LaboratoryofBionicSensors
andDetectionTechnologyofAnhuiProvince,AnhuiLiuan237000,China)
Abstract:Usingbenzaldehyde
as
rawmaterial,phenytoinsodiumwassynthesizedthroughbenzoincondensation,OX—
as
idationandringclosurereaction.Inthepreparationofbenzoin,VBl
at
catalyst,withpH8~9,temperature60℃~70℃,
thesametime,someZincpowderwasaddedintonewstilledbenzaldehyde.Intheoxidationstep,FeCl3?6H20was
as
used
oxidizerinsteadofnitrate.Theexperimentalrestiltsindicatedthatreactions
rate
can
proceedundermoderatecondi—
yieldofphenytoinsodium
tions,furthermore,theproduction
inthisexperimentwas37.57%.
increasedcompared
to
formerexperimentalmethods.The
Keywords:benzaldehyde;benzoin;phenytoin;phenytoinsodium;VBl;FeCl3?6H20
苯妥英钠(5,5一二苯基乙内酰脲钠)在医学上有着广泛的用途,主要用于抗癫痫及抗心律失常疾病的治疗,也可用于治疗慢性支气管炎和哮喘。本实验中以苯甲醛为原料,通过安息香缩合,氧化和环合三步合成苯妥英钠。经典的安息香合成以氰化钠或氰化钾为催化剂,由于氰化钠是剧毒品,使用不当易造成危害。目前普遍采用噻胺替代氰化钠催化此缩合反应,条件温和、无毒且产率较高。硝酸作氧化剂,产生了大量腐蚀性的棕黄色NO:气体,使用FeCl,?6H:O作氧化剂,可避免上述污染。本文对苯妥英钠合成步骤进行了改进,在较温和的条件下得到了较高的产率。1
1.1
1.2主要仪器和试剂
苯甲醛;维生素B1;冰乙酸;FeEl3?6也0;尿素;活性炭;95%乙醇;NaOH溶液,盐酸,磁力加热搅拌器,抽滤装置,熔点测定仪。2
实验方法‘1—5]
2.1安息香的制备
(1)在25mL圆底烧瓶中依次加入29VB。和2mL蒸馏水,摇匀溶解,再加入8mL95%乙醇。冷却至0℃。
(2)取10%NaOH溶液2mL于小锥型瓶中并冷却至O。C。(3)再往圆底烧瓶中加入5mL新蒸的苯甲醛及适量锌粉,充分摇匀,调整反应液的pH值为8~9。
(4)冰浴下将10%NaOH溶液逐滴加入步骤(1)的圆底烧瓶中。
(5)加入几粒沸石,装上回流冷凝管,用60℃~70℃水浴加热1.5h(不能使反应物剧烈沸腾)。反应后期可将水浴为温度
实验部分
实验原理
合成路线如下:
:6
寸l一一心。0≈》…。
万方数据
一C-C。H.--囝旦p8穗勺
升高到80。C~90℃。其间注意摇动反应瓶并保持反应液的pH值为8~9,必要时可滴加10%NaOH溶液。
(6)反应混合物冷至室温后冰水冷却,使结晶析出完全。(7)抽滤,并用冷水洗涤晶体,粗产物可用95%乙醇重结晶,干燥,称重。
2.2联苯甲酰的制备
在25mL圆底烧瓶中加入6.5mL冰乙酸、5mL水、9.09
作者简介:陈新(1972一),男,皖西学院讲师,博士。E—mail:cx810101@163.corn
?98?
广州化工
计算收率。
2010年38卷第7期
FeCl,?6心0,装上回流管,加热至沸腾5min后,再加入自制的安息香,加热并不断搅动。回流1h后,将反应混合物冷至室温,在搅拌下倾入10mL的冰水中,此时即有二苯乙二酮析出。结晶抽滤并用冷水充分洗涤,干燥,称重。
3结果与讨论
3.1
2.3苯妥英的制备
按投料比:二苯乙二酮:尿素:15%NaOH:乙醇:水=19:0.69:3mL:5mL:10mL,将二苯乙二酮、尿素、15%NaOH溶液及乙醇置圆底烧瓶中,安装电磁搅拌,回流冷凝管,加热到100。C,然后分批加入15%NaOH水溶液,回流1.5h后加入计算量的水,得浅黄色溶液,用活性炭脱色,然后冷却至室温,过滤。滤液转移到小烧杯中,水浴控制温度在45。C左右,用5%的盐酸酸化至pH值为5~6,即有大量白色固体出现,充分冷却,抽滤。滤出物用水洗涤,充分干燥,即得苯妥英,称重。
实验结果
3.2讨论
(1)本实验中安息香制备的关键在于调pH值。pH值为7~8时,因维生素B。不能很好发挥活性MJ,产率较低。pH值为9~10时,碱性太强,苯甲醛分子间可能发生康尼查罗反应o“,降低了产率。因此最佳的pH值应为8~9。制备安息香时,本实验中采用先加入VB,,再加入苯甲醛,最后加入NaOH溶液的方法,这样更加有利于控制反应过程中的pH值,不同于文献怛一70中先加入VB。,再加入NaOH溶液,最后加入苯甲醛的方法。在加入苯甲醛的同时加入适量锌粉"J,可以有效地减少苯甲醛被氧化,从而提高产品的收率。另外VB。在酸性条件下稳定,但易吸水,在水溶液中易被空气氧化失效。在NaOH溶液中嘧唑环易开环失效。因此NaOH溶液在反应前必须用冰水充分冷却,否则,VB,在碱性条件下会分解,这是本实验成败的另一关键因素。
2.4成盐与精制
将苯妥英粗品置100mL烧杯中,按粗品与水为1:4之比例加入水,水浴加热至40℃,加入20%NaOH至全溶,加活性碳少许,在搅拌下加热5min,趁热抽滤,滤液加氯化钠至饱和。放冷,析出结晶,抽滤,少量冰水洗涤,干燥得苯妥英钠,测熔点,称重,
表1产品的产量和收率
Table1
Outputandyieldofproducts
(2)目前文献中制备二苯乙二酮采用的催化剂主要有FeCl3?6H:0、硝酸或乙酸和硝酸钠、硫酸铜的混合物,但是使用硝酸或乙酸和硝酸钠、硫酸铜的混合物都会有棕黄色NO:有毒气体生成,使用FeCl,?6H:0作氧化剂可以使反应在较为温和的条件下进行,同时产率也有所提高。若产物呈油状析出,应重新加热溶解,然后静置任其冷却,必要时可用两头封口的毛细管代替玻棒摩擦瓶壁,或放人品种以诱发结晶。
(3)在苯妥英的合成中,应分批加入15%NaOH溶液,若一次性加入,则会产生副反应,使溶液颜色过深,若脱色不完全所得产物呈黄色,且降低产率。本反应直接酸化得到的苯妥英如果是无定形的泥状,则难以烘干,而且不纯。此时可用80%的乙醇进行重结晶,再用乙醇洗涤而纯化,得到苯妥英的白色针状晶体。
妥英钠。用维生素B。为催化剂制备安息香时,VB。和NaOH溶液在反应前必须用冰水充分冷却,同时控制反应液pH值为8~9,这是本实验成败的两个关键因素;氧化步骤中用FeCl,?6心0代替硝酸作为催化剂,可以使反应在较温和的条件下进行,而且产品收率有所提高。在苯妥英的合成中,应分批加入15%NaOH溶液,若一次性加入,则会产生副反应,使溶液颜色过深,若脱色不完全所得产物呈黄色,且降低产率。
参考文献
[1]周隆春主编.精细化工实验法[M].北京:中国石化出版社,1998:
235—236.
[2]冯金城,麦禄诚.苯妥英钠的制备[J].天津大学学报(自然科学
版),2000,20(3):70—72.[3]
杨仕豪,李莉萍,等.苯妥英钠合成工艺改进[J].中国医药工业杂志,1995,26(1):4—5.
[4]何黎琴,见玉娟,等.苯妥英钠合成路线改进[J].安徽化工,2003,
126(6):24—24.
[5]王瑞,孙铁民.沈阳药科大学药物化学教研室编.药物化学实验.
2004:15—18.
4注意事项
(1)维生素B。易吸水,且受热时易分解变质,遇光和Fe、Cu、Mn等金属离子可加速氧化。故应使用新鲜的。不用时应放在冰箱中保存,否则维生素B。在碱性条件下会发生分解,失去活性。
(2)水浴加热时应严格控制温度,切勿加热过剧。5
[6]兰州大学,复旦大学化学系有机化学教研室.有机化学实验(第二
版)[M].北京:高等教育出版社,1994:236—237.
[7]曾昭琼.有机化学(第三版)[M].北京:高等教育出版社,2000:116
—117.
结论
以苯甲醛为原料,通过安息香缩合,氧化和环合三步合成苯
[8]潘英明,黄朗,梁敏,等.安息香的微型制备方法研究[J].内蒙古民
族大学学报(自然科学版),2004,19(3):285—286.
万方数据

苯妥英钠合成实验的改进
作者:
作者单位:
刊名:
英文刊名:
年,卷(期):陈新, CHEN Xin皖西学院化生系;安徽仿生传感与检测技术省级实验室,安徽,六安,237012广州化工GUANGZHOU CHEMICAL INDUSTRY2010,38(7)
参考文献(8条)
1.周隆春 精细化工实验法 1998
2.潘英明;黄玥;梁敏 安息香的微型制备方法研究[期刊论文]-内蒙古民族大学学报(自然科学版) 2004(03)
3.曾昭琼 有机化学 2000
4.兰州大学;复旦大学化学系有机化学教研室 有机化学实验 1994
5.王瑞;孙铁民;沈阳药科大学药物化学教研室 药物化学实验 2004
6.何黎琴;见玉娟 苯妥英钠合成路线改进[期刊论文]-安徽化工 2003(06)
7.杨仕豪;李莉萍 苯妥英钠合成工艺改进 1995(01)
8.冯金城;麦禄诚 苯妥英钠的制备[期刊论文]-天津大学学报(自然科学版) 2000(03)
本文链接:http://d..cn/Periodical_gzhg201007033.aspx
