关于定期安全性更新报告(PSUR)、境外发生的严重
药品不良反应有关事宜的通知
各相关单位:
自20xx年1月1日起,使用“国家药品不良反应监测系统”(下简称“新系统”)上报个例药品不良反应、药品群体不良事件及境外发生的严重药品不良反应。新系统中定期安全性更新报告(PSUR)上报功能尚在开发过程中。现将PSUR及境外发生的严重药品不良反应报告相关事宜通知如下:
一、关于PSUR
(一)PSUR报告方式
1.进口药品PSUR仍继续使用“进口药品不良反应/事件报告监测系统”报告,直到新系统PSUR报告功能开发完成。
2.国产药品PSUR待新系统相关功能开发完成后才能报告。
3.使用新系统报告PSUR时间另行通知。
(二)进口药品PSUR上报网址及权限获取
1.网址:http://114.255.93.205:9080/impadr/。
2.未注册用户获取登陆账号方法
申请用户将单位名称、联系人、电话、电子邮箱名称发送至邮箱impadr@,管理员确认后将登录账号邮件反馈给申请用户。
二、关于境外发生的严重药品不良反应
自20xx年1月1日起,使用新系统报告境外发生的严重药品不良反应,原“进口药品不良反应/事件报告监测系统”中进口药品境外不良反应报告功能停止使用。现对用户通过新系统报告境外发生严重药品不良反应有关情况做如下说明:
(1)不能使用“进口药品不良反应/事件报告监测系统”的用户名和密码登陆新系统。
(2)生产企业如果在“全国药品不良反应监测网络”(2012月1月1日以前使用的不良反应报告网络)中已经注册过用户且可以上报,则在新系统中可以上报境外发生的严重药品不良反应,登录账号为:在 “全国药品不良反应监测网络”登录账号前增加前缀“adr-”,密码为初始化默认,进入系统后请尽早修改密码。
(3)如果生产企业在“全国药品不良反应监测网络”没有注册过,则需要在新系统中注册,通过审核后登录新系统进行上报。
(4)使用新系统报告境外发生严重药品不良反应需首先在系统中添加、维护本企业产品信息(在新系统中重新注册产品信息,具体方法详见新系统公告栏中有关使用手册)。
(5)“进口药品不良反应/事件报告监测系统”完全停止使用后,通过该系统报告的数据将导入到新系统,具体时间另行通知。
三、未尽事宜请联系我们
邱红梅:010-82116450转821
张 霜:010-82116450转822
冯翔宇:028-85153791
侯永芳:010-68586184 QQ群:22032767
特此通知。
第二篇:药品不良反应/事件报告表
附表1 制表单位:国家食品药品监督管理局
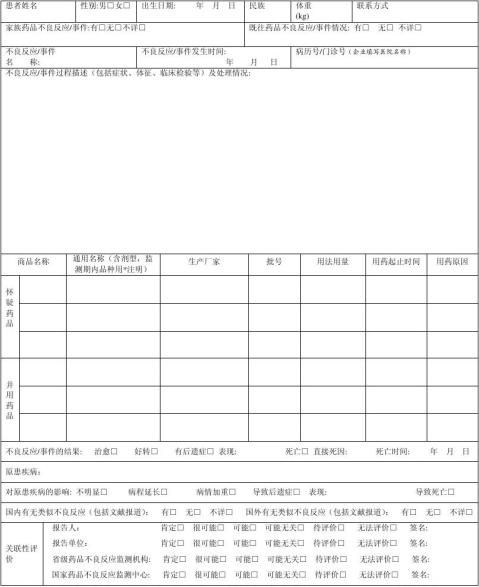
药 品 不 良 反 应 / 事 件 报 告 表
新的□ 严重□一般□ 医疗卫生机构□ 生产企业经营企业□ 个人□ 编码□□□□□□□□□□□□□□□□□□□
单位名称: 部门: 电话: 报告日期: 年 月 日
◇不良反应/事件分析
1. 用药与不良反应/事件的出现有无合理的时间关系? 有□ 无□
2. 反应是否符合该药已知的不良反应类型? 是□ 否□ 不明□
3. 停药或减量后,反应/事件是否消失或减轻? 是□ 否□ 不明□ 未停药或未减量□
4. 再次使用可疑药品后是否再次出现同样反应/事件? 是□ 否□ 不明□ 未再使用□
5. 反应/事件是否可用并用药的作用、患者病情的进展、其他治疗的影响来解释?是□ 否□ 不明□
◇严重药品不良反应/事件是指有下列情形之一者:
① 引起死亡 □
② 致畸、致癌、致出生缺陷 □
③ 对生命有危险并能够导致人体永久的或显著的伤残 □
④ 对器官功能产生永久损伤 □
⑤ 导致住院或住院时间延长 □
◇编码规则:
省(自治区、直辖市) 市(地区) 县(区) 单位 年代 流水号
□□ □□ □□ □□□□ □□□□ □□□□□ 注:省(自治区、直辖市)、市(地区)、县(区)编码按中华人民共和国行政区划代码填写。 单位编码第一位如下填写:医疗机构1、军队医院2、计生机构3、生产企业4、经营企业5。 个人报告单位编码一栏填写6000
◇ 注:通用名称一栏,首次获准进口5年内的进口品种用*注明
国家药品不良反应监测中心 药品不良反应监测中心 通信地址:北京市崇文区法华南里11号楼二层 通信地址:
邮 编:100061 邮 编:
电 话:(010)67164979 电 话:
传 真:(010)67184951 传 真:
E – mail :report@ E – mail:
新的、严重的药品不良反应/事件病例报告要求
药品生产企业报告要求
1. 填报《药品不良反应/事件报告表》;
2. 产品质量检验报告;
3. 药品说明书(进口药品还须报送国外药品说明书);
4. 产品注册、再注册时间,是否在监测期内(进口药是否为首次获准进口5年内);
5. 产品状态(是否是国家基本药物、国家非处方药、国家医疗保险药品、中药保护品种);
6. 国内上年度的销售量和销售范围;
7. 境外使用情况(包括注册国家、注册时间);
8. 变更情况(药品成分或处方、质量标准、生产工艺、说明书变更情况);
9. 国内外临床安全性研究及有关文献报道情况;
10. 除第1、2项以外,其他项目一年之内如无变更,可以免报。
